名校
解题方法
1 .  是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
实验(一)制备 。
。
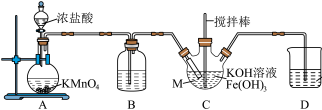
(1)仪器M的名称是_____ ,装置B的作用是_____ 。
(2)装置C中生成 的化学方程式为
的化学方程式为_____ 。
(3)实验得知装置D中吸收的 为装置A中生成
为装置A中生成 的25%,不考虑其他消耗,若装置D中生成的氧化产物只有
的25%,不考虑其他消耗,若装置D中生成的氧化产物只有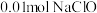 ,则生成
,则生成_____ 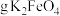 。
。
实验(二)探究 的性质。
的性质。

实验中观察到b中溶液变为蓝色,a中溶液由紫红色变为黄色,并产生气泡。
(4)酸R选择稀硫酸,不选择盐酸,其主要原因是_____ ;酸R选择稀硫酸时,从d口逸出的气体_____ (填“可以”或“不可以”)直接排放至大气中。
(5)当选用硫酸时,装置a中的离子方程式为_____ 。
(6)另设计一种方案确认有 产生:
产生:_____ 。
(7)向另一试管中的 溶液中滴加
溶液中滴加 溶液,溶液变为紫红色。不能证明氧化性:
溶液,溶液变为紫红色。不能证明氧化性: ,其原因是
,其原因是_____ 。
 是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:实验(一)制备
 。
。
(1)仪器M的名称是
(2)装置C中生成
 的化学方程式为
的化学方程式为(3)实验得知装置D中吸收的
 为装置A中生成
为装置A中生成 的25%,不考虑其他消耗,若装置D中生成的氧化产物只有
的25%,不考虑其他消耗,若装置D中生成的氧化产物只有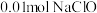 ,则生成
,则生成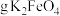 。
。实验(二)探究
 的性质。
的性质。
实验中观察到b中溶液变为蓝色,a中溶液由紫红色变为黄色,并产生气泡。
(4)酸R选择稀硫酸,不选择盐酸,其主要原因是
(5)当选用硫酸时,装置a中的离子方程式为
(6)另设计一种方案确认有
 产生:
产生:(7)向另一试管中的
 溶液中滴加
溶液中滴加 溶液,溶液变为紫红色。不能证明氧化性:
溶液,溶液变为紫红色。不能证明氧化性: ,其原因是
,其原因是
您最近一年使用:0次
2023-09-28更新
|
89次组卷
|
2卷引用:湖南省三湘创新发展联合体2023-2024学年高三上学期9月月考化学试题
名校
解题方法
2 . 实验小组制备高铁酸钾( )并探究其性质。
)并探究其性质。
资料: 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备 。(夹持装置略)
。(夹持装置略)
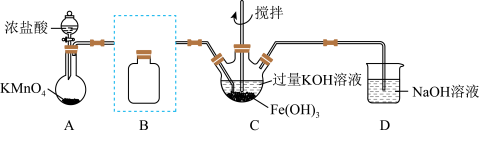
①A为氯气发生装置,A中反应的离子方程式是_______ 。
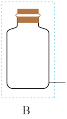
②将除杂装置B补充完整并标明所用试剂_______ 。
③C中得到紫色固体和溶液,C中 发生的反应有
发生的反应有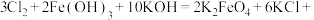
 ,另外还有
,另外还有_______ 。
(2)探究 的性质
的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
ⅰ.向沸水中逐滴滴加1mol/L  溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是_______ nm。
ⅱ.由方案上可知a中含有 离子,但该离子的产生不能判断一定是
离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由_______ 产生(用离子方程式表示)。
ⅲ.方案Ⅱ可证明 氧化了
氧化了 用KOH溶液洗涤的目的是
用KOH溶液洗涤的目的是_______ 。
②根据 的制备实验得出:氧化性
的制备实验得出:氧化性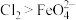 ,而方案Ⅱ实验表明,
,而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因可能是
的氧化性强弱关系相反,原因可能是_______ 。
 )并探究其性质。
)并探究其性质。资料:
 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)制备
 。(夹持装置略)
。(夹持装置略)
①A为氯气发生装置,A中反应的离子方程式是
②将除杂装置B补充完整并标明所用试剂

③C中得到紫色固体和溶液,C中
 发生的反应有
发生的反应有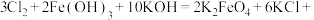
 ,另外还有
,另外还有(2)探究
 的性质
的性质①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有
 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:| 方案Ⅰ | 取少量a,经过检验溶液中含有 。 。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 溶出,得到紫色溶液b,取少量b,滴加盐酸,有 溶出,得到紫色溶液b,取少量b,滴加盐酸,有 产生。 产生。 |
 溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是ⅱ.由方案上可知a中含有
 离子,但该离子的产生不能判断一定是
离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由ⅲ.方案Ⅱ可证明
 氧化了
氧化了 用KOH溶液洗涤的目的是
用KOH溶液洗涤的目的是②根据
 的制备实验得出:氧化性
的制备实验得出:氧化性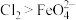 ,而方案Ⅱ实验表明,
,而方案Ⅱ实验表明, 和
和 的氧化性强弱关系相反,原因可能是
的氧化性强弱关系相反,原因可能是
您最近一年使用:0次
名校
解题方法
3 . 某硫酸厂以硫铁矿焙烧后的烧渣(其主要成分为 、
、 、
、 )为原料来制取铵明矾晶体
)为原料来制取铵明矾晶体 的一种工艺流程如图。
的一种工艺流程如图。
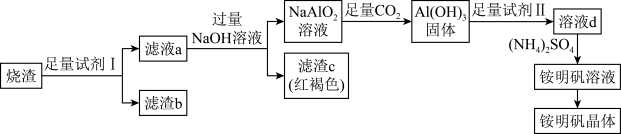
已知:① 是酸性氧化物,难溶于水,酸浸时不发生反应。
是酸性氧化物,难溶于水,酸浸时不发生反应。
② 固体可溶于
固体可溶于 等强碱溶液。
等强碱溶液。
请回答下列问题:
(1)写出 中含有的化学键类型:
中含有的化学键类型:_______ 。
(2)“试剂Ⅰ”为_______ (填试剂名称),“滤渣b”为_______ (填化学式)。
(3)写出“滤液a”和 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 、_______ 。
(4)“滤渣c”的化学式为_______ ,证明铁元素已沉淀完全的实验方法是_______ 。
(5)向 溶液中通入足量
溶液中通入足量 的离子方程式为
的离子方程式为_______ 。
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、_______ (填操作名称)、洗涤、干燥。
 、
、 、
、 )为原料来制取铵明矾晶体
)为原料来制取铵明矾晶体 的一种工艺流程如图。
的一种工艺流程如图。
已知:①
 是酸性氧化物,难溶于水,酸浸时不发生反应。
是酸性氧化物,难溶于水,酸浸时不发生反应。②
 固体可溶于
固体可溶于 等强碱溶液。
等强碱溶液。请回答下列问题:
(1)写出
 中含有的化学键类型:
中含有的化学键类型:(2)“试剂Ⅰ”为
(3)写出“滤液a”和
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)“滤渣c”的化学式为
(5)向
 溶液中通入足量
溶液中通入足量 的离子方程式为
的离子方程式为(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、
您最近一年使用:0次
名校
4 . 根据元素周期表和元素周期律,回答下列问题。
Ⅰ.将NaOH溶液和NH4Cl溶液混合生成NH3·H2O,验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______ 。
Ⅱ.A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: ,B、C可形成两种离子化合物B2C和B2C2.据此填空:
,B、C可形成两种离子化合物B2C和B2C2.据此填空:
(1)A的元素名称为_______ ,位于第_______ 周期_______ 族。
(2)A、C、D气态氢化物稳定性由强到弱的顺序是(填化学式)_______ 。
(3)A、B形成的含氧酸盐与D最高价氧化物对应的水化物反应的方程式是_______ 。
(4)利用下图装置若要证明非金属性:C>Si,则A中加_______ ,B中加Na2CO3、C中加_______ ,观察到C中溶液的现象为_______ 。

Ⅰ.将NaOH溶液和NH4Cl溶液混合生成NH3·H2O,验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:
Ⅱ.A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为:
 ,B、C可形成两种离子化合物B2C和B2C2.据此填空:
,B、C可形成两种离子化合物B2C和B2C2.据此填空:(1)A的元素名称为
(2)A、C、D气态氢化物稳定性由强到弱的顺序是(填化学式)
(3)A、B形成的含氧酸盐与D最高价氧化物对应的水化物反应的方程式是
(4)利用下图装置若要证明非金属性:C>Si,则A中加

您最近一年使用:0次
5 . 下表是元素周期表的一部分,①~⑫分别代表12种元素,请回答:
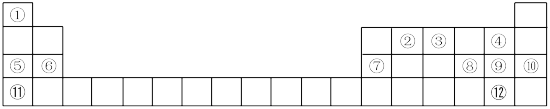
(1)写出12种元素中化学性质最不活泼的元素的原子结构示意图______________ 。
(2)⑪在元素周期表中的位置是____________________________ 。
(3)12种元素形成的单质中硬度最大的是________________ (填名称)。
(4)用电子式表示①与⑪形成化合物的过程_______________________ 。
(5)可以用来验证⑥⑦两种元素金属性强弱的实验是__________ (填字母序号)。
a 将在空气中放置已久的这两种元素的块状单质分别放入水中
b 将形状、大小相同的无氧化膜的这两种元素的单质分别和同浓度同体积的盐酸反应
c 将形状、大小相同的无氧化膜的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d 比较这两种元素的氢化物的热稳定性
(6)⑧⑨两种元素的简单阴离子中还原性较强的是________ (填离子名称);用一个置换反应证明这一结论__________________________ (写化学方程式)。

(1)写出12种元素中化学性质最不活泼的元素的原子结构示意图
(2)⑪在元素周期表中的位置是
(3)12种元素形成的单质中硬度最大的是
(4)用电子式表示①与⑪形成化合物的过程
(5)可以用来验证⑥⑦两种元素金属性强弱的实验是
a 将在空气中放置已久的这两种元素的块状单质分别放入水中
b 将形状、大小相同的无氧化膜的这两种元素的单质分别和同浓度同体积的盐酸反应
c 将形状、大小相同的无氧化膜的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d 比较这两种元素的氢化物的热稳定性
(6)⑧⑨两种元素的简单阴离子中还原性较强的是
您最近一年使用:0次
解题方法
6 . 铝是重要的金属材料,铝土矿(主要成分A12O3另含少量的SiO2、Fe2O3等)是工业上制铝的原料。实验室模拟工业上以铝土矿为原料制取铵明矾晶体 [NH4Al(SO4)2·12H2O]的工艺流程如下图所示:

请回答下列问题:
(1)为提高铝土矿与盐酸的反应速率,可采取的措施有______________________________ (写两条)。
(2)固体a的主要成分为__________________ (写化学式)。
(3)II中烧碱过量的原因是________________________________________ 。
(4)写出III中主要反应的离子方程式__________________________________________ 。
(5)制取铵明矾溶液的化学方程式为_________________________________________ ;由铵明矾溶液制取铵明矾晶体的实验操作依次为(填操作名称)______________________ 、____________ 、过滤、洗涤。
(6)设计实验证明铵明矾溶液中含有NH4+_______________________________________ 。

请回答下列问题:
(1)为提高铝土矿与盐酸的反应速率,可采取的措施有
(2)固体a的主要成分为
(3)II中烧碱过量的原因是
(4)写出III中主要反应的离子方程式
(5)制取铵明矾溶液的化学方程式为
(6)设计实验证明铵明矾溶液中含有NH4+
您最近一年使用:0次
名校
7 . A、B、C、D、E、F六种元素为原子序数依次增大的短周期元素。A为原子半径最小的元素,A和B可形成4原子10电子的分子X;C的最外层电子数是内层的3倍;D原子的最外层电子数是最内层电子数的一半;E是地壳中含量最多的金属元素;F元素的最高正价与最低负价代数和为6。请回答下列问题:(用化学用语填空)
(1)B、C、D、E、F五种元素原子半径由大到小的顺序是________ 。
(2)A和C按原子个数比1:1形成4原子分子Y,Y的结构式是________ 。
(3)B、C两种元素的简单气态氢化物结合质子的能力较强的为________ (填化学式),用一个离子方程式证明:________ 。
(4)D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式________ 。
(5)实验证明,熔融的EF3不导电,其原因是________ 。
(1)B、C、D、E、F五种元素原子半径由大到小的顺序是
(2)A和C按原子个数比1:1形成4原子分子Y,Y的结构式是
(3)B、C两种元素的简单气态氢化物结合质子的能力较强的为
(4)D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式
(5)实验证明,熔融的EF3不导电,其原因是
您最近一年使用:0次
名校
解题方法
8 . 某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
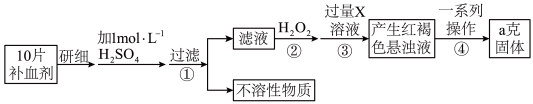
请回答下列问题:
Ⅰ、
(1)实验时用 的浓硫酸,配制100mL
的浓硫酸,配制100mL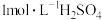 溶液,所需浓硫酸的体积为
溶液,所需浓硫酸的体积为___________ mL(计算结果精确到小数点后一位)。
(2)下列操作中,容量瓶所具备的功能有___________(填序号)。
(3)在下列配制过程示意图中,有错误的是(填写序号)___________ 。
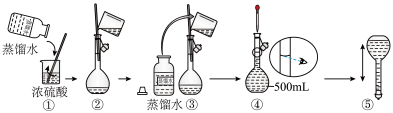
(4)下列说法正确的___________。
Ⅱ、
(5)步骤②加入过量 的目的:
的目的:___________ 。发生反应的离子方程式为:___________ 。
(6)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a、___________ ,b、洗涤,c、灼烧,d、冷却
(7)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为___________ g。

请回答下列问题:
Ⅰ、
(1)实验时用
 的浓硫酸,配制100mL
的浓硫酸,配制100mL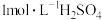 溶液,所需浓硫酸的体积为
溶液,所需浓硫酸的体积为(2)下列操作中,容量瓶所具备的功能有___________(填序号)。
| A.配制一定体积准确浓度的标准溶液 | B.长期贮存溶液 |
| C.用来溶解固体溶质 | D.常用来代替量筒量取一定体积的液体 |

(4)下列说法正确的___________。
| A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差 |
| B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低 |
| C.定容时仰视观察,所配溶液浓度会偏低 |
| D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可 |
Ⅱ、
(5)步骤②加入过量
 的目的:
的目的:(6)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a、
(7)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为
您最近一年使用:0次
2023-01-10更新
|
195次组卷
|
3卷引用:湖南省邵阳市第二中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
9 . 常温时在刚性容器内部有一个不漏气,且可滑动的活塞将容器分成左右两室。左室充入1molN2,右室充入H2与O2的混合气体,活塞恰好停留在离左端四分之一处,然后引燃氢、氧混合气体,反应完毕后恢复至原来温度,活塞恰好停在中间,忽略水的体积,下列说法错误的是
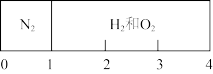
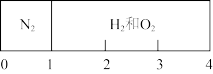
| A.反应前,右室充入H2与O2共3mol |
| B.反应完毕后,恢复至原来温度,左室的压强变为原来的一半 |
| C.反应完毕后,右室剩余气体中含有NA个原子 |
| D.反应前,H2与O2的体积比是4:5或7:2 |
您最近一年使用:0次
2022-11-29更新
|
521次组卷
|
2卷引用:湖南长沙麓山国际实验中学2022-2023学年高一上学期期末线上化学试题
名校
解题方法
10 . 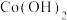 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用 盐酸将其恰好完全溶解,得到
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是

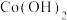 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用 盐酸将其恰好完全溶解,得到
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
A.290℃时,若固体中只含有两种元素,则为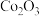 |
B.400℃时, |
| C.500℃时,固体中氧元素质量分数约为26.6% |
| D.生成的黄绿色气体可用于工业上生产“84”消毒液 |
您最近一年使用:0次
2022-10-18更新
|
528次组卷
|
3卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高三上学期月考化学试题(二)



