1 . 现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。 试回答下列问题:
(1)其中操作正确的同学是_______ ,写出此过程中的化学方程式:_______ ;
(2)证明有Fe(OH)3胶体生成的最简单实验操作是_______ ;
(3)Fe(OH)3胶体能不能透过滤纸:_______ (填“能”或“不能”)。
(4)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带_______ 电荷。
②向其中加入饱和Na2SO4溶液,产生的现象是_______ ;
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为______ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式_______ ;
④欲除去Fe(OH)3胶体中混有的NaCl,所用仪器物品是______ ;操作名称是______ 。
I.甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。 试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的最简单实验操作是
(3)Fe(OH)3胶体能不能透过滤纸:
(4)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
②向其中加入饱和Na2SO4溶液,产生的现象是
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
④欲除去Fe(OH)3胶体中混有的NaCl,所用仪器物品是
您最近一年使用:0次
2022-12-15更新
|
285次组卷
|
2卷引用:云南省昆明北大博雅实验中学2021-2022学年高一上学期第一次月考化学试题
解题方法
2 . 如表列出了①~⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是____ (填写化学式)。
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为____ (用元素符号表示)。
(3)元素①的气态氢化物的电子式是____ 。
(4)元素③的原子结构示意图是___ ,元素⑤的单质导电性介于导体和绝缘体之间。因此是一种良好的____ 材料。
(5)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为____ 。
(6)用离子方程式证明⑦⑧两素非金属性的强弱_____ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑦ | |||
| 4 | ⑥ | ⑧ |
(1)②、③、④三种元素的最高价氧化物对应的水化物,其中碱性最强的是
(2)②、③、⑥三种元素按原子半径由大到小的顺序排列为
(3)元素①的气态氢化物的电子式是
(4)元素③的原子结构示意图是
(5)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(6)用离子方程式证明⑦⑧两素非金属性的强弱
您最近一年使用:0次
名校
3 . 某工厂的工业废水中含有大量的 和
和 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收
,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 和金属
和金属 。请回答相关问题:
。请回答相关问题:
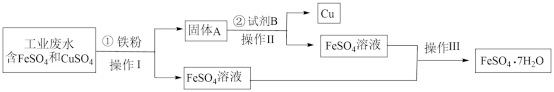
(1)操作I分离方法的名称是___________ 。
(2)实验室模拟操作II使用的主要玻璃仪器有___________ 种。
(3)为得到纯净的铜需要进行洗涤,请简述如何证明洗涤干净___________ 。
(4)从 溶液中得到
溶液中得到 的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为
的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为___________ 。
(5)流程图中, 溶液只含有
溶液只含有 而不含
而不含 ,可证明该事实的实验方法是
,可证明该事实的实验方法是______ (填序号)。
①先加氯水,后加 溶液后显红色
溶液后显红色
②先加 溶液,不显红色,再加氯水后显红色
溶液,不显红色,再加氯水后显红色
③只滴加 溶液不显红色
溶液不显红色
 和
和 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收
,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 和金属
和金属 。请回答相关问题:
。请回答相关问题:
(1)操作I分离方法的名称是
(2)实验室模拟操作II使用的主要玻璃仪器有
(3)为得到纯净的铜需要进行洗涤,请简述如何证明洗涤干净
(4)从
 溶液中得到
溶液中得到 的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为
的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为(5)流程图中,
 溶液只含有
溶液只含有 而不含
而不含 ,可证明该事实的实验方法是
,可证明该事实的实验方法是①先加氯水,后加
 溶液后显红色
溶液后显红色②先加
 溶液,不显红色,再加氯水后显红色
溶液,不显红色,再加氯水后显红色③只滴加
 溶液不显红色
溶液不显红色
您最近一年使用:0次
2022-01-24更新
|
138次组卷
|
2卷引用:云南省镇沅彝族哈尼族拉祜族自治县第一中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
4 . 现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,B为日常生活中最常见的无色无味液体,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,G为黄绿色气体单质,H是漂白液的有效成分,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。
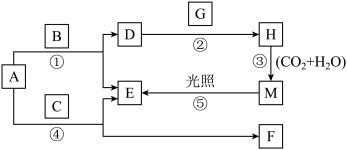
请回答下列问题:
(1)写出H的化学式:___________ 。F的俗名是___________ 。
(2)①写出反应⑤的化学方程式:___________ 。
②写出反应④的化学方程式:___________ 。
(3)利用下图装置进行实验,证明氧化性强弱: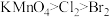 。限选试剂:
。限选试剂: 溶液、
溶液、 、浓盐酸。
、浓盐酸。
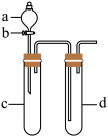
已知: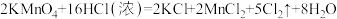 。
。
请回答下列问题:
①如何将装置a中的液体加入c中___________ ,
②d中发生反应的离子方程式为___________ 。
③该装置存在一个缺陷,如何改进___________ 。

请回答下列问题:
(1)写出H的化学式:
(2)①写出反应⑤的化学方程式:
②写出反应④的化学方程式:
(3)利用下图装置进行实验,证明氧化性强弱:
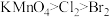 。限选试剂:
。限选试剂: 溶液、
溶液、 、浓盐酸。
、浓盐酸。
已知:
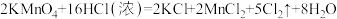 。
。请回答下列问题:
①如何将装置a中的液体加入c中
②d中发生反应的离子方程式为
③该装置存在一个缺陷,如何改进
您最近一年使用:0次
名校
解题方法
5 . 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:

①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO+5HCl
可能发生的副反应:
C2H5OH + HCl → C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
(1)仪器a中盛放的试剂是_____ ;装置B的作用是__________ 。
(2)若撤去装置C,可能导致装置D中副产物________ (填化学式)的量增加;装置D可采用_________ 加热的方法以控制反应温度在70℃左右。
(3)装置E中可能发生的无机反应的离子方程式有____________________ 。
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行,为什么?_______________
(5)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol·L-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 mol·L-1 Na2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为_________ 。
滴定的反应原理:CCl3CHO +OH- → CHCl3 + HCOO-、 HCOO-+ I2 =H+ + 2I- + CO2↑ I2 + 2S2O32- = 2I-+ S4O62-
(6)请设计实验证明三氯乙酸的酸性比乙酸强。__________________

①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO+5HCl
可能发生的副反应:
C2H5OH + HCl → C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水,可溶于乙醇 |
(1)仪器a中盛放的试剂是
(2)若撤去装置C,可能导致装置D中副产物
(3)装置E中可能发生的无机反应的离子方程式有
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行,为什么?
(5)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol·L-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 mol·L-1 Na2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为
滴定的反应原理:CCl3CHO +OH- → CHCl3 + HCOO-、 HCOO-+ I2 =H+ + 2I- + CO2↑ I2 + 2S2O32- = 2I-+ S4O62-
(6)请设计实验证明三氯乙酸的酸性比乙酸强。
您最近一年使用:0次
2020-04-03更新
|
556次组卷
|
3卷引用:云南省曲靖市第一中学2020届高三第二次模拟考试(全国III)理综化学试题
名校
解题方法
6 . 制备某无机化合物的转化流程如图所示,下列说法错误的是


A.该转化流程中 均被循环使用,是催化剂 均被循环使用,是催化剂 |
| B.该循环过程中未涉及氧化还原反应 |
C.存在反应 |
| D.该工艺是利用食盐和石灰石制取纯碱 |
您最近一年使用:0次
2024-01-07更新
|
97次组卷
|
2卷引用: 云南省曲靖市罗平县第一中学2023-2024学年高一上学期期中考试化学试题
7 . I.无水四氯化锡(SnCl4)用于制作FTO导电玻璃,FTO导电玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等领域,可用如图所示装置制备四氯化锡。
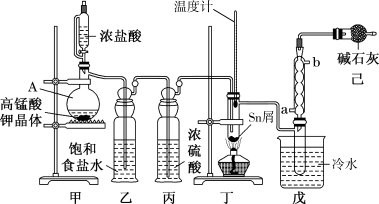
有关信息如下表所示:
(1)仪器A中发生反应的化学方程为_______ 。
(2)将装置按图示连接好,先检在装置的气密性,再慢慢滴入浓盐酸,待观察到装置丁内充满黄绿色气体后,开始加热装置丁。如果缺少装置乙,装置丁内还可能发生的副反应的化学方程式为_______ ,装置已的作用是_______ 。
II.FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了以下实验:
i.实验需要90mL0.10mol·L-1FeBr2溶液
(3)配制FeBr2溶液除烧杯、量筒、玻璃棒、胶头滴管外还需要的玻璃仪器是_______ 。
(4)下列有关配制过程的说法正确的是_______(填序号)。
ii.探究FeBr2的还原性。取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
(5)请你完成下表,验证假设
已知:①Br2易溶于有机溶剂四氯化碳(CCl4)且所得溶液呈橙红色;②四氯化碳(CCl4)不溶于水且密度比水大。
(6)若假设2正确,向20L上述浓度的FeBr2溶液中通入标准状况下56LCl2,反应的离子方程式为_______ 。

有关信息如下表所示:
| 化学式 | Sn | SnCl2 | SnCl4 |
| 熔点/°C | 232 | 247 | -34 |
| 沸点/°C | 2602 | 623 | 114 |
| 其他性质 | 银白色固体 | 无色晶体,Sn2+易被Fe3+、I2等氧化为Sn4+ | 无色液体,易溶于水并能与水反应 |
(2)将装置按图示连接好,先检在装置的气密性,再慢慢滴入浓盐酸,待观察到装置丁内充满黄绿色气体后,开始加热装置丁。如果缺少装置乙,装置丁内还可能发生的副反应的化学方程式为
II.FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了以下实验:
i.实验需要90mL0.10mol·L-1FeBr2溶液
(3)配制FeBr2溶液除烧杯、量筒、玻璃棒、胶头滴管外还需要的玻璃仪器是
(4)下列有关配制过程的说法正确的是_______(填序号)。
| A.用托盘天平称量质量为1.944g的FeBr2 |
| B.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解 |
| C.洗涤溶解FeBr2的烧杯和玻璃棒,并将洗涤液转移至容量瓶中 |
| D.容量瓶贴签存放配好的FeBr2溶液 |
ii.探究FeBr2的还原性。取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
(5)请你完成下表,验证假设
已知:①Br2易溶于有机溶剂四氯化碳(CCl4)且所得溶液呈橙红色;②四氯化碳(CCl4)不溶于水且密度比水大。
| 实验步骤、预期现象 | 结论 |
| ①取适量溶液于试管中,向其中加入 现象:溶液分层,下层呈橙红色,上层呈无色 | 假设1正确 |
| ②另取适量溶液于试管中,向其中加入 现象:溶液变为红色 | 假设2正确 |
您最近一年使用:0次
8 . 二氧化氯具有杀菌消毒作用,是一种广谱型消毒剂。工业上常用 氧化
氧化 制得,方程式为:
制得,方程式为: ,下列相关说法正确的是
,下列相关说法正确的是
 氧化
氧化 制得,方程式为:
制得,方程式为: ,下列相关说法正确的是
,下列相关说法正确的是A.反应中 被氧化 被氧化 | B.消耗5个 时,转移5个电子 时,转移5个电子 |
C. 是还原产物 是还原产物 | D.还原剂与氧化剂的计量系数之比为1∶2 |
您最近一年使用:0次
9 . 同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,说法正确的是
①分子数之比为11:16②摩尔质量之比为11:16③物质的量之比为16:11④原子个数之比为11:16
①分子数之比为11:16②摩尔质量之比为11:16③物质的量之比为16:11④原子个数之比为11:16
| A.①③ | B.①④ | C.②③ | D.②④ |
您最近一年使用:0次
名校
10 . 向59.2 g Fe2O3和FeO的混合物中加入某浓度的稀硝酸1.0 L,固体物质完全反应,生成NO和Fe(NO3)3。在所得溶液中加入1.0 mol/L的NaOH溶液2.8 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为85.6 g。下列有关说法错误的是
| A.Fe2O3与FeO的物质的量之比为1∶6 |
| B.硝酸的物质的量浓度为3.0 mol/L |
| C.产生的NO在标准状况下的体积为4.48 L |
| D.Fe2O3,FeO与硝酸反应后剩余HNO3为0.2 mol |
您最近一年使用:0次
2016-11-17更新
|
3612次组卷
|
21卷引用:云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题
云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题2016届辽宁省沈阳市第二中学高三10月月考化学试卷2016届湖南省衡阳市第八中学高三上学期第三次月考化学试卷2017届湖南省衡阳八中高三上学期9月月考化学试卷2017届辽宁省瓦房店市高级中学高三上10月月考化学试卷四川省眉山中学2018届高三10月月考理科综合化学试题甘肃省天水市第一中学2017-2018学年度上学期高三第三阶段考试化学试题甘肃省天水市一中2018届高三上学期第三学段考试化学试题(已下线)《2018,我的高考我的教师君》-【临考技能篇】速解高考题——高考化学题型分类技巧指导(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密四川省广安市第二中学2019届高三上学期第一次月考化学试题(已下线)考点05 氧化还原反应——备战2019年浙江新高考化学考点(已下线)2019年1月16日 《每日一题》高考二轮复习-铁及其化合物湖南省长沙市雅礼中学2020-2021学年高一下学期期中考试化学试题浙江省台州市书生中学2021-2022学年高一下学期阶段性测试(3月)化学试题湖南省邵阳市第二中学2021-2022学年高一下学期期中考试化学试题湖南省邵东市第一中学2021-2022学年高一下学期第三次月考化学试题辽宁省实验中学2022-2023学年高三上学期期中考试化学试题江西省宜春市丰城拖船中学2023-2024学年高三上学期11月期中化学试题河南省周口市太康县第一高级中学2023-2024学年高一下学期4月第三次月考化学试题



