1 . 下图为氯化钠在不同状态下的导电实验微观示意图(X、Y都是石墨电极)。下列说法不正确 的是
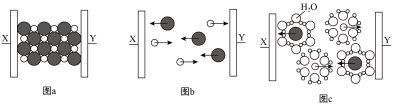

A.图示中的 代表的是 代表的是 | B.图a表示氯化钠固体,不导电 |
| C.图b表示氯化钠熔融时离子键被破坏 | D.图c能证明氯化钠溶液是电解质 |
您最近一年使用:0次
名校
解题方法
2 . 某小组设计实验探究 和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
回答下列问题:
(1)装置B中试剂是________ (填名称),装置E的作用是____________ 。
(2)装置A中反应的离子方程式为______________ 。
(3)能证明氯的非金属性比硫强的实验现象是___________ 。经检验装置C中最终生成了 ,写出C中浑浊变澄清时反应的化学方程式:
,写出C中浑浊变澄清时反应的化学方程式:____________ 。
(4)根据装置D中现象,有人认为 被氧化了。请你设计实验证明他的观点是否正确:
被氧化了。请你设计实验证明他的观点是否正确:____________ 。
(5)实验完毕后,利用下列装置测定装置A中剩余盐酸的浓度:
将装置A中剩余溶液过滤,取 滤液进行实验,最终收集
滤液进行实验,最终收集 的体积为
的体积为 (已折合成标准状况)。
(已折合成标准状况)。
a.读数 b.冷却至室温 c.调平量气管和烧杯的液面
正确操作步骤的顺序为________ (填字母)。
②能与 反应的最低盐酸浓度为
反应的最低盐酸浓度为________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
回答下列问题:
(1)装置B中试剂是
(2)装置A中反应的离子方程式为
(3)能证明氯的非金属性比硫强的实验现象是
 ,写出C中浑浊变澄清时反应的化学方程式:
,写出C中浑浊变澄清时反应的化学方程式:(4)根据装置D中现象,有人认为
 被氧化了。请你设计实验证明他的观点是否正确:
被氧化了。请你设计实验证明他的观点是否正确:(5)实验完毕后,利用下列装置测定装置A中剩余盐酸的浓度:
将装置A中剩余溶液过滤,取
 滤液进行实验,最终收集
滤液进行实验,最终收集 的体积为
的体积为 (已折合成标准状况)。
(已折合成标准状况)。
a.读数 b.冷却至室温 c.调平量气管和烧杯的液面
正确操作步骤的顺序为
②能与
 反应的最低盐酸浓度为
反应的最低盐酸浓度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-04-04更新
|
634次组卷
|
5卷引用:河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题
河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题河南省濮阳市2024届高三第一次模拟考试理综-化学试题山西省晋中市2024届高三第二次优生测试理综合化学试题-(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届河南省鹤壁市高中高三下学期模拟预测化学试题
名校
解题方法
3 . 小组同学探究 和不同铜盐溶液的反应,实验如下。
和不同铜盐溶液的反应,实验如下。
实验:向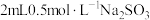 溶液中加入
溶液中加入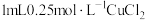 溶液,立即产生橙黄色沉淀(沉淀A),放置
溶液,立即产生橙黄色沉淀(沉淀A),放置 左右,转化为白色沉淀(沉淀B)。
左右,转化为白色沉淀(沉淀B)。
已知:i.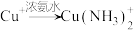 (无色)
(无色)
ii.
(1)研究沉淀B的成分。
向洗涤后的沉淀B中加入足量浓氨水,得到无色溶液,在空气中放置一段时间,溶液变为深蓝色。取少量深蓝色溶液,滴加试剂X,产生白色沉淀。
①白色沉淀是 ,试剂X是
,试剂X是_______ 。
②无色溶液在空气中放置变为深蓝色,反应的离子方程式为_______ 。
(2)经检验,沉淀A不含 。推测沉淀A能转化为沉淀B与
。推测沉淀A能转化为沉淀B与 有关,为研究沉淀A的成分及沉淀A转化为B的原因,实验如下。
有关,为研究沉淀A的成分及沉淀A转化为B的原因,实验如下。 ,补充实验:向少量洗净的沉淀A中加入稀硫酸,证实沉淀A中含有
,补充实验:向少量洗净的沉淀A中加入稀硫酸,证实沉淀A中含有 的证据是
的证据是_______ 。
②无色溶液中含有 ,推测
,推测 的产生有两个途径:
的产生有两个途径:
途径1:实验过程中 氧化
氧化 ;
;
途径2:_______ (将途径补充完整)。
经研究,途径1不合理,途径2合理。
③解释 和
和 溶液反应时,先产生橙黄色沉淀,再转化为白色的原因:
溶液反应时,先产生橙黄色沉淀,再转化为白色的原因:_______ 。
(3) 和
和 溶液反应最终生成
溶液反应最终生成 沉淀,并检测到有
沉淀,并检测到有 生成,离子方程式是
生成,离子方程式是_______ 。用 和
和 溶液重复上述实验,仅产生橙黄色沉淀,放置
溶液重复上述实验,仅产生橙黄色沉淀,放置 后变为暗红色沉淀(可溶于氨水,得到无色溶液,放置变为深蓝色)。
后变为暗红色沉淀(可溶于氨水,得到无色溶液,放置变为深蓝色)。
(4)根据上述实验所得结论:_______ (答出两点)。
 和不同铜盐溶液的反应,实验如下。
和不同铜盐溶液的反应,实验如下。实验:向
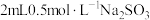 溶液中加入
溶液中加入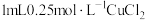 溶液,立即产生橙黄色沉淀(沉淀A),放置
溶液,立即产生橙黄色沉淀(沉淀A),放置 左右,转化为白色沉淀(沉淀B)。
左右,转化为白色沉淀(沉淀B)。已知:i.
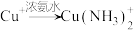 (无色)
(无色)ii.

(1)研究沉淀B的成分。
向洗涤后的沉淀B中加入足量浓氨水,得到无色溶液,在空气中放置一段时间,溶液变为深蓝色。取少量深蓝色溶液,滴加试剂X,产生白色沉淀。
①白色沉淀是
 ,试剂X是
,试剂X是②无色溶液在空气中放置变为深蓝色,反应的离子方程式为
(2)经检验,沉淀A不含
 。推测沉淀A能转化为沉淀B与
。推测沉淀A能转化为沉淀B与 有关,为研究沉淀A的成分及沉淀A转化为B的原因,实验如下。
有关,为研究沉淀A的成分及沉淀A转化为B的原因,实验如下。
 ,补充实验:向少量洗净的沉淀A中加入稀硫酸,证实沉淀A中含有
,补充实验:向少量洗净的沉淀A中加入稀硫酸,证实沉淀A中含有 的证据是
的证据是②无色溶液中含有
 ,推测
,推测 的产生有两个途径:
的产生有两个途径:途径1:实验过程中
 氧化
氧化 ;
;途径2:
经研究,途径1不合理,途径2合理。
③解释
 和
和 溶液反应时,先产生橙黄色沉淀,再转化为白色的原因:
溶液反应时,先产生橙黄色沉淀,再转化为白色的原因:(3)
 和
和 溶液反应最终生成
溶液反应最终生成 沉淀,并检测到有
沉淀,并检测到有 生成,离子方程式是
生成,离子方程式是 和
和 溶液重复上述实验,仅产生橙黄色沉淀,放置
溶液重复上述实验,仅产生橙黄色沉淀,放置 后变为暗红色沉淀(可溶于氨水,得到无色溶液,放置变为深蓝色)。
后变为暗红色沉淀(可溶于氨水,得到无色溶液,放置变为深蓝色)。(4)根据上述实验所得结论:
您最近一年使用:0次
2023-05-07更新
|
1280次组卷
|
3卷引用:北京市朝阳区2022-2023年高三下学期第二次模拟考试化学试题
解题方法
4 . 含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取 的化学方程式为
的化学方程式为_______ 。
(2)实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为_______ 。

(3)某氯水久置后不能使品红溶液褪色,可推测氯水中_______ 已分解。检验此久置氯水中 存在的操作及现象是
存在的操作及现象是_______ 。
(4)某合作学习小组进行以下实验探究。
①实验任务 通过测定溶液电导率,探究温度对AgCl溶解度的影响。
②查阅资料 电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。
③提出猜想 猜想a:较高温度的AgCl饱和溶液的电导率较大。
猜想b:AgCl在水中的溶解度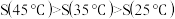
④设计实验、验证猜想 取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的AgCl饱和溶液),在设定的测试温度下,进行表1中实验1~3,记录数据。
表1
⑤数据分析、交流讨论
实验结果为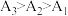 。小组同学认为,此结果可以证明③中的猜想a成立,但不足以证明猜想b成立。结合②中信息,猜想b不足以成立的理由有
。小组同学认为,此结果可以证明③中的猜想a成立,但不足以证明猜想b成立。结合②中信息,猜想b不足以成立的理由有_______ 。
⑥优化实验 小组同学为进一步验证猜想b,在实验1~3的基础上完善方案,进行实验4和5,请完成表2中内容。
表2
⑦实验总结 根据实验1~5的结果,并结合②中信息,小组同学认为猜想b也成立。猜想b成立的判断依据是_______ 。
 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。(1)实验室沿用舍勒的方法制取
 的化学方程式为
的化学方程式为(2)实验室制取干燥
 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中
 存在的操作及现象是
存在的操作及现象是(4)某合作学习小组进行以下实验探究。
①实验任务 通过测定溶液电导率,探究温度对AgCl溶解度的影响。
②查阅资料 电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。
③提出猜想 猜想a:较高温度的AgCl饱和溶液的电导率较大。
猜想b:AgCl在水中的溶解度
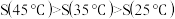
④设计实验、验证猜想 取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的AgCl饱和溶液),在设定的测试温度下,进行表1中实验1~3,记录数据。
表1
| 实验序号 | 试样 | 测试温度/℃ | 电导率/( ) ) |
| 1 | Ⅰ:25℃的AgCl饱和溶液 | 25 | A1 |
| 2 | Ⅱ:35℃的AgCl饱和溶液 | 35 | A2 |
| 3 | Ⅲ:45℃的AgCl饱和溶液 | 45 | A3 |
实验结果为
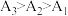 。小组同学认为,此结果可以证明③中的猜想a成立,但不足以证明猜想b成立。结合②中信息,猜想b不足以成立的理由有
。小组同学认为,此结果可以证明③中的猜想a成立,但不足以证明猜想b成立。结合②中信息,猜想b不足以成立的理由有⑥优化实验 小组同学为进一步验证猜想b,在实验1~3的基础上完善方案,进行实验4和5,请完成表2中内容。
表2
| 实验序号 | 试样 | 测试温度/℃ | 电导率/( ) ) |
| 4 | Ⅰ | B1 | |
| 5 | B2 |
您最近一年使用:0次
2022-08-17更新
|
407次组卷
|
2卷引用:第二章 海水中的重要元素——钠和氯 ★综合拔高练
名校
5 . 用零价铁( )去除含氮废水中的硝酸盐(
)去除含氮废水中的硝酸盐( )是环境修复的重要方法。一种去除
)是环境修复的重要方法。一种去除 的过程如下。
的过程如下。_______ 。
(2)Ⅱ中反应的离子方程式是_______ 。
(3)实验发现,在Ⅱ中补充一定量的 可以明显提高
可以明显提高 的去除率。向两份含氮废水[
的去除率。向两份含氮废水[
 ]中均加入足量
]中均加入足量 粉,做对比研究。
粉,做对比研究。
分析ⅱ中 的去除率提高的原因:
的去除率提高的原因:
a. 直接还原
直接还原 了。
了。
通过计算说明电子得、失数量关系:_______ ,证明该原因不合理。
b.研究发现: (导电)覆盖在铁粉表面;随着反应的进行,产生
(导电)覆盖在铁粉表面;随着反应的进行,产生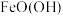 (不导电),它覆盖在
(不导电),它覆盖在 表面,形成钝化层,阻碍电子传输。
表面,形成钝化层,阻碍电子传输。
c. 能与
能与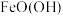 反应生成
反应生成 。
。
用 做同位素示踪实验,证明该原因合理。
做同位素示踪实验,证明该原因合理。
d. 破坏钝化层。
破坏钝化层。
将ⅱ中的 替换为
替换为_______ , 的去除率约为50%,证明该原因不合理。
的去除率约为50%,证明该原因不合理。
(4)ⅰ、ⅱ中均能发生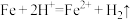 。该反应明显有助于ⅰ中
。该反应明显有助于ⅰ中 的去除,结合方程式解释原因:
的去除,结合方程式解释原因:_______ 。
(5)测定 含量
含量
步骤1.取v 含氮(
含氮( )水样,加入催化剂、
)水样,加入催化剂、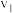



 标准溶液(过量),再加入稀
标准溶液(过量),再加入稀 。
。
步骤2.用

 标准溶液滴定剩余的
标准溶液滴定剩余的 (
( 被还原为
被还原为 ),终点时消耗
),终点时消耗
 。
。
已知:
①水样中 的含量为
的含量为_______  。
。
②溶液中 影响测定。向步骤1中加入适量
影响测定。向步骤1中加入适量 ,产生
,产生 驱赶
驱赶 ,否则会使测定结果
,否则会使测定结果_______ (填“偏大”或“偏小”)。
 )去除含氮废水中的硝酸盐(
)去除含氮废水中的硝酸盐( )是环境修复的重要方法。一种去除
)是环境修复的重要方法。一种去除 的过程如下。
的过程如下。
(2)Ⅱ中反应的离子方程式是
(3)实验发现,在Ⅱ中补充一定量的
 可以明显提高
可以明显提高 的去除率。向两份含氮废水[
的去除率。向两份含氮废水[
 ]中均加入足量
]中均加入足量 粉,做对比研究。
粉,做对比研究。| 实验序号 | ⅰ | ⅱ |
| 所加试剂 |  粉 粉 |  粉、 粉、 ( ( ) ) |
 的去除率 的去除率 | ≈50% | ≈100% |
 的去除率提高的原因:
的去除率提高的原因:a.
 直接还原
直接还原 了。
了。通过计算说明电子得、失数量关系:
b.研究发现:
 (导电)覆盖在铁粉表面;随着反应的进行,产生
(导电)覆盖在铁粉表面;随着反应的进行,产生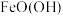 (不导电),它覆盖在
(不导电),它覆盖在 表面,形成钝化层,阻碍电子传输。
表面,形成钝化层,阻碍电子传输。c.
 能与
能与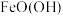 反应生成
反应生成 。
。用
 做同位素示踪实验,证明该原因合理。
做同位素示踪实验,证明该原因合理。d.
 破坏钝化层。
破坏钝化层。将ⅱ中的
 替换为
替换为 的去除率约为50%,证明该原因不合理。
的去除率约为50%,证明该原因不合理。(4)ⅰ、ⅱ中均能发生
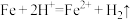 。该反应明显有助于ⅰ中
。该反应明显有助于ⅰ中 的去除,结合方程式解释原因:
的去除,结合方程式解释原因:(5)测定
 含量
含量步骤1.取v
 含氮(
含氮( )水样,加入催化剂、
)水样,加入催化剂、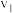



 标准溶液(过量),再加入稀
标准溶液(过量),再加入稀 。
。步骤2.用


 标准溶液滴定剩余的
标准溶液滴定剩余的 (
( 被还原为
被还原为 ),终点时消耗
),终点时消耗
 。
。已知:

①水样中
 的含量为
的含量为 。
。②溶液中
 影响测定。向步骤1中加入适量
影响测定。向步骤1中加入适量 ,产生
,产生 驱赶
驱赶 ,否则会使测定结果
,否则会使测定结果
您最近一年使用:0次
2022-05-19更新
|
1168次组卷
|
8卷引用:北京市朝阳区2022届高三 二模化学试题
北京市朝阳区2022届高三 二模化学试题北京市东城区第五中学2022届高三三模化学试题(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)北京市通州区2022届高三下学期三模考试化学试题(已下线)北京市第四中学2022-2023学年高三下学期零模化学试题(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)北京市顺义区第二中学2023-2024学年高三下学期3月月考化学试题北京市第五中学2024届高三下学期三模检测化学试题
解题方法
6 . 某小组同学利用一定浓度的HCl溶液和MnO2制备Cl2,并进行有关实验。
Ⅰ.为了防止制备的Cl2逸散,该小组同学设计装置Ⅰ、Ⅱ、Ⅲ。
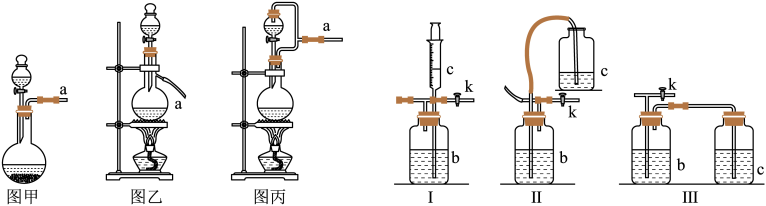
试回答:
(1)发生装置选择_______ (填“图甲”、“图乙”或“图丙”)。
(2)①若用所选的发生装置和装置Ⅰ制取氯气,b瓶加入的液体一般为_______ 。反应开始后,关闭活塞K时,发现c中液面上升不明显,可能的原因是_______ ,检查的简单方法是_______ 。
②装置Ⅰ能防止多余气体逸散的原因是_______ 。
③欲用装置Ⅱ(或装置Ⅲ)代替装置Ⅰ中的b~c部分(试剂相同),装置Ⅱ_______ (填“是”或“否”)可行,理由是_______ 。装置Ⅲ_______ (填“是”或“否”)可行,理由是_______ 。
Ⅱ.在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
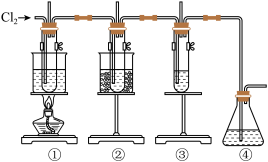
图中:①的试管里盛有15 mL 30% KOH溶液,置于水浴中;②的试管里盛有15 mL 8% NaOH溶液,置于冰水浴中;③的试管里加有紫色石蕊试液;④为尾气吸收装置。
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是①_______ ;②_______ 。
(4)反应完毕经冷却后,①的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是_______ (填写编号字母);从①的试管中分离出该晶体的方法是_______ (填写操作名称)。
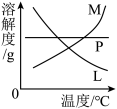
(5)根据③的试管里试液的颜色变化可否证明氯气的强氧化性_______ 。为什么?_______ 。
Ⅰ.为了防止制备的Cl2逸散,该小组同学设计装置Ⅰ、Ⅱ、Ⅲ。

试回答:
(1)发生装置选择
(2)①若用所选的发生装置和装置Ⅰ制取氯气,b瓶加入的液体一般为
②装置Ⅰ能防止多余气体逸散的原因是
③欲用装置Ⅱ(或装置Ⅲ)代替装置Ⅰ中的b~c部分(试剂相同),装置Ⅱ
Ⅱ.在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①的试管里盛有15 mL 30% KOH溶液,置于水浴中;②的试管里盛有15 mL 8% NaOH溶液,置于冰水浴中;③的试管里加有紫色石蕊试液;④为尾气吸收装置。
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
(4)反应完毕经冷却后,①的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是

(5)根据③的试管里试液的颜色变化可否证明氯气的强氧化性
您最近一年使用:0次
21-22高一·全国·课时练习
7 . 某化学小组同学发现“84”消毒液(主要成分为NaClO)与洁厕剂(主要成分为盐酸)室温下混和有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2。
(1)若用次氯酸钙、浓盐酸为原料,利用如图装置制取Cl2.装置中仪器a的名称为_______ 。
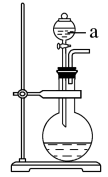
(2)甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,观察有无色气泡产生。乙同学认为不合理,理由是_______ 。
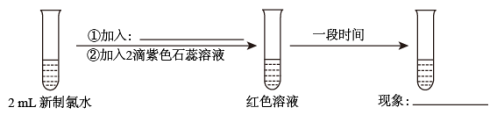
(3)某实验小组对氯水成分和性质进行研究,实验如图:
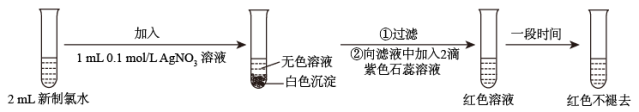
甲同学认为,“红色不褪去”不是因为氯水被稀释所致。乙同学持反对意见。为了证明甲同学错误,乙同学继续以下实验,请在横线上补充所加入的试剂和观察到的现象。
加入:_______ ,现象:_______ 。
(4)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如图装置制备无水FeCl3。
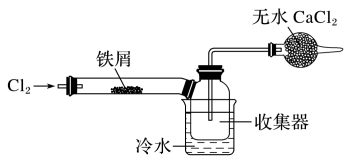
①下列操作步骤的正确排序为_______ (填字母)
a.体系冷却后,停止通入Cl2
b.通入干燥的Cl2赶尽装置中的空气
c.在铁屑下方加热至反应完成
d.用干燥的H2赶尽Cl2
e.检验装置的气密性
②该实验装置存在的明显缺陷是_______ 。
(1)若用次氯酸钙、浓盐酸为原料,利用如图装置制取Cl2.装置中仪器a的名称为

(2)甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,观察有无色气泡产生。乙同学认为不合理,理由是
(3)某实验小组对氯水成分和性质进行研究,实验如图:

甲同学认为,“红色不褪去”不是因为氯水被稀释所致。乙同学持反对意见。为了证明甲同学错误,乙同学继续以下实验,请在横线上补充所加入的试剂和观察到的现象。
加入:

(4)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如图装置制备无水FeCl3。

①下列操作步骤的正确排序为
a.体系冷却后,停止通入Cl2
b.通入干燥的Cl2赶尽装置中的空气
c.在铁屑下方加热至反应完成
d.用干燥的H2赶尽Cl2
e.检验装置的气密性
②该实验装置存在的明显缺陷是
您最近一年使用:0次
8 . 某化学兴趣小组为探究高锰酸钾与铜的反应,设计实验如下:
资料:a. 在酸性溶液中不能稳定存在:
在酸性溶液中不能稳定存在: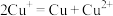
b. 为粉红色沉淀、溶于强酸;
为粉红色沉淀、溶于强酸; 为黑色沉淀、不溶于强酸
为黑色沉淀、不溶于强酸
(1) 被氧化成
被氧化成___________ ,依据是___________ 。
(2)为探究 的还原产物,取A区中溶液
的还原产物,取A区中溶液___________ (填操作和现象),证明有 生成。
生成。
(3)A区中 与
与 反应的离子方程式是
反应的离子方程式是___________ 。
(4)经检验,B区的棕黑色固体是 ,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:
,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:___________ 。
(5)小组同学又进行了以下定量实验:
通过计算,分析溶液紫色变浅而未完全褪色的原因:___________ 。
| 实验一 | 现象 |
  酸性溶液 酸性溶液 | 一段时间后,培养皿中由铜片向外侧依次呈现: A区澄清且几乎无色; B区底部覆盖棕黑色固体; C区澄清且紫色变浅 |
 在酸性溶液中不能稳定存在:
在酸性溶液中不能稳定存在: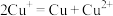
b.
 为粉红色沉淀、溶于强酸;
为粉红色沉淀、溶于强酸; 为黑色沉淀、不溶于强酸
为黑色沉淀、不溶于强酸(1)
 被氧化成
被氧化成(2)为探究
 的还原产物,取A区中溶液
的还原产物,取A区中溶液 生成。
生成。(3)A区中
 与
与 反应的离子方程式是
反应的离子方程式是(4)经检验,B区的棕黑色固体是
 ,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:
,从溶液中离子扩散的角度,结合离子方程式解释B区和C区中的现象:(5)小组同学又进行了以下定量实验:
| 实验一 | 现象 |
 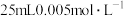  酸性溶液 酸性溶液 | 一段时间后,铜片质量减少了0.02g,溶液中无固体析出、溶液紫色变浅 |
您最近一年使用:0次
名校
解题方法
9 . 如图所示,根据实验室制取氯气的原理制备氯气并进行性质验证,回答下列问题:
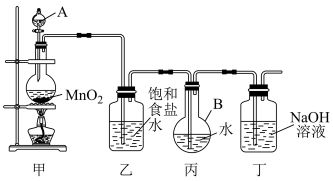
(1)写出装置甲中发生反应的化学方程式:___________ 。装置甲中的仪器使用前需要检漏的是___________ (写名称)。
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是___________ 。
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是___________ 。
(3)饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一、某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
ⅰ.在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量无色气泡产生,溶液的黄绿色褪去;
ⅱ.过滤,将滤液滴在有色布条上,发现其漂白性比饱和氯水更强;
ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与澄清石灰水混合,立即产生白色沉淀。
第二份与稀盐酸混合,立刻产生大量无色气体。
第三份加热,看到溶液变浑浊且有无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
①试根据所学知识推测,在ⅱ的滤液中除了溶解的极少量氯气外,还含有的其他溶质为___________ (写化学式)。
②写出步骤ⅲ中第一份滤液发生反应的离子方程式:___________ 。

(1)写出装置甲中发生反应的化学方程式:
(2)利用装置丙制取饱和氯水并测其pH。
①证明氯水已饱和的现象是
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是
(3)饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一、某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
ⅰ.在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量无色气泡产生,溶液的黄绿色褪去;
ⅱ.过滤,将滤液滴在有色布条上,发现其漂白性比饱和氯水更强;
ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与澄清石灰水混合,立即产生白色沉淀。
第二份与稀盐酸混合,立刻产生大量无色气体。
第三份加热,看到溶液变浑浊且有无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
①试根据所学知识推测,在ⅱ的滤液中除了溶解的极少量氯气外,还含有的其他溶质为
②写出步骤ⅲ中第一份滤液发生反应的离子方程式:
您最近一年使用:0次
2021-11-13更新
|
193次组卷
|
4卷引用:练习7 氧化还原反应-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)
(已下线)练习7 氧化还原反应-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)河南省商丘名校2021-2022学年高一上学期期中联考化学试题河南省虞城县高级中学2021-2022学年高一上学期中考试化学试题山东省济宁市任城区2020-2021学年高一上学期期中考试化学试题
解题方法
10 . 化合物X由三种短周期元素组成,可用作氧化剂和气体干燥剂。某兴趣小组对化合物X开展探究实验。

其中:混合气体B中含有两种单质气体,其中一种呈黄绿色。
(1)组成X的三种元素为___ 。
(2)写出X隔绝空气加热分解的化学方程式___ 。
(3)将溶液C蒸发结晶可得晶体的化学式为___ ,直接加热并灼烧该晶体得不到该晶体的无水盐,请说明理由___ 。
(4)将黄绿色气体B缓慢通入含有酚酞的NaOH稀溶液中,当通到一定量时,红色突然褪去。产生上述现象可能的原因有两种①___ ,②___ ;请设计相关实验证明红色褪去的原因___ 。

其中:混合气体B中含有两种单质气体,其中一种呈黄绿色。
(1)组成X的三种元素为
(2)写出X隔绝空气加热分解的化学方程式
(3)将溶液C蒸发结晶可得晶体的化学式为
(4)将黄绿色气体B缓慢通入含有酚酞的NaOH稀溶液中,当通到一定量时,红色突然褪去。产生上述现象可能的原因有两种①
您最近一年使用:0次



