名校
解题方法
1 . 一种利用磁铁矿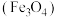 制备铁红的流程如下:
制备铁红的流程如下:
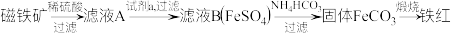
下列说法正确的是
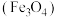 制备铁红的流程如下:
制备铁红的流程如下: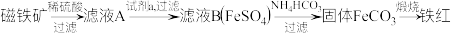
下列说法正确的是
| A.往滤液A中滴加少量酸性KMnO4溶液,可观察到紫红色褪去 |
B.可以用KSCN溶液和氯水检验滤液A中是否有 |
C.FeCO3在空气中煅烧的反应方程式为 |
| D.最终得到铁红中的Fe元素的质量小于原磁铁矿中的Fe元素的质量 |
您最近一年使用:0次
名校
2 . 下列各组离子在给定条件下能大量共存的是
A.含有大量ClO‒的溶液:K+、H+、Cl‒、SO |
B.澄清透明的溶液中:Cu2+、Na+、SO 、NO 、NO |
C.遇铝能产生H2的溶液:NH 、K+、Cl‒、CO 、K+、Cl‒、CO |
D.使紫色石蕊溶液呈红色的溶液:Mg2+、Fe2+、SO 、NO 、NO |
您最近一年使用:0次
2024-05-27更新
|
244次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
3 . “协同去污,变废为宝”为处理工业废水提供了新思路。现有含 、
、 的电镀废液以及含
的电镀废液以及含 的废液。现联合处理废水,回收
的废液。现联合处理废水,回收 并生产铁红和媒染剂
并生产铁红和媒染剂 ,回收过程如下,请回答以下问题:
,回收过程如下,请回答以下问题:________ 。
(2)对于该工艺的说法错误的是________。
(3)写出铁铜废液中加入试剂1发生的离子方程式________ 。滤液与含酸性 的废液反应的离子方程式为
的废液反应的离子方程式为________ 。
(4)证明滤液已被试剂3完全氧化的实验方法是________ 。
(5)从 溶液制取
溶液制取 晶体的实验操作方法为蒸发浓缩、
晶体的实验操作方法为蒸发浓缩、________ 、过滤、________ 、干燥。
(6)已知 化学性质与
化学性质与 类似,若将流程中
类似,若将流程中 的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为________ 。
 、
、 的电镀废液以及含
的电镀废液以及含 的废液。现联合处理废水,回收
的废液。现联合处理废水,回收 并生产铁红和媒染剂
并生产铁红和媒染剂 ,回收过程如下,请回答以下问题:
,回收过程如下,请回答以下问题: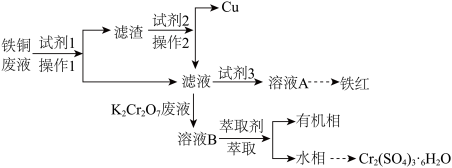
(2)对于该工艺的说法错误的是________。
| A.操作1和操作2都是过滤 |
B.试剂1是过量的 粉,试剂2是过量的 粉,试剂2是过量的 |
| C.可从有机相中提取出某成分加入到溶液A中,提高产量,剩余成分可循环利用 |
D.试剂3只能是 ,目的是将 ,目的是将 氧化成 氧化成 |
(3)写出铁铜废液中加入试剂1发生的离子方程式
 的废液反应的离子方程式为
的废液反应的离子方程式为(4)证明滤液已被试剂3完全氧化的实验方法是
(5)从
 溶液制取
溶液制取 晶体的实验操作方法为蒸发浓缩、
晶体的实验操作方法为蒸发浓缩、(6)已知
 化学性质与
化学性质与 类似,若将流程中
类似,若将流程中 的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
的溶液转化为氢氧化铬,则转化过程中发生的离子方程式为
您最近一年使用:0次
名校
4 . 下列有关离子(或物质)的检验、现象及结论,都正确的是
| A.向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色,该溶液中一定含有Fe2+ |
| B.向某溶液中滴加KSCN溶液,溶液变成红色,该溶液中一定不存在Fe2+ |
| C.将某种铁的氧化物溶于足量的稀硫酸中,取其溶液滴加酸性KMnO4溶液,振荡,溶液褪色,原氧化物中含有+2价铁 |
| D.向久置的FeCl2溶液中滴入用硫酸酸化的H2O2溶液,溶液变黄,滴加KSCN溶液,溶液变成红色,说明发生氧化还原反应,且氧化性:H2O2<Fe3+ |
您最近一年使用:0次
5 . 黄铁矿(主要成分 ,含杂质
,含杂质 )是工业制硫酸的重要原料,还可用来制备绿矾晶体(
)是工业制硫酸的重要原料,还可用来制备绿矾晶体( ),工艺流程如下:
),工艺流程如下:______ 。
(2)试剂A为______ (写化学式),操作Ⅰ所用玻璃仪器为烧杯、______ 。
(3)结合下图,若想得到 ,“操作2”过程为蒸发浓缩,
,“操作2”过程为蒸发浓缩,______ ,过滤,……;母液放置在空气中一段时间,应返回“______ ”工序循环使用
ⅰ.快速称取样品 ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
ⅱ.向ⅰ所得溶液中滴加足量 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。
根据实验数据,样品中
______ (用含a,b的代数式表示),若样品溶于水后在空气中放置时间过长,测定结果将______ (填“偏大”、“偏小”或“无影响”)。
 ,含杂质
,含杂质 )是工业制硫酸的重要原料,还可用来制备绿矾晶体(
)是工业制硫酸的重要原料,还可用来制备绿矾晶体( ),工艺流程如下:
),工艺流程如下: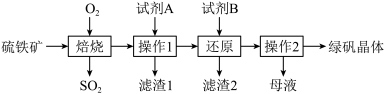
(2)试剂A为
(3)结合下图,若想得到
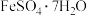 ,“操作2”过程为蒸发浓缩,
,“操作2”过程为蒸发浓缩,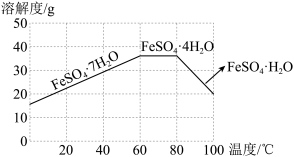
ⅰ.快速称取样品
 ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
ag,用适量蒸馏水溶解,再滴加几滴盐酸酸化。ⅱ.向ⅰ所得溶液中滴加足量
 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为b g。根据实验数据,样品中

您最近一年使用:0次
6 . 实验室通过下列过程制取草酸亚铁晶体。
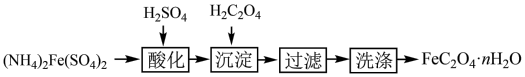
A.“酸化”后的溶液,根据电荷守恒存在等量关系:n( )+2×n(Fe2+)=2×n( )+2×n(Fe2+)=2×n( ) ) |
B.“沉淀”时发生反应的离子方程式:Fe2++ +nH2O=FeC2O4·nH2O↓ +nH2O=FeC2O4·nH2O↓ |
| C.可以用酸性KMnO4溶液检验“沉淀”后的上层清液中是否含有Fe2+ |
| D.“洗涤”时先水洗,再用乙醇洗涤,有利于晶体快速干燥和防止失去结晶水 |
您最近一年使用:0次
解题方法
7 . 部分含铁物质的分类与相应化合价关系如图所示,下列推断错误的是
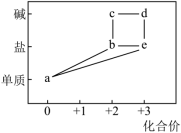
| A.a与硫粉充分加热反应可生成b |
| B.制备c时,应将胶头滴管伸入液面以下 |
| C.c、d在空气中充分加热,均可得到氧化铁 |
| D.b和e的混合溶液中,可先滴加KSCN溶液,再滴加少量新制氯水,证明溶液中含Fe2+ |
您最近一年使用:0次
名校
解题方法
8 . 某研究性学习小组进行某补血剂中铁元素( 价)含量测定的实验,其流程如下:
价)含量测定的实验,其流程如下:不 正确的是
 价)含量测定的实验,其流程如下:
价)含量测定的实验,其流程如下: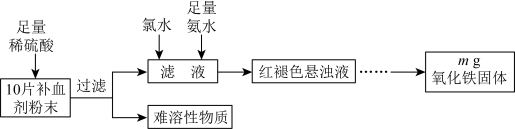
A.向过滤后的滤液中滴加 溶液,溶液可能呈红色 溶液,溶液可能呈红色 |
B.可以用 替代上述流程中的氯水 替代上述流程中的氯水 |
| C.红褐色悬浊液经过滤、洗涤、干燥,得到氧化铁固体 |
D.每片补血剂中铁元素的质量为 |
您最近一年使用:0次
2024-05-06更新
|
280次组卷
|
3卷引用:江苏省苏州市2023-2024学年高一下学期期中统考化学试题
名校
9 . 通过如下实验,比较 、
、 、
、 的氧化性。
的氧化性。
(1)实验室 溶液通常盛放在
溶液通常盛放在___________ 试剂瓶中。
(2)Ⅱ中反应的离子方程式为___________ 。
(3)I、Ⅱ中的现象说明___________。
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
(5)写出检验I中是否含有 的方法。
的方法。___________ 。
(6)检验Ⅱ中是否含有 不可选用:___________。(不定项)
不可选用:___________。(不定项)
(7)推测Ⅲ中未发生 氧化
氧化 的原因
的原因___________ 。
 、
、 、
、 的氧化性。
的氧化性。
| 实验现象 |
I中产生黑色沉淀,滴加 溶液,变红 溶液,变红 | |
| Ⅱ中溶液呈棕黄色,滴加淀粉溶液,变蓝 | |
| Ⅲ中产生黄色沉淀,滴加淀粉溶液,未变蓝 |
(1)实验室
 溶液通常盛放在
溶液通常盛放在(2)Ⅱ中反应的离子方程式为
(3)I、Ⅱ中的现象说明___________。
A.氧化性顺序: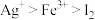 | B.氧化性顺序: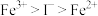 |
C.还原性顺序: | D.还原性顺序: |
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
| A.酒精 | B.二硫化碳 | C.浓硝酸 | D.热盐酸 |
(5)写出检验I中是否含有
 的方法。
的方法。(6)检验Ⅱ中是否含有
 不可选用:___________。(不定项)
不可选用:___________。(不定项)| A.氢氧化钠溶液 | B.酸性高辒酸钾溶液 | C.硫氰化钾溶液 | D.稀氨水 |
(7)推测Ⅲ中未发生
 氧化
氧化 的原因
的原因
您最近一年使用:0次
10 . 电子工业常用 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有___________ 。
(2) 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为___________ 。
(3)试剂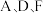 的化学式分别是
的化学式分别是___________ 、___________ 、___________ 。用 溶液制取
溶液制取 晶体的方法是
晶体的方法是___________ 。
A.蒸发结晶 B.降温结晶
 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: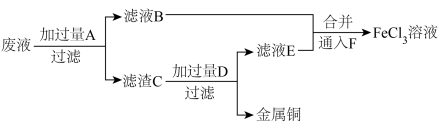
 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有(2)
 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为(3)试剂
 的化学式分别是
的化学式分别是 溶液制取
溶液制取 晶体的方法是
晶体的方法是A.蒸发结晶 B.降温结晶
您最近一年使用:0次