1 . a.有下列物质:①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖
请回答下列问题:
(1)属于电解质的有___________ (填序号)
(2)属于非电解质的有___________ (填序号)
b.某同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为___________ 。FeCl3溶液,加入1滴___________ 溶液,溶液变___________ 。
(4)FeCl2溶液与氯水反应的化学方程式为___________ 。
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程___________ 。
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量___________ mol。含有O数目___________ 。
(7)100 mL 0.2 mol/L Na2SO4溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(8)标准状况下11.2 L的CO2的物质的量是___________ mol。
请回答下列问题:
(1)属于电解质的有
(2)属于非电解质的有
b.某同学用如下实验探究
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(4)FeCl2溶液与氯水反应的化学方程式为
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量
(7)100 mL 0.2 mol/L Na2SO4溶液中
 的物质的量浓度为
的物质的量浓度为(8)标准状况下11.2 L的CO2的物质的量是
您最近一年使用:0次
解题方法
2 . 下列离子的检验方法中合理的是
A.向某溶液中滴入H2O2溶液产生气泡,说明不含 |
B.用酸性KMnO4溶液检验FeSO4溶液中是否含有 |
C.向某溶液中加入NaOH溶液,直接得到红褐色沉淀,说明溶液中含有 |
D.向某溶液中加入NaOH溶液得到白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有 ,不含有 ,不含有 |
您最近一年使用:0次
名校
3 . 某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为___________ 。(写出一条即可)

(2)乙组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:
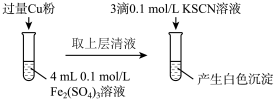
①Fe3+与Cu反应的离子方程式为___________ 。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
iii.2Cu2++4I-=2CuI↓+I2。
实验方案:
Cu2+与SCN-反应的离子方程式为 ___________ 。
(3)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称猜测该糖浆中含有Fe2+,设计方案进行验证。
①方案ⅰ预期现象与实际现象相同,并不能证明补贴口服液中一定含有Fe2+,猜想理由是:___________ 。
②方案ⅱ中实验现象是___________ ,证明补铁口服液中含有Fe2+。
(1)甲组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为

(2)乙组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:

①Fe3+与Cu反应的离子方程式为
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
iii.2Cu2++4I-=2CuI↓+I2。
实验方案:
| 实验方案 | 现象 |
| 步骤1:取4mL0.2mol/L的FeSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液 | 无明显现象 |
| 步骤2:取4mL 0.1 mol/L的CuSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液 | 产生白色沉淀 |
(3)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称猜测该糖浆中含有Fe2+,设计方案进行验证。
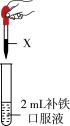 | 方案 | 试剂X |
| 方案ⅰ | 1mL 1mol/L酸性KMnO4溶液 | |
| 方案ⅱ | 依次加入5滴KSCN溶液、1mL新制氯水 |
②方案ⅱ中实验现象是
您最近一年使用:0次
名校
解题方法
4 . 进行化学实验时应强化安全意识,下列做法正确的是
| A.金属钠着火时使用泡沫灭火器灭火 |
| B.浓硫酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
| C.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 |
| D.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 |
您最近一年使用:0次
2024-01-25更新
|
92次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高一上学期1月期末化学试题
名校
5 . 电子工业中,人们常用FeCl3溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
(1)请用化学方程式表示制造印刷电路板的反应原理_________________ 。
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:
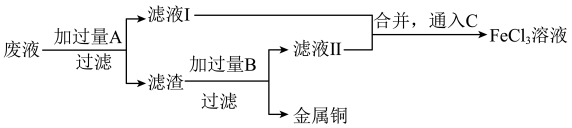
(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A________ ,B________ ,C________ 。
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是_________________ 。为检验该金属阳离子,可设计的实验操作及实验现象为_________________ (可选择的试剂为“锌片”、KSCN溶液、“酸性H2O2”、“酸性KMnO4溶液”或“NaOH溶液”),且该过程发生的氧化还原反应离子方程式为_______________ 。
(4)上述步骤中,通入C发生反应的离子方程式为___________________ 。
(1)请用化学方程式表示制造印刷电路板的反应原理
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:

(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是
(4)上述步骤中,通入C发生反应的离子方程式为
您最近一年使用:0次
2024-01-09更新
|
67次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
6 . 《新修本草》是我国古代中药著作,记载药物844种,其中“青矾”条目下写到:“本来绿色,新出窟未见风者,正如玻璃∙∙∙∙∙∙∙烧之赤色∙∙∙∙∙∙”,据此推测“青矾”的主要成分为
A. | B. | C. | D. |
您最近一年使用:0次
2023-12-29更新
|
56次组卷
|
13卷引用:新疆和田地区皮山县高级中学2021-2022学年高二下学期期末考试化学试题
新疆和田地区皮山县高级中学2021-2022学年高二下学期期末考试化学试题新疆维吾尔自治区皮山县高级中学2023-2024学年高一上学期1月期末化学试题河北省武邑中学2018届高三上学期第二次调研化学试题【全国市级联考】河北省邯郸市2017-2018学年高二下学期期末考试化学试题安徽省宿州市2018届高三上学期第一次教学质量检测理综化学试题山西省运城市2021届高三上学期9月调研考试化学试题北京市新学道临川学校2021届高三上学期第一次月考化学试题天津市咸水沽第一中学2022-2023学年高三上学期学开学考试化学试题陕西省铜川市耀州中学2022-2023学年高一上学期期末考试化学试题天津市五校2023届高三一模联考化学试题广东省韶关市武江区北江实验中学2022-2023学年高三上学期第一次月考化学试题山东省青岛市格兰德学校2023-2024学年高一上学期12月月考化学试题河北省唐山市第十二高级中学2023-2024学年高一上学期12月月考化学试题
名校
7 . 为了检验某长期放置的FeCl2溶液是否完全变质,可选用的试剂是
| A.氨水 | B.酸性高锰酸钾溶液 | C.KSCN | D.淀粉 |
您最近一年使用:0次
2023-12-03更新
|
246次组卷
|
2卷引用:新疆喀什地区十四校2023-2024学年高一上学期期末质量检测化学试卷
解题方法
8 . 铁元素是人体内一种微量元素,主要以Fe2+的形式存在。请回答下列问题:
(1)下列微粒中,既有氧化性又有还原性的是______ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中______ 是还原剂
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸反应的离子方程式是___________ 。
(4)含硫酸亚铁的药片可治疗缺铁性贫血,其表面有糖衣,糖衣的作用是___________ 。可用___________ 溶液检验该硫酸亚铁药片是否变质。
(1)下列微粒中,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸反应的离子方程式是
(4)含硫酸亚铁的药片可治疗缺铁性贫血,其表面有糖衣,糖衣的作用是
您最近一年使用:0次
解题方法
9 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价—类”二维图。铁元素的“价—类”二维图如图所示,下列说法正确的是

| A.工业上用CO还原Fe2O3炼铁,该反应为置换反应 |
| B.Fe3O4中铁元素为+4价 |
| C.要除去FeCl2溶液中少量的FeCl3,可加入适量铁粉并过滤 |
| D.Fe(OH)2浊液露置于空气中,由白色立即变为红褐色 |
您最近一年使用:0次
名校
解题方法
10 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)从 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
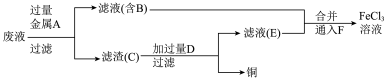
滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答:
(2)实验I中反应的化学方程式是___________ 。
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(4)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:(1)从
 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
滤渣C中所含物质的化学式为
II.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验I | 实验II |
 | 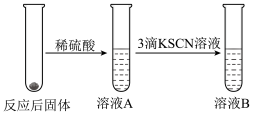 |
(2)实验I中反应的化学方程式是
(3)甲同学观察到实验I中持续产生肥皂泡,但实验II中溶液B未呈现红色,则溶液B未呈现红色的原因是
(4)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次



