名校
1 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用淀粉 溶液和醋酸检验加碘盐中的 溶液和醋酸检验加碘盐中的 : : |
B. 溶液中通入少量 溶液中通入少量 : :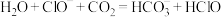 |
C.氯化亚铁溶液中加入酸性的 溶液: 溶液: |
D. 固体与氢碘酸反应: 固体与氢碘酸反应: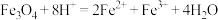 |
您最近一年使用:0次
2 . 室温下,探究0.1mol/LFeSO4溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | Fe2+能否催化H2O2分解 | 向2mL5%H2O2溶液中滴加几滴FeSO4溶液,观察气泡产生情况 |
| B | 溶液中是否含有Fe2+ | 向2mLFeSO4溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液颜色变化 |
| C | Fe2+是否水解 | 向2mLFeSO4溶液中滴加2~3滴酚酞试液,观察溶液颜色变化 |
| D | Fe2+是否有还原性 | 向2mLFeSO4溶液中滴加几滴酸性KMnO4溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 硫酸锰是一种重要的化工中间体,是锰行业研究的热点。工业以软锰矿(主要成分是 ,含有
,含有 、
、 等少量杂质)为主要原料制备
等少量杂质)为主要原料制备 。其工业流程如图:
。其工业流程如图:

(1)为了提高浸锰的浸取率可采取的措施是_______ (任写一条),滤渣Ⅱ为_______ 。
(2)浸锰过程中 与
与 反应的离子方程式为
反应的离子方程式为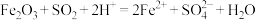 ,该反应是经历以下两步反应实现的:
,该反应是经历以下两步反应实现的:
Ⅰ.
Ⅱ.……
写出Ⅱ的离子方程式:_______ 。
(3)过滤1所得滤液中主要存在的金属阳离子为_______ (填离子符号)。
(4)氧化过程中被 氧化的主要微粒为
氧化的主要微粒为_______ 。
(5)加入 溶液后,生成
溶液后,生成 沉淀,同时还有气体生成,写出反应的离子方程式:
沉淀,同时还有气体生成,写出反应的离子方程式:_______ 。
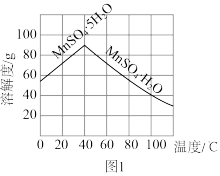
(6)已知 的溶解度曲线如图1所示,从酸溶后析出
的溶解度曲线如图1所示,从酸溶后析出 晶体的“系列操作”是
晶体的“系列操作”是_______ 、洗涤、低温干燥。
(7)通过锻烧 可制得软磁铁氧体材料
可制得软磁铁氧体材料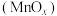 ,在不同温度下锻烧
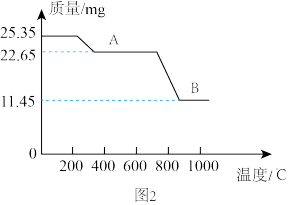
,在不同温度下锻烧 时剩余质量变化的曲线如图2所示,根据图2中数据可得
时剩余质量变化的曲线如图2所示,根据图2中数据可得 中
中 的值为
的值为_______ 。
 ,含有
,含有 、
、 等少量杂质)为主要原料制备
等少量杂质)为主要原料制备 。其工业流程如图:
。其工业流程如图:
(1)为了提高浸锰的浸取率可采取的措施是
(2)浸锰过程中
 与
与 反应的离子方程式为
反应的离子方程式为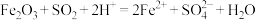 ,该反应是经历以下两步反应实现的:
,该反应是经历以下两步反应实现的:Ⅰ.

Ⅱ.……
写出Ⅱ的离子方程式:
(3)过滤1所得滤液中主要存在的金属阳离子为
(4)氧化过程中被
 氧化的主要微粒为
氧化的主要微粒为(5)加入
 溶液后,生成
溶液后,生成 沉淀,同时还有气体生成,写出反应的离子方程式:
沉淀,同时还有气体生成,写出反应的离子方程式:(6)已知
 的溶解度曲线如图1所示,从酸溶后析出
的溶解度曲线如图1所示,从酸溶后析出 晶体的“系列操作”是
晶体的“系列操作”是
(7)通过锻烧
 可制得软磁铁氧体材料
可制得软磁铁氧体材料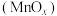 ,在不同温度下锻烧
,在不同温度下锻烧 时剩余质量变化的曲线如图2所示,根据图2中数据可得
时剩余质量变化的曲线如图2所示,根据图2中数据可得 中
中 的值为
的值为
您最近一年使用:0次
名校
解题方法
4 . 下列各组离子在指定溶液中能大量共存的是
①无色溶液中:K+、Na+、Cu2+、OH-
②pH=11的溶液中: 、Na+、[Al(OH)4]-、
、Na+、[Al(OH)4]-、
③加入Al能放出H2的溶液中:Cl-、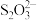 、
、 、
、
④由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、 、SCN-、
、SCN-、
⑥酸性溶液中:Fe2+、Al3+、NO 、I-、Cl-
、I-、Cl-
①无色溶液中:K+、Na+、Cu2+、OH-
②pH=11的溶液中:
 、Na+、[Al(OH)4]-、
、Na+、[Al(OH)4]-、
③加入Al能放出H2的溶液中:Cl-、
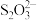 、
、 、
、
④由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、
 、SCN-、
、SCN-、
⑥酸性溶液中:Fe2+、Al3+、NO
 、I-、Cl-
、I-、Cl-| A.①② | B.③⑥ | C.②④ | D.③⑤ |
您最近一年使用:0次
2023-08-26更新
|
1315次组卷
|
3卷引用:新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题
名校
解题方法
5 . 向仅含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法错误的是
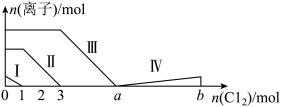

| A.线段Ⅰ、Ⅱ、Ⅲ、Ⅳ分别代表I-、Fe2+、Br-、HIO3的变化情况 |
| B.Fe2+、I-和Br-的物质的量之比为1∶2∶3 |
| C.根据图像可计算b=11 |
| D.线段Ⅳ对应的反应中氧化剂和还原剂的物质的量之比是5∶1 |
您最近一年使用:0次
2023-08-14更新
|
495次组卷
|
3卷引用:河北省迁安市第一中学2022-2023学年高三上学期期中考试化学试题
名校
6 . 下列表示反应的离子方程式正确的是
A.向 溶液中通入过量的氯气: 溶液中通入过量的氯气: |
B. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
C.将 溶液滴入明矾 溶液滴入明矾 溶液中至沉淀质量最大: 溶液中至沉淀质量最大: |
D.用醋酸和淀粉-KI溶液检验加碘盐中的 : : |
您最近一年使用:0次
2023-07-19更新
|
1856次组卷
|
4卷引用:湖南师范大学附属中学2024届高三摸底考试化学试题
2023高三·全国·专题练习
解题方法
7 . 书写下列离子方程式,体会Fe2+与Fe3+的转化条件。
(1)将H2S气体通入FeCl3溶液中产生淡黄色沉淀:_______ 。
(2)将FeCl3溶液滴入KI-淀粉溶液,溶液变蓝:_______ 。
(3)向酸性FeSO4溶液中滴入H2O2:_______ 。
(4)FeSO4使酸性高锰酸钾溶液褪色:_______ 。
(5)将FeCl2溶液滴入HNO3溶液中,有无色气体放出:_______ 。
(1)将H2S气体通入FeCl3溶液中产生淡黄色沉淀:
(2)将FeCl3溶液滴入KI-淀粉溶液,溶液变蓝:
(3)向酸性FeSO4溶液中滴入H2O2:
(4)FeSO4使酸性高锰酸钾溶液褪色:
(5)将FeCl2溶液滴入HNO3溶液中,有无色气体放出:
您最近一年使用:0次
解题方法
8 . 下列离子方程式正确的是
A.用醋酸除去水垢: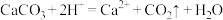 |
B.向 溶液中加过量的 溶液中加过量的 溶液: 溶液: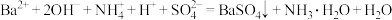 |
C.向饱和 溶液中通入过量 溶液中通入过量 : :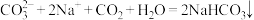 |
D.1mol  通入含1mol 通入含1mol  的溶液中: 的溶液中: |
您最近一年使用:0次
解题方法
9 . 某小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
【实验1】试剂:酸化的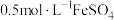 溶液(
溶液( ),
),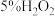 溶液(
溶液( )
)
(1)上述实验中 溶液与
溶液与 溶液反应的离子方程式是
溶液反应的离子方程式是_______ 。
(2)产生气泡的原因是_______ 。
【实验Ⅱ】试剂:未酸化的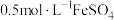 溶液(
溶液( ),
), 溶液(
溶液( )
)
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加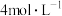 盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有
盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有 ,经检验还含有
,经检验还含有 。检验棕黄色沉淀中
。检验棕黄色沉淀中 的方法是
的方法是_______ 。
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ. 溶液氧化
溶液氧化 消耗
消耗
ⅱ. 氧化的产物发生了水解
氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是_______ 。
②实验验证假设ⅱ:取_______ ,加热,溶液变为红褐色, 下降,证明假设ⅱ成立。
下降,证明假设ⅱ成立。
(5)将 溶液加入
溶液加入 溶液后,产生红褐色胶体,反应的离子方程式是:
溶液后,产生红褐色胶体,反应的离子方程式是:_______ 。
 溶液的反应。
溶液的反应。【实验1】试剂:酸化的
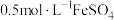 溶液(
溶液( ),
),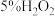 溶液(
溶液( )
)| 操作 | 现象 |
取 上述 上述 溶液于试管中,加入5滴 溶液于试管中,加入5滴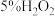 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与
溶液与 溶液反应的离子方程式是
溶液反应的离子方程式是(2)产生气泡的原因是
【实验Ⅱ】试剂:未酸化的
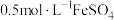 溶液(
溶液( ),
), 溶液(
溶液( )
)| 操作 | 现象 |
取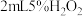 溶液于试管中,加入5滴上述 溶液于试管中,加入5滴上述 溶液 溶液 | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液 |
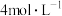 盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有
盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有 ,经检验还含有
,经检验还含有 。检验棕黄色沉淀中
。检验棕黄色沉淀中 的方法是
的方法是(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.
 溶液氧化
溶液氧化 消耗
消耗
ⅱ.
 氧化的产物发生了水解
氧化的产物发生了水解①根据实验Ⅱ记录否定假设ⅰ,理由是
②实验验证假设ⅱ:取
 下降,证明假设ⅱ成立。
下降,证明假设ⅱ成立。(5)将
 溶液加入
溶液加入 溶液后,产生红褐色胶体,反应的离子方程式是:
溶液后,产生红褐色胶体,反应的离子方程式是:
您最近一年使用:0次
2023-07-05更新
|
350次组卷
|
3卷引用:吉林省通化市辉南县第六中学2024届高三上学期第二次半月考化学试题
10 . 下列关于Na2O和Na2O2的叙述正确的是
| A.将Na2O与Na2O2分别加入滴有酚酞的水中,二者现象相同 |
| B.在Na2O2与水的反应中,氧化产物与还原产物物质的量之比为1:4 |
| C.将Na2O2分别加入FeCl3和FeCl2溶液中最终所得沉淀颜色相同 |
| D.等质量的Na2O与Na2O2投入等量且足量水中充分反应后所得溶液物质的量浓度相等 |
您最近一年使用:0次
2023-06-20更新
|
425次组卷
|
3卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题



