1 . 在溶液中能大量共存的离子组是
A.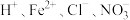 | B.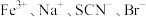 |
C.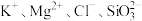 | D. |
您最近一年使用:0次
名校
解题方法
2 . 一种利用磁铁矿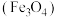 制备铁红的流程如下:
制备铁红的流程如下:
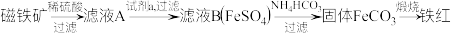
下列说法正确的是
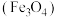 制备铁红的流程如下:
制备铁红的流程如下:
下列说法正确的是
| A.往滤液A中滴加少量酸性KMnO4溶液,可观察到紫红色褪去 |
B.可以用KSCN溶液和氯水检验滤液A中是否有 |
C.FeCO3在空气中煅烧的反应方程式为 |
| D.最终得到铁红中的Fe元素的质量小于原磁铁矿中的Fe元素的质量 |
您最近一年使用:0次
名校
3 . 某实验小组为了探究过量铁粉与硝酸酸化的 溶液反应过程中溶液显黄色的原因,设计实验如下:
溶液反应过程中溶液显黄色的原因,设计实验如下:
已知: 与
与 反应生成白色沉淀
反应生成白色沉淀 ,下列说法错误的是
,下列说法错误的是
 溶液反应过程中溶液显黄色的原因,设计实验如下:
溶液反应过程中溶液显黄色的原因,设计实验如下:实验编号 | 实验操作 | 实验现象 |
1 | 向硝酸酸化的 溶液 溶液 中加入过量铁粉,搅拌后静置 中加入过量铁粉,搅拌后静置 | 烧杯底部有黑色固体,约 后溶液明显变黄 后溶液明显变黄 |
2 | 在实验1中反应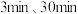 、和 、和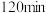 时,分别取上层清液滴加等量 时,分别取上层清液滴加等量 溶液 溶液 |  时产生白色沉淀,溶液呈红色: 时产生白色沉淀,溶液呈红色: 时白色沉淀减少,溶液颜色加深; 时白色沉淀减少,溶液颜色加深;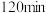 时白色沉淀更少,溶液颜色较 时白色沉淀更少,溶液颜色较 更浅 更浅 |
3 | 向硝酸酸化的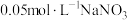 溶液 溶液 中加入过量铁粉,搅拌后静置,分别取反应 中加入过量铁粉,搅拌后静置,分别取反应 和 和 时的上层清液滴加等量 时的上层清液滴加等量 溶液 溶液 |  时溶液呈浅红色; 时溶液呈浅红色; 时溶液颜色较 时溶液颜色较 时更浅 时更浅 |
 与
与 反应生成白色沉淀
反应生成白色沉淀 ,下列说法错误的是
,下列说法错误的是A.由上述实验可知溶液变黄的主要原因是酸性环境下 的氧化性引起 的氧化性引起 |
B.由实验1和实验2可知,黄色溶液中含有 |
C.由实验2的现象推断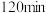 时溶液颜色变浅是因为发生了反应 时溶液颜色变浅是因为发生了反应 |
D.要验证实验1中黑色固体是否含有 ,可向黑色固体中加稀盐酸 ,可向黑色固体中加稀盐酸 |
您最近一年使用:0次
4 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是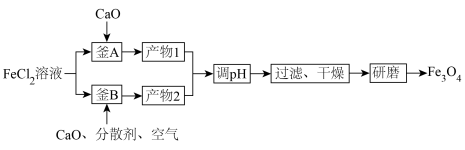
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为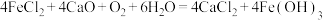 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近一年使用:0次
5 . 碘及其化合物广泛用于医药、染料等。一种从海水中获取单质碘的部分工艺流程如下,下列有关说法错误的是
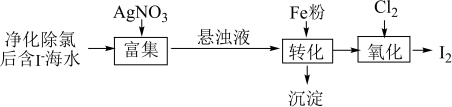
| A.过滤操作用到的玻璃仪器有漏斗、烧杯、玻璃棒 |
| B.将“沉淀”与稀硝酸反应,生成的物质可循环使用 |
C.通入氯气的过程中,先生成的氧化产物为 |
D.将“氧化”后的溶液直接蒸馏可得 |
您最近一年使用:0次
6 . 下列关于Fe及其化合物反应的离子方程式书写正确的是
A.实验室配制的亚铁盐溶液在空气中被氧化: |
B. 固体溶于HI溶液: 固体溶于HI溶液: 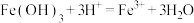 |
C.用FeCl3饱和溶液制备 胶体: 胶体:  |
D.过量铁粉与稀硝酸反应: |
您最近一年使用:0次
名校
7 . 下列有关离子(或物质)的检验、现象及结论,都正确的是
| A.向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色,该溶液中一定含有Fe2+ |
| B.向某溶液中滴加KSCN溶液,溶液变成红色,该溶液中一定不存在Fe2+ |
| C.将某种铁的氧化物溶于足量的稀硫酸中,取其溶液滴加酸性KMnO4溶液,振荡,溶液褪色,原氧化物中含有+2价铁 |
| D.向久置的FeCl2溶液中滴入用硫酸酸化的H2O2溶液,溶液变黄,滴加KSCN溶液,溶液变成红色,说明发生氧化还原反应,且氧化性:H2O2<Fe3+ |
您最近一年使用:0次
8 . 下列物质放置在空气中易变质,因发生氧化反应而变质的是
| A.Na2O2 | B.NaOH | C.FeCl2 | D.NaClO |
您最近一年使用:0次
9 . 下列离子方程式书写不正确的是
A.向 溴化亚铁溶液中通入标准状况下的 溴化亚铁溶液中通入标准状况下的 氯气: 氯气: |
B.硫酸亚铁溶液与稀硫酸、双氧水混合: |
C.碳酸钙溶于硝酸: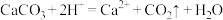 |
D.碳酸氢钠溶液与少量石灰水反应: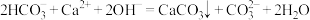 |
您最近一年使用:0次
10 . 实验室通过下列过程制取草酸亚铁晶体。
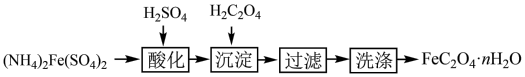
A.“酸化”后的溶液,根据电荷守恒存在等量关系:n( )+2×n(Fe2+)=2×n( )+2×n(Fe2+)=2×n( ) ) |
B.“沉淀”时发生反应的离子方程式:Fe2++ +nH2O=FeC2O4·nH2O↓ +nH2O=FeC2O4·nH2O↓ |
| C.可以用酸性KMnO4溶液检验“沉淀”后的上层清液中是否含有Fe2+ |
| D.“洗涤”时先水洗,再用乙醇洗涤,有利于晶体快速干燥和防止失去结晶水 |
您最近一年使用:0次



