名校
1 . 实验室制备 溶液并用于处理含氨氮废水。
溶液并用于处理含氨氮废水。
I:低温下将 通入
通入 溶液中制得
溶液中制得 溶液,装置如图所示。
溶液,装置如图所示。
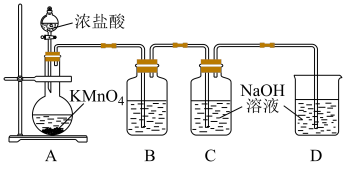
(1)装置B中盛放的试剂是___________ 。
(2)写出C装置中发生的化学方程式:___________ ,为了防止装置C温度升高生成副产物 ,可采取的操作为
,可采取的操作为___________ 。
II: 溶液处理含氨氮废水(
溶液处理含氨氮废水( 为
为 ),氨氮废水中的氮元素多以和
),氨氮废水中的氮元素多以和 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下:

已知:达标废水中氯元素主要以 形式存在。
形式存在。
(3)过程I的目的是将 转化为
转化为 ,并通过鼓入大显空气将氨气吹出,写出
,并通过鼓入大显空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
(4)过程II加入 溶液可将废水中的
溶液可将废水中的 转化为无毒物质,写出反应的离子方程式:
转化为无毒物质,写出反应的离子方程式:___________ 。
(5)含余氯废水的主要成分是 以及
以及 ,X可选用以下哪种物质以达到去除余氯的目的
,X可选用以下哪种物质以达到去除余氯的目的___________ (填字母),
a. b.
b. c.
c. d.
d.
写出其中一个反应的离子方程式:___________ 。
 溶液并用于处理含氨氮废水。
溶液并用于处理含氨氮废水。I:低温下将
 通入
通入 溶液中制得
溶液中制得 溶液,装置如图所示。
溶液,装置如图所示。
(1)装置B中盛放的试剂是
(2)写出C装置中发生的化学方程式:
 ,可采取的操作为
,可采取的操作为II:
 溶液处理含氨氮废水(
溶液处理含氨氮废水( 为
为 ),氨氮废水中的氮元素多以和
),氨氮废水中的氮元素多以和 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下:
已知:达标废水中氯元素主要以
 形式存在。
形式存在。(3)过程I的目的是将
 转化为
转化为 ,并通过鼓入大显空气将氨气吹出,写出
,并通过鼓入大显空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式:(4)过程II加入
 溶液可将废水中的
溶液可将废水中的 转化为无毒物质,写出反应的离子方程式:
转化为无毒物质,写出反应的离子方程式:(5)含余氯废水的主要成分是
 以及
以及 ,X可选用以下哪种物质以达到去除余氯的目的
,X可选用以下哪种物质以达到去除余氯的目的a.
 b.
b. c.
c. d.
d.
写出其中一个反应的离子方程式:
您最近一年使用:0次
解题方法
2 . 室温下,下列实验方案能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 取样,加入澄清石灰水,观察是否有沉淀产生 | 鉴别 溶液与 溶液与 溶液 溶液 |
| B | 取 溶液少许,滴加 溶液少许,滴加 溶液,向所得沉淀中加入足量稀盐酸,观察沉淀溶解程度 溶液,向所得沉淀中加入足量稀盐酸,观察沉淀溶解程度 | 检验 是否变质 是否变质 |
| C |  固体中滴加稀盐酸,加热,观察是否有黄绿色气体产生 固体中滴加稀盐酸,加热,观察是否有黄绿色气体产生 |  的氧化性比 的氧化性比 强 强 |
| D | 向装有 的试管中滴加少量水,观察是否有气泡产生 的试管中滴加少量水,观察是否有气泡产生 | 检验 是否变质 是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示如下:
,其实验过程可表示如下:
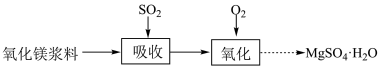
(1)在搅拌下向氧化镁浆料[主要成分为 ]中匀速缓慢通入
]中匀速缓慢通入 气体,生成
气体,生成 “吸收”过程中,发生的主要反应的化学方程式为
“吸收”过程中,发生的主要反应的化学方程式为________ 。
(2)在催化剂作用下 可被
可被 氧化为
氧化为 。“氧化”过程若转移
。“氧化”过程若转移 ,则消耗标准状况下
,则消耗标准状况下 的体积约为
的体积约为______ L。
(3)制取 晶体。将氧化后的溶液
晶体。将氧化后的溶液_____ 、_____ 、_____ (填写操作名称),洗涤,干燥,制得 晶体;
晶体;
 ,其实验过程可表示如下:
,其实验过程可表示如下:
(1)在搅拌下向氧化镁浆料[主要成分为
 ]中匀速缓慢通入
]中匀速缓慢通入 气体,生成
气体,生成 “吸收”过程中,发生的主要反应的化学方程式为
“吸收”过程中,发生的主要反应的化学方程式为(2)在催化剂作用下
 可被
可被 氧化为
氧化为 。“氧化”过程若转移
。“氧化”过程若转移 ,则消耗标准状况下
,则消耗标准状况下 的体积约为
的体积约为(3)制取
 晶体。将氧化后的溶液
晶体。将氧化后的溶液 晶体;
晶体;
您最近一年使用:0次
名校
解题方法
4 . 常温下,能大量共存的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
名校
5 . Ⅰ、有以下13种物质:①石墨 ②氯化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钠溶液 ⑧纯醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
(1)能导电的是_______ ;属于非电解质的是_______ 。
Ⅱ、“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(
,得到亚硫酸钠( )粗品。其流程如下:
)粗品。其流程如下:
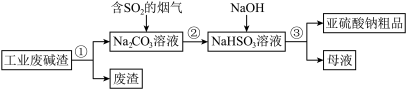
(2)过程①进行的操作是_______ 。
(3)上述流程中的 是酸性氧化物,原因是:
是酸性氧化物,原因是:_______ 。(用化学方程式表示)
(4)加入NaOH后,发生反应的离子方程式为_______ 。
(5)亚硫酸钠粗品中含有少量 ,原因是
,原因是_______ 。
(6)设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有 。
。
(1)能导电的是
Ⅱ、“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为
 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(
,得到亚硫酸钠( )粗品。其流程如下:
)粗品。其流程如下:
(2)过程①进行的操作是
(3)上述流程中的
 是酸性氧化物,原因是:
是酸性氧化物,原因是:(4)加入NaOH后,发生反应的离子方程式为
(5)亚硫酸钠粗品中含有少量
 ,原因是
,原因是(6)设计实验证明亚硫酸钠粗品含有少量
 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解, 。
。
您最近一年使用:0次
名校
6 . 实验室模拟“镁法工业烟气脱硫”并制备MgSO4∙H2O,其实验过程可表示如下:

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成 。
。
①“吸收”过程中,发生的主要反应的化学方程式为___________ ;
②64gSO2在标准状况下的体积约为___________ L;
③NaOH溶液也可以用于捕集SO2,配制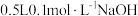 溶液,需NaOH
溶液,需NaOH___________ g;
(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为___________ L;
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,___________ (填写操作步骤),洗涤,干燥,制得MgSO4∙H2O晶体;
(4)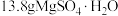 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为___________ mol。

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成
 。
。①“吸收”过程中,发生的主要反应的化学方程式为
②64gSO2在标准状况下的体积约为
③NaOH溶液也可以用于捕集SO2,配制
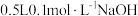 溶液,需NaOH
溶液,需NaOH(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,
(4)
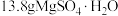 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为
您最近一年使用:0次
2023-11-09更新
|
172次组卷
|
2卷引用:江苏省扬州市江都区2023-2024学年高一上学期期中考试化学试题
名校
解题方法
7 . 填空。
(1)硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:
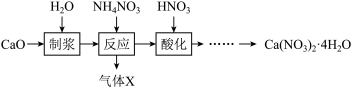
①“制浆”过程中发生反应的化学方程式是___________ 。
②“气体X”的化学式是___________ 。
③Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。
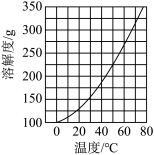
“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、___________ 、过滤、洗涤、干燥。实验室过滤操作必须用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。
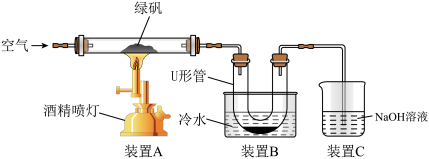
①实验过程中,装置A玻璃管中可观察到的实验现象是___________ 。
②装置C的作用是___________ 。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入___________ (填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有 的方法是
的方法是___________ 。
④某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,反应原理为:2(FeSO4•7H2O) Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程___________ 。
(1)硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:

①“制浆”过程中发生反应的化学方程式是
②“气体X”的化学式是
③Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。

“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、
(2)绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。

①实验过程中,装置A玻璃管中可观察到的实验现象是
②装置C的作用是
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入
 的方法是
的方法是④某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,反应原理为:2(FeSO4•7H2O)
 Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
您最近一年使用:0次
名校
8 . 室温下,为探究Na2SO3、 NaHSO3 溶液的性质,进行如下实验。
实验 1:测得 0.1mol·L-1NaHSO3 溶液的 pH 约为 5。
实验 2:向 0.1 mol·L -1 Na2SO3 溶液中滴加H2O2,再滴加 BaCl2 溶液,产生白色沉淀。
实验 3:向 0.1 mol·L-1 NaHSO3 中滴加少量 Ba(OH)2 溶液,产生白色沉淀
实验 4:向 0.1mol·L-1Na2SO3溶液中滴加少量酸性KMnO4 溶液,溶液的紫红色褪去。
下列说法正确的是:
实验 1:测得 0.1mol·L-1NaHSO3 溶液的 pH 约为 5。
实验 2:向 0.1 mol·L -1 Na2SO3 溶液中滴加H2O2,再滴加 BaCl2 溶液,产生白色沉淀。
实验 3:向 0.1 mol·L-1 NaHSO3 中滴加少量 Ba(OH)2 溶液,产生白色沉淀
实验 4:向 0.1mol·L-1Na2SO3溶液中滴加少量酸性KMnO4 溶液,溶液的紫红色褪去。
下列说法正确的是:
A.实验 1 中NaHSO3 溶液呈酸性的主要原因是HSO 在水中发生电离,产生了H+ 在水中发生电离,产生了H+ |
B.实验 2 说明SO 被H2O2 氧化生成了SO 被H2O2 氧化生成了SO |
C.实验 3 中发生的离子方程式为:Ba2++SO =BaSO3↓ =BaSO3↓ |
| D.实验 4 说明 Na2SO3溶液具有漂白性 |
您最近一年使用:0次
解题方法
9 . 下列物质的性质与用途具有对应关系的是
| A.NaHCO3受热易分解,可用于缓解胃酸过多 |
| B.Na2SO3具有还原性,可用作脱氧剂 |
| C.NaOH具有强碱性,可用作干燥剂 |
| D.Na2O2为淡黄色固体,可用作供氧剂 |
您最近一年使用:0次
名校
解题方法
10 . 元素周期表中第ⅥA族元素单质及其化合物有着广泛应用。 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 与
与 的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 与
与 的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是A. 有还原性,可用于吸收尾气 有还原性,可用于吸收尾气 | B. 有强氧化性,可用作食品的漂白剂 有强氧化性,可用作食品的漂白剂 |
| C.浓硫酸具有脱水性,可用作酯化反应的催化剂 | D.乙醇是有机溶剂,可用于萃取碘水中的碘单质 |
您最近一年使用:0次



