名校
解题方法
1 . 氯化亚铜(CuCl)微溶于水,易被氧化,广泛应用于医药等行业。以废铜渣(铜单质的质量分数为64%,CuO的质量分数为8%,其他杂质不含铜元素)为原料,可制备CuCl并获得副产品(NH4)2SO4,流程如图:
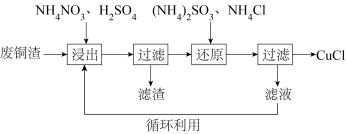
(1)“浸出”时发生的主要反应有:
反应Ⅰ:CuO与H2SO4反应的化学方程式为______ 。
反应Ⅱ:4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O。
①浸出温度为20℃时,铜元素浸出率随时间的变化如图所示。

铜元素浸出率=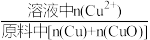 ×100%
×100%
结合图像,从反应速率的角度分析,可得出的结论是______ 。
②实际浸出温度选择65℃,可提高单位时间内铜元素浸出率。若温度过高,会产生红棕色气体,该气体的化学式为______ 。
(2)充分浸出后,“还原”时加入的(NH4)2SO3溶液需略过量,“还原”后的滤液经多次循环可提取一定量的(NH4)2SO4 (忽略转化流程中杂质参与的反应)。
①“还原”时(NH4)2SO4溶液过量的原因是______ 。
②假设铜元素完全浸出,忽略过量的(NH4)2SO4,计算100g废铜渣理论上可制得CuCl与(NH4)2SO4的物质的量(写出计算过程)。______

(1)“浸出”时发生的主要反应有:
反应Ⅰ:CuO与H2SO4反应的化学方程式为
反应Ⅱ:4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O。
①浸出温度为20℃时,铜元素浸出率随时间的变化如图所示。

铜元素浸出率=
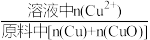 ×100%
×100%结合图像,从反应速率的角度分析,可得出的结论是
②实际浸出温度选择65℃,可提高单位时间内铜元素浸出率。若温度过高,会产生红棕色气体,该气体的化学式为
(2)充分浸出后,“还原”时加入的(NH4)2SO3溶液需略过量,“还原”后的滤液经多次循环可提取一定量的(NH4)2SO4 (忽略转化流程中杂质参与的反应)。
①“还原”时(NH4)2SO4溶液过量的原因是
②假设铜元素完全浸出,忽略过量的(NH4)2SO4,计算100g废铜渣理论上可制得CuCl与(NH4)2SO4的物质的量(写出计算过程)。
您最近一年使用:0次
名校
2 . 焦亚硫酸钠 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。
(1)化学兴趣小组同学利用下图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取 并探究
并探究 的性质。
的性质。
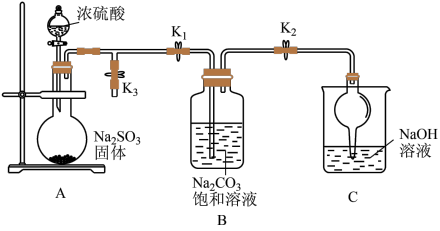
Ⅰ.打开 和
和 ,关闭
,关闭 ,制取
,制取 。
。
① 中O元素化合价为
中O元素化合价为 ,其中S的化合价为
,其中S的化合价为_______ ;装置C中干燥管的作用是_______ 。
②B中通入过量 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应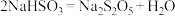 可获得
可获得 晶体。B中生成
晶体。B中生成 的化学方程式为
的化学方程式为_______ 。
③B中所得 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有_______ 。
④已知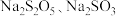 分别与稀硫酸反应得到的产物相同。请设计检验
分别与稀硫酸反应得到的产物相同。请设计检验 样品中是否含
样品中是否含 的实验方案
的实验方案_______ 。
Ⅱ.更换B瓶中的溶液,探究 的性质。
的性质。
⑤将B中溶液更换为品红的乙醇溶液,无明显现象;而将 通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是
通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是_______ 。(写化学式)
(2)葡萄酒中常加入 作抗氧化剂。测定某葡萄酒中
作抗氧化剂。测定某葡萄酒中 残留量的实验步骤如下:取
残留量的实验步骤如下:取 葡萄酒样品,用
葡萄酒样品,用 的
的 标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液
标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液 ,已知滴定过程中发生的反应为:
,已知滴定过程中发生的反应为: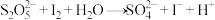 (未配平)。计算该葡萄酒中
(未配平)。计算该葡萄酒中 的残留量
的残留量_______ (以 为单位,写出计算过程)。
为单位,写出计算过程)。
 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。(1)化学兴趣小组同学利用下图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取
 并探究
并探究 的性质。
的性质。
Ⅰ.打开
 和
和 ,关闭
,关闭 ,制取
,制取 。
。①
 中O元素化合价为
中O元素化合价为 ,其中S的化合价为
,其中S的化合价为②B中通入过量
 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应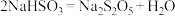 可获得
可获得 晶体。B中生成
晶体。B中生成 的化学方程式为
的化学方程式为③B中所得
 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有④已知
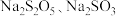 分别与稀硫酸反应得到的产物相同。请设计检验
分别与稀硫酸反应得到的产物相同。请设计检验 样品中是否含
样品中是否含 的实验方案
的实验方案Ⅱ.更换B瓶中的溶液,探究
 的性质。
的性质。⑤将B中溶液更换为品红的乙醇溶液,无明显现象;而将
 通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是
通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是(2)葡萄酒中常加入
 作抗氧化剂。测定某葡萄酒中
作抗氧化剂。测定某葡萄酒中 残留量的实验步骤如下:取
残留量的实验步骤如下:取 葡萄酒样品,用
葡萄酒样品,用 的
的 标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液
标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液 ,已知滴定过程中发生的反应为:
,已知滴定过程中发生的反应为: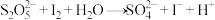 (未配平)。计算该葡萄酒中
(未配平)。计算该葡萄酒中 的残留量
的残留量 为单位,写出计算过程)。
为单位,写出计算过程)。
您最近一年使用:0次
3 . SO2、Na2SO3、Na2S2O5(焦亚硫酸钠)中都含有+4价的S,具有还原性。
(1)Na2SO3是实验室常用试剂。
①Na2SO3固体需密封保存,其原因是______ 。
②实验室用Na2SO3固体与浓硫酸制备SO2,该反应的化学方程式为______ 。
③在Br2水中加入Na2SO3溶液反应的离子方程式为______ 。
(2)一定条件下,将SO2通入TeOSO4溶液中,反应一段时间后过滤、洗涤得到粗Te。
①SO2还原TeOSO4溶液得到Te的反应中,n(SO2):n(TeOSO4)=______ 。
②“洗涤”的具体操作为______ 。
③过程中须控制反应温度为80℃,温度不能过高的原因是______ 。
(3)焦亚硫酸钠(Na2S2O5)空气法处理含氰废水的部分机理如下,其中[O]代表活性氧原子,具有强氧化性:S2O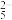 +H2O=2SO
+H2O=2SO +2H+、SO
+2H+、SO +O2=SO
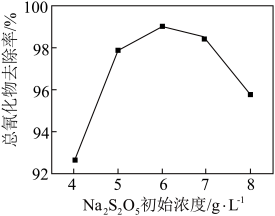
+O2=SO +[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是
+[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是______ 。
(1)Na2SO3是实验室常用试剂。
①Na2SO3固体需密封保存,其原因是
②实验室用Na2SO3固体与浓硫酸制备SO2,该反应的化学方程式为
③在Br2水中加入Na2SO3溶液反应的离子方程式为
(2)一定条件下,将SO2通入TeOSO4溶液中,反应一段时间后过滤、洗涤得到粗Te。
①SO2还原TeOSO4溶液得到Te的反应中,n(SO2):n(TeOSO4)=
②“洗涤”的具体操作为
③过程中须控制反应温度为80℃,温度不能过高的原因是
(3)焦亚硫酸钠(Na2S2O5)空气法处理含氰废水的部分机理如下,其中[O]代表活性氧原子,具有强氧化性:S2O
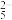 +H2O=2SO
+H2O=2SO +2H+、SO
+2H+、SO +O2=SO
+O2=SO +[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是
+[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是
您最近一年使用:0次
4 . 下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素,回答(1)(2)两小问
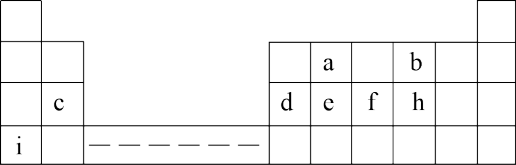
(1)a、b、c三种元素的原子半径由大到小的顺序是___________ (填元素符号);
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是_____ (填水化物的化学式)。
(3)配平下列离子方程式___ __MnO + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:___________ 。

(1)a、b、c三种元素的原子半径由大到小的顺序是
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是
(3)配平下列离子方程式
 + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:
您最近一年使用:0次
5 . 下列物质的性质与用途对应关系正确的是
A. 能与碱反应,可用作食品疏松剂 能与碱反应,可用作食品疏松剂 |
B. 具有还原性,可用于吸收含 具有还原性,可用于吸收含 的尾气 的尾气 |
| C.石墨具有还原性,可用作于电池的正极材料 |
| D.过氧化钠具有强氧化性,可用作漂白剂、消毒剂 |
您最近一年使用:0次
6 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生产,溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加1.0mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | 向少许待测溶液中滴加稀盐酸 | 有刺激性气味气体放出 | 待测液中一定含有SO |
| D | 加热盛有NH4Cl固体的试管 | 试管底部固体消失 | NH4Cl固体受热分解,产生氨气和氯化氢气体常温下重新结合成NH4Cl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-21更新
|
297次组卷
|
3卷引用:江苏省前黄高级中学2021-2022学年高一下学期4月调研考试化学试题
江苏省前黄高级中学2021-2022学年高一下学期4月调研考试化学试题山西省沁源县第一中学、榆社第一中学2021-2022学年高一下学期3月月考化学试题(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
7 . 下列物质的性质与用途对应关系,说法错误的是
| A.常温下浓硫酸能钝化铝,可用铝槽车贮运浓硫酸 |
| B.钠钾合金常温下呈液态,导热性好,可用于快中子反应堆的热交换剂 |
| C.Na2SO3具有还原性,可用于废水脱氯(Cl2) |
| D.NaHCO3能与碱反应,可用作抗酸药 |
您最近一年使用:0次
8 . 下列物质的性质与用途具有对应关系的是
| A.Al 的金属活泼性强,可用于制作铝金属制品 |
| B.S有氧化性,可用于生产SO2 |
| C.Na2SO3具有还原性,可用于废水脱氯(Cl2) |
| D.NaHCO3受热易分解,可用于制抗酸药物 |
您最近一年使用:0次
2022-01-14更新
|
547次组卷
|
6卷引用:江苏省苏州市2021-2022学年高一上学期期末学业质量阳光指标调研化学试题
名校
9 . 部分含硫物质的分类与相应的化合价关系如图,下列推断不合理的是
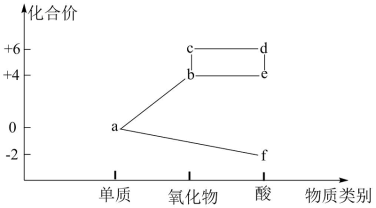

| A.b可与f反应生成a |
| B.b既可被氧化,也可被还原 |
| C.酸雨包括e→d的转化 |
| D.d的浓溶液与Cu反应可生成c |
您最近一年使用:0次
2021-12-22更新
|
2157次组卷
|
14卷引用:江苏省苏州市2022-2023学年高一上学期12月期末考试化学试题
江苏省苏州市2022-2023学年高一上学期12月期末考试化学试题(已下线)专题07 硫及含硫化合物 环境保护-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)(已下线)周末培优1 硫、氮及其化合物的相互转化-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)第15讲 硫酸-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)第五章 化工生产中的重要非金属元素(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)黑龙江省牡丹江市第三高级中学2022-2023学年高一下学期期中考试化学试题广东省湛江市坡头区第一中学2022-2023学年高一下学期期中考试化学试题河南省实验中学2023-2024学年高一上学期月考 化学试卷(已下线)第五章 化工生产中的重要非金属元素【单元测试B卷】云南省开远市第一中学校2023-2024学年高一下学期3月月考化学试题广东省广州市2021-2022学年高三上学期12月调研考试化学试题(已下线)押新高考卷03题 元素化合物的性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)化学-2022年高考考前押题密卷(广东卷)(已下线)考点巩固卷04 非金属及其化合物(4大考点60题)?-2024年高考化学一轮复习考点通关卷(新高考通用)
名校
10 . 在澄清溶液中能大量共存的一组离子是
A.Cu2+、SO 、OH-、K+ 、OH-、K+ | B.Fe3+、NO 、Cl-、H+ 、Cl-、H+ |
C.K+、CO 、Cl-、H+ 、Cl-、H+ | D.H+、Na+、ClO-、SO |
您最近一年使用:0次



