解题方法
1 . 室温下,下列实验方案能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 取样,加入澄清石灰水,观察是否有沉淀产生 | 鉴别 溶液与 溶液与 溶液 溶液 |
| B | 取 溶液少许,滴加 溶液少许,滴加 溶液,向所得沉淀中加入足量稀盐酸,观察沉淀溶解程度 溶液,向所得沉淀中加入足量稀盐酸,观察沉淀溶解程度 | 检验 是否变质 是否变质 |
| C |  固体中滴加稀盐酸,加热,观察是否有黄绿色气体产生 固体中滴加稀盐酸,加热,观察是否有黄绿色气体产生 |  的氧化性比 的氧化性比 强 强 |
| D | 向装有 的试管中滴加少量水,观察是否有气泡产生 的试管中滴加少量水,观察是否有气泡产生 | 检验 是否变质 是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示如下:
,其实验过程可表示如下:
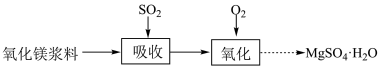
(1)在搅拌下向氧化镁浆料[主要成分为 ]中匀速缓慢通入
]中匀速缓慢通入 气体,生成
气体,生成 “吸收”过程中,发生的主要反应的化学方程式为
“吸收”过程中,发生的主要反应的化学方程式为________ 。
(2)在催化剂作用下 可被
可被 氧化为
氧化为 。“氧化”过程若转移
。“氧化”过程若转移 ,则消耗标准状况下
,则消耗标准状况下 的体积约为
的体积约为______ L。
(3)制取 晶体。将氧化后的溶液
晶体。将氧化后的溶液_____ 、_____ 、_____ (填写操作名称),洗涤,干燥,制得 晶体;
晶体;
 ,其实验过程可表示如下:
,其实验过程可表示如下:
(1)在搅拌下向氧化镁浆料[主要成分为
 ]中匀速缓慢通入
]中匀速缓慢通入 气体,生成
气体,生成 “吸收”过程中,发生的主要反应的化学方程式为
“吸收”过程中,发生的主要反应的化学方程式为(2)在催化剂作用下
 可被
可被 氧化为
氧化为 。“氧化”过程若转移
。“氧化”过程若转移 ,则消耗标准状况下
,则消耗标准状况下 的体积约为
的体积约为(3)制取
 晶体。将氧化后的溶液
晶体。将氧化后的溶液 晶体;
晶体;
您最近一年使用:0次
名校
解题方法
3 . 常温下,能大量共存的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
4 . 化学是以实验为基础的科学。根据下列实验操作和现象得出的结论错误的是
选项 | 实验操作和现象 | 结论 |
A | 用激光笔照射蛋白质溶液,在与光束垂直的方向观察到一条光亮的通路 | 蛋白质溶液中分散质粒子直径介于1~100 nm之间 |
B | 取一根洁净的铂丝,放在酒精灯火焰上灼烧至无色,然后蘸取少量试液,置于火焰上灼烧,火焰呈黄色 | 该试液一定含有 ,不能确定是否含有 ,不能确定是否含有 |
C | 向某白色粉末中滴加稀盐酸,产生的气体能使澄清石灰水变浑浊 | 该白色粉末一定是碳酸盐 |
D | 向某溶液中加入AgNO3溶液,产生白色浑浊 | 该溶液中不一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
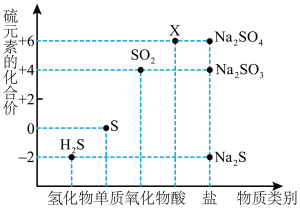
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(3)将H2S与SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目____________ 。
____Na2S+____Na2SO3+___H2SO4=____Na2SO4+____S↓+____H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设NA为阿伏加德罗常数的值。下列说法正确的是

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将H2S与SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
____Na2S+____Na2SO3+___H2SO4=____Na2SO4+____S↓+____H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
(6)设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 mol铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4 L SO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6 g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 mol Na2O2与足量H2O反应,转移的电子数为NA |
您最近一年使用:0次
名校
解题方法
6 . 在指定溶液中,下列离子一定能大量共存的是
A.透明澄清的溶液: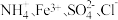 |
B.加入 NaHCO₃放出无色无味气体的溶液中: |
C.使酚酞变红的溶液: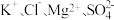 |
D.通入Cl₂至饱和的溶液: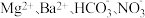 |
您最近一年使用:0次
名校
解题方法
7 . 常温下,在下列透明溶液中可能大量共存的离子组是
A.Fe2+、Mg2+、 、 、 | B.Fe3+、K+、Cl-、 |
C.Na+、 、OH-、 、OH-、 | D.H+、K+、S2-、 |
您最近一年使用:0次
名校
8 . 实验室模拟“镁法工业烟气脱硫”并制备MgSO4∙H2O,其实验过程可表示如下:

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成 。
。
①“吸收”过程中,发生的主要反应的化学方程式为___________ ;
②64gSO2在标准状况下的体积约为___________ L;
③NaOH溶液也可以用于捕集SO2,配制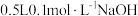 溶液,需NaOH
溶液,需NaOH___________ g;
(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为___________ L;
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,___________ (填写操作步骤),洗涤,干燥,制得MgSO4∙H2O晶体;
(4)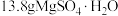 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为___________ mol。

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成
 。
。①“吸收”过程中,发生的主要反应的化学方程式为
②64gSO2在标准状况下的体积约为
③NaOH溶液也可以用于捕集SO2,配制
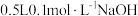 溶液,需NaOH
溶液,需NaOH(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,
(4)
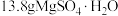 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为
您最近一年使用:0次
2023-11-09更新
|
174次组卷
|
2卷引用:江苏省扬州市江都区2023-2024学年高一上学期期中考试化学试题
名校
解题方法
9 . 设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。
ⅱ. 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。
某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,
溶液,___________ (填实验现象)。
上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是___________
(3)写出NO与碱性 溶液反应的离子方程式
溶液反应的离子方程式___________
(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: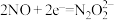 ,则氧化反应为:
,则氧化反应为:___________ 。
(5)某同学结合所学知识设计处理工业废气中 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式___________
②再向生成的溶液中加入一定量___________ ,以此溶液来吸收NO气体。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性
 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。资料:ⅰ.NO与碱性
 溶液会发生氧化还原反应,
溶液会发生氧化还原反应, 被还原为
被还原为 。
。ⅱ.
 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和
 溶液,加入少量冰醋酸,再滴加5滴
溶液,加入少量冰醋酸,再滴加5滴 的
的 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ:
(1)取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴
 的
的 溶液,
溶液,上述实验证明NO有氧化性。
(2)实验Ⅱ的目的是
(3)写出NO与碱性
 溶液反应的离子方程式
溶液反应的离子方程式(4)一个氧化还原反应可以看成“氧化”和“还原”两个半反应,试用此角度分析NO与碱性
 溶液的反应。若还原反应为:
溶液的反应。若还原反应为: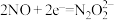 ,则氧化反应为:
,则氧化反应为:(5)某同学结合所学知识设计处理工业废气中
 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。①先用饱和纯碱溶液吸收废气中的
 ,生成
,生成 ,写出该反应的离子方程式
,写出该反应的离子方程式②再向生成的溶液中加入一定量
您最近一年使用:0次
名校
解题方法
10 . 某同学从物质类别、元素价态的角度,预测 和
和 部分化学性质。
部分化学性质。
(1)从物质类别角度, 属于酸性氧化物,预测
属于酸性氧化物,预测 可以和强碱反应,将少量
可以和强碱反应,将少量 通入NaOH溶液中,反应的离子方程式为
通入NaOH溶液中,反应的离子方程式为___________ 。
(2)从硫元素的价态角度分析, 既有氧化性又有还原性,
既有氧化性又有还原性,___________ 。
①将 通入酸性
通入酸性 溶液中,溶液紫色褪去,生成
溶液中,溶液紫色褪去,生成 。反应结束后,硫元素存在形式应该是
。反应结束后,硫元素存在形式应该是___________ 。
A. B.S C.
B.S C. D.
D.
② 还能和
还能和 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为___________ 。
(3)查阅资料后发现, 的部分化学性质与
的部分化学性质与 类似。该同学向
类似。该同学向 溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是___________ 。但在实验过程中,他并没有检测到该气体生成,可能的原因是___________ 。
 和
和 部分化学性质。
部分化学性质。(1)从物质类别角度,
 属于酸性氧化物,预测
属于酸性氧化物,预测 可以和强碱反应,将少量
可以和强碱反应,将少量 通入NaOH溶液中,反应的离子方程式为
通入NaOH溶液中,反应的离子方程式为(2)从硫元素的价态角度分析,
 既有氧化性又有还原性,
既有氧化性又有还原性,①将
 通入酸性
通入酸性 溶液中,溶液紫色褪去,生成
溶液中,溶液紫色褪去,生成 。反应结束后,硫元素存在形式应该是
。反应结束后,硫元素存在形式应该是A.
 B.S C.
B.S C. D.
D.
②
 还能和
还能和 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为(3)查阅资料后发现,
 的部分化学性质与
的部分化学性质与 类似。该同学向
类似。该同学向 溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
您最近一年使用:0次



