解题方法
1 . 图1是自然界中硫元素的存在示意图,图2表示硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:
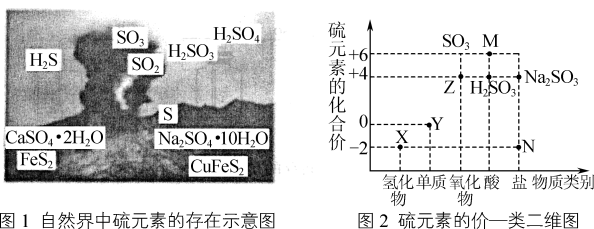
(1)图1中能与水反应生成强酸的物质的化学式为___________ 。
(2)煤的燃烧会产生大量SO2造成环境污染,下列关于SO2治理措施不可行的是___________(填字母)。
(3)Cu和M的浓溶液反应生成Z的化学方程式为___________ 。
(4)Na2SO3溶液易变质,实验室验证Na2SO3溶液已变质的操作和现象是___________ 。

(1)图1中能与水反应生成强酸的物质的化学式为
(2)煤的燃烧会产生大量SO2造成环境污染,下列关于SO2治理措施不可行的是___________(填字母)。
| A.在燃煤中添加生石灰固硫 | B. SO2 |
| C.将煤燃烧产生的尾气排放到高空 | D.用氨水吸收烟气中的SO2 |
(4)Na2SO3溶液易变质,实验室验证Na2SO3溶液已变质的操作和现象是
您最近半年使用:0次
2 . I.硫元素是动植物生长不可缺少的元素,硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是_______ 。
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是_______ 。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
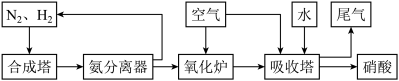
(3)合成塔中发生反应的化学方程式为_______ 。
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的_______ 性质。
(5)氧化炉中,NH3转化为NO的化学方程式为_______ 。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(3)合成塔中发生反应的化学方程式为
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(5)氧化炉中,NH3转化为NO的化学方程式为
您最近半年使用:0次
解题方法
3 . 依据图中硫元素及其化合物的转化关系,回答问题:
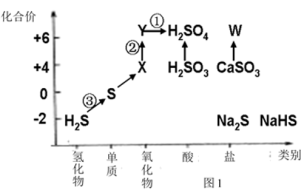
(1)图中,请写出反应①的离子方程式___________ 。
(2)图中,X的化学式为___________ ,从化合价上看,X具有___________ (填数字)
①氧化性;②还原性
(3)图中,W在医疗上可用作石膏绷带,关于它的用途还有___________ (填数字)。
①在工业上,可来调节水泥的硬化速率 ②在食品中,可用来作营养强化剂
③在美术上,可用来制作各种模型 ④在日常生活中,“卤水点豆腐”
(4)反应③可表示为H2S+Cl2=2HCl+S↓,当生成1molS时,转移的电子为___________ mol。也可表示为2H2S+SO2=3S↓+2H2O,当生成1molS时,转移的电子为___________ mol。
(5)SO2可使酸性高锰酸钾溶液褪色,体现了___________ (填数字)
①氧化性;②还原性;③漂白性。
请写出该反应的化学方程式:___________ 。

(1)图中,请写出反应①的离子方程式
(2)图中,X的化学式为
①氧化性;②还原性
(3)图中,W在医疗上可用作石膏绷带,关于它的用途还有
①在工业上,可来调节水泥的硬化速率 ②在食品中,可用来作营养强化剂
③在美术上,可用来制作各种模型 ④在日常生活中,“卤水点豆腐”
(4)反应③可表示为H2S+Cl2=2HCl+S↓,当生成1molS时,转移的电子为
(5)SO2可使酸性高锰酸钾溶液褪色,体现了
①氧化性;②还原性;③漂白性。
请写出该反应的化学方程式:
您最近半年使用:0次
名校
4 . 钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是____ 。
(2)向上述所得溶液中加入KClO3溶液,完善并配平反应的离子方程式______ 。
ClO + VO2++ = Cl-+ VO
+ VO2++ = Cl-+ VO +
+
(3) V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是____ 。
(4)在20.00 mL 0.1 mol.L-1 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 ___ 。
a.VO2+ b. c. V2+ d.V
c. V2+ d.V
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(2)向上述所得溶液中加入KClO3溶液,完善并配平反应的离子方程式
ClO
 + VO2++ = Cl-+ VO
+ VO2++ = Cl-+ VO +
+ (3) V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则
 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是(4)在20.00 mL 0.1 mol.L-1
 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 a.VO2+ b.
 c. V2+ d.V
c. V2+ d.V
您最近半年使用:0次
2021-01-31更新
|
660次组卷
|
4卷引用:安徽省合肥市2021年高三第一次教学质量检测化学试题
安徽省合肥市2021年高三第一次教学质量检测化学试题(已下线)热点10 氧化还原反应与电极反应-2021年高考化学【热点·重点·难点】专练(新高考)山东省泰安市宁阳县第四中学2022-2023学年高三上学期10月月考化学试题(等级考)山东省泰安市宁阳县第四中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
5 . 氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_____ (选填编号)。
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。
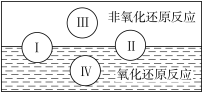
试写出有水参加且符合反应类型 IV 的一个化学方程式:___________________ 。
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
_____ NaIO3+ NaHSO3→ I2+ Na2SO4+ H2SO4+ H2O
②该反应还原剂是_____ ,_____ 元素被还原,若生成 1mol 氧化产物则转移电子数目为_____ NA。
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-_____ I-(填“>”或“<”),完成该反应_____________________________________ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。

试写出有水参加且符合反应类型 IV 的一个化学方程式:
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
②该反应还原剂是
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-
您最近半年使用:0次
2017-12-22更新
|
280次组卷
|
2卷引用:上海交通大学附属中学2017-2018学年高一12月月考化学试题
10-11高三上·四川成都·阶段练习
解题方法
6 . (Ⅰ)近年来我国对碳纳米管的研究也有了较大突破,即用电弧合成法来制碳纳米管,但往往有大量的碳纳米颗粒,需用氧化法来提纯这些颗粒,化学方程式为:

试回答下列问题:
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂为_______ ,被氧化的元素为________ 。
(3)H2SO4在上述反应中表现出来的性质是___ (填字母)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若生成11 g CO2,则转移电子的数目为__________ 。
(Ⅱ)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1型流感(或称H1N1型猪流感)疫情,随后也不断蔓延我国各地.防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感.
(5)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
_______________________________________________________
(6)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只被还原的是____ 。
A. MnO2 B.KMnO4溶液
C.稀盐酸 D.Na2SO3溶液
(7)漂白剂亚氯酸钠(NaClO2)在常温于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是____ 。

试回答下列问题:
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂为
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若生成11 g CO2,则转移电子的数目为
(Ⅱ)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1型流感(或称H1N1型猪流感)疫情,随后也不断蔓延我国各地.防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感.
(5)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
(6)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只被还原的是
A. MnO2 B.KMnO4溶液
C.稀盐酸 D.Na2SO3溶液
(7)漂白剂亚氯酸钠(NaClO2)在常温于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是
您最近半年使用:0次



