名校
解题方法
1 . 硫、氮元素是高中化学学习的两种重要非金属元素,其价类二维图分别如图所示:
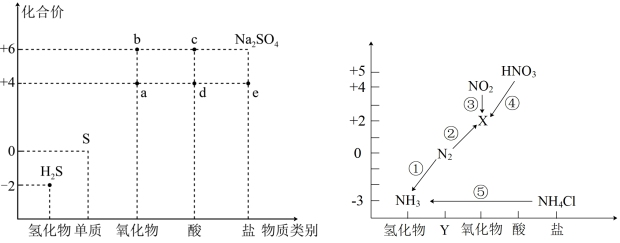
(1)图中物质“d”的化学式是_______ ;“Y”代表的物质类别是_______ 。
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______(填标号)。
(3)写出反应③的离子方程式:_______ 。
(4)H2S水溶液的俗名为_______ 。d的溶液与H2S发生反应的化学方程式:_______ 。
(5)已知e为钾元素的正盐,且能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O 被还原为Cr3+,写出此反应的化学方程式:
被还原为Cr3+,写出此反应的化学方程式:_______ 。
(6)图为合成氨以及氨氧化制硝酸的流程示意图:
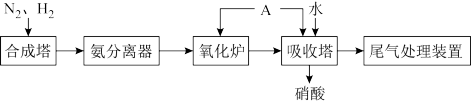
为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积比的范围是_______ 。

(1)图中物质“d”的化学式是
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______(填标号)。
| A.Ba(NO3)2溶液 | B.CaCl2溶液 | C.H2O2溶液 | D.Na2CO3溶液 |
(4)H2S水溶液的俗名为
(5)已知e为钾元素的正盐,且能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O
 被还原为Cr3+,写出此反应的化学方程式:
被还原为Cr3+,写出此反应的化学方程式:(6)图为合成氨以及氨氧化制硝酸的流程示意图:

为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积比的范围是
您最近一年使用:0次
解题方法
2 . 写出符合下列要求的离子反应方程式。
(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:__ 。
(2)向NaHSO4溶液中滴加过量氢氧化钡溶液,离子反应方程式为:__ 。
(3)向1Llmol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液,离子反应方程式为:___ 。
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO 还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为
还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为__ 。
(5)利用 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为__ 。
(6)Fe的一种含氧酸根FeO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是__ 。
(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:
(2)向NaHSO4溶液中滴加过量氢氧化钡溶液,离子反应方程式为:
(3)向1Llmol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液,离子反应方程式为:
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO
 还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为
还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为(5)利用
 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为(6)Fe的一种含氧酸根FeO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近一年使用:0次
3 . 某溶液中含有 、Na+、
、Na+、 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
(1)离子浓度保持不变的是___________ ;
(2)离子浓度减小的是___________ ;
(3)离子浓度增大的是___________ ;
(4)其中发生的非氧化还原反应有___________ (用离子方程式表示);
(5)发生的氧化还原反应的有___________ (用离子方程式表示);。
 、Na+、
、Na+、 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:(1)离子浓度保持不变的是
(2)离子浓度减小的是
(3)离子浓度增大的是
(4)其中发生的非氧化还原反应有
(5)发生的氧化还原反应的有
您最近一年使用:0次
名校
解题方法
4 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,请分析此图并回答有关问题。
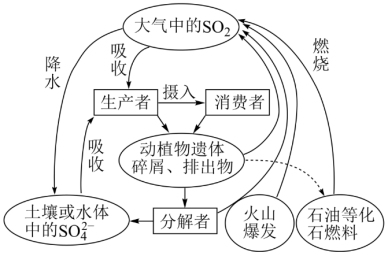
(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是________ 。
(2)分解者可将含硫有机物分解为H2S,硫磺细菌和硫化细菌可将H2S进一步变为硫单质或硫酸盐,下列关于硫化氢说法正确的是_______ 。
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是_________________ ,收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是________________ 。(用化学方程式表示)
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ (填化学式)。

(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是
| 选项 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫元素不会进入大气 |
| B | 氮循环过程有生物圈参与 | 硫循环过程无生物圈参与 | |
| C | 同 | 人类活动对氮循环和硫循环都造成巨大影响 | |
| D | 氮循环和硫循环对环境的影响是都能导致温室效应 | ||
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是
您最近一年使用:0次



