名校
解题方法
1 . 钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)工业上先用 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液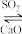 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是___________ 。(用化学方程式表示)
(2)常温下进行“钠碱法”的模拟实验。用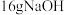 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________  (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了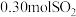 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:___________ 。(写出溶质组成和每种溶质的物质的量)
(3)若用碱液吸收工业尾气中的 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式___________ 。
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)工业上先用
 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液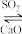 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是(2)常温下进行“钠碱法”的模拟实验。用
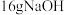 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为 (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了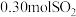 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:(3)若用碱液吸收工业尾气中的
 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式
您最近半年使用:0次
名校
解题方法
2 .  是一种重要的大气污染物。氨水、
是一种重要的大气污染物。氨水、 水悬浊液吸收烟气中
水悬浊液吸收烟气中 后经
后经 催化氧化,可得到某些硫酸盐。溶液中
催化氧化,可得到某些硫酸盐。溶液中 、
、 、
、 的物质的量分数随
的物质的量分数随 的分布如图1所示。
的分布如图1所示。
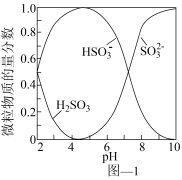
已知:室温下,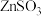 微溶于水,
微溶于水, 易溶于水;回答下列问题:
易溶于水;回答下列问题:
(1)氨水吸收 。向氨水中通入过量
。向氨水中通入过量 ,主要反应的离子方程式为
,主要反应的离子方程式为_______ ;当通入 至溶液
至溶液 时,溶液中大量存在的阴离子是
时,溶液中大量存在的阴离子是_______ (填化学式)。
(2) 水悬浊液吸收
水悬浊液吸收 。向
。向 水悬浊液中匀速缓慢通入
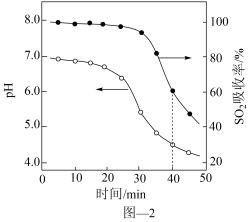
水悬浊液中匀速缓慢通入 ,在开始吸收的40min内,
,在开始吸收的40min内, 吸收率、溶液
吸收率、溶液 均经历了从几乎不变到迅速降低的变化(如图2),溶液
均经历了从几乎不变到迅速降低的变化(如图2),溶液 几乎不变阶段,主要产物是
几乎不变阶段,主要产物是_______ (填化学式); 吸收率迅速降低阶段,
吸收率迅速降低阶段, 也迅速降低的主要原因
也迅速降低的主要原因_______ ,该阶段主要反应的离子方程式为_______ 。若增大气体流速,会使 的吸收率
的吸收率_______ (填“增大”、“减小”或“不变”)。
(3) 催化氧化。其他条件相同时,调节吸收
催化氧化。其他条件相同时,调节吸收 得到溶液的
得到溶液的 在4.5~6.5范围内,该范围内
在4.5~6.5范围内,该范围内 越低
越低 生成速率越大,其主要原因是
生成速率越大,其主要原因是_______ ;随着氧化反应的进行,溶液的 将
将_______ (填“增大”、“减小”或“不变”)。
 是一种重要的大气污染物。氨水、
是一种重要的大气污染物。氨水、 水悬浊液吸收烟气中
水悬浊液吸收烟气中 后经
后经 催化氧化,可得到某些硫酸盐。溶液中
催化氧化,可得到某些硫酸盐。溶液中 、
、 、
、 的物质的量分数随
的物质的量分数随 的分布如图1所示。
的分布如图1所示。
已知:室温下,
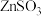 微溶于水,
微溶于水, 易溶于水;回答下列问题:
易溶于水;回答下列问题:(1)氨水吸收
 。向氨水中通入过量
。向氨水中通入过量 ,主要反应的离子方程式为
,主要反应的离子方程式为 至溶液
至溶液 时,溶液中大量存在的阴离子是
时,溶液中大量存在的阴离子是(2)
 水悬浊液吸收
水悬浊液吸收 。向
。向 水悬浊液中匀速缓慢通入
水悬浊液中匀速缓慢通入 ,在开始吸收的40min内,
,在开始吸收的40min内, 吸收率、溶液
吸收率、溶液 均经历了从几乎不变到迅速降低的变化(如图2),溶液
均经历了从几乎不变到迅速降低的变化(如图2),溶液 几乎不变阶段,主要产物是
几乎不变阶段,主要产物是 吸收率迅速降低阶段,
吸收率迅速降低阶段, 也迅速降低的主要原因
也迅速降低的主要原因 的吸收率
的吸收率
(3)
 催化氧化。其他条件相同时,调节吸收
催化氧化。其他条件相同时,调节吸收 得到溶液的
得到溶液的 在4.5~6.5范围内,该范围内
在4.5~6.5范围内,该范围内 越低
越低 生成速率越大,其主要原因是
生成速率越大,其主要原因是 将
将
您最近半年使用:0次
2022-11-11更新
|
192次组卷
|
2卷引用:山东省菏泽市郓城第一中学2022-2023学年高二上学期期中考试化学试题
3 . I.某地出现硫酸型酸雨,现采集了一份雨水样品,其pH随时间变化如下:
(1)用化学方程式表示雨水样品pH变化的原因_______ 。
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气), pH将_______ (选填“变大”、 “变小”、 “不变”。反应的方程式为_______ 。
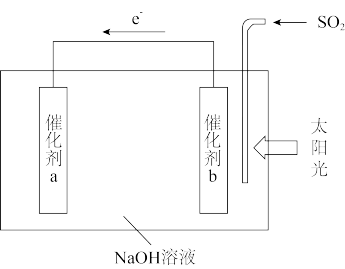
(3)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。产生标况下2.24LH2时,脱除SO2_______ g。
II.如图是土壤中发生的氮循环示意图,回答下列问题:
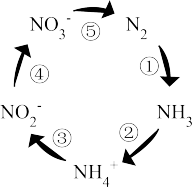
(4)固氮过程的序 号是_______ 。人工固氮的反应方程式为_______ 。
(5)为了消除NOx对大气的污染,工业上通常利用NH3还原的方法实现无害化处理,现有 NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为_______ 。
| 测试时间/h | 0 | 2 | 4 | 6 |
| pH | 4.73 | 4.55 | 4.42 | 4.41 |
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气), pH将
(3)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。产生标况下2.24LH2时,脱除SO2

II.如图是土壤中发生的氮循环示意图,回答下列问题:

(4)固氮过程的序 号是
(5)为了消除NOx对大气的污染,工业上通常利用NH3还原的方法实现无害化处理,现有 NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为
您最近半年使用:0次
名校
解题方法
4 . 硫、氮元素是高中化学学习的两种重要非金属元素,其价类二维图分别如图所示:
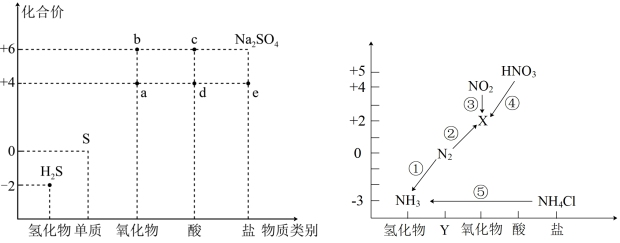
(1)图中物质“d”的化学式是_______ ;“Y”代表的物质类别是_______ 。
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______(填标号)。
(3)写出反应③的离子方程式:_______ 。
(4)H2S水溶液的俗名为_______ 。d的溶液与H2S发生反应的化学方程式:_______ 。
(5)已知e为钾元素的正盐,且能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O 被还原为Cr3+,写出此反应的化学方程式:
被还原为Cr3+,写出此反应的化学方程式:_______ 。
(6)图为合成氨以及氨氧化制硝酸的流程示意图:
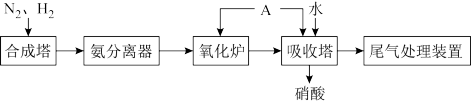
为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积比的范围是_______ 。

(1)图中物质“d”的化学式是
(2)将足量的a气体通入下列溶液中,始终没有明显反应现象的是_______(填标号)。
| A.Ba(NO3)2溶液 | B.CaCl2溶液 | C.H2O2溶液 | D.Na2CO3溶液 |
(4)H2S水溶液的俗名为
(5)已知e为钾元素的正盐,且能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O
 被还原为Cr3+,写出此反应的化学方程式:
被还原为Cr3+,写出此反应的化学方程式:(6)图为合成氨以及氨氧化制硝酸的流程示意图:

为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积比的范围是
您最近半年使用:0次
名校
5 . 油画的白色燃料中曾含二价铅盐,二价铅盐经过长时间空气(含有微量H2S)的侵蚀,生成PbS而变黑。可用一定量的H2O2溶液擦铁修复。完成下列填空:
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式___________ 。
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为___________ 。当PbSO4和CH3COONH4恰好完全反应时,溶液显___________ 性(选填“酸性”、“中性”或“碱性”)。
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为___________ ;该物质在空气中很快变为红褐色,原因是___________ 。
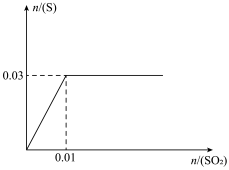
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为___________ 。从开始通SO2至饱和,再继续通一段时间,整个过程中c(H+)的变化情况为___________ 。
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S
 +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
您最近半年使用:0次
解题方法
6 . 写出符合下列要求的离子反应方程式。
(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:__ 。
(2)向NaHSO4溶液中滴加过量氢氧化钡溶液,离子反应方程式为:__ 。
(3)向1Llmol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液,离子反应方程式为:___ 。
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO 还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为
还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为__ 。
(5)利用 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为__ 。
(6)Fe的一种含氧酸根FeO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是__ 。
(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:
(2)向NaHSO4溶液中滴加过量氢氧化钡溶液,离子反应方程式为:
(3)向1Llmol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液,离子反应方程式为:
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO
 还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为
还原为N2,一段时间后溶液碱性明显增强。上述反应的离子方程式为(5)利用
 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为(6)Fe的一种含氧酸根FeO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近半年使用:0次
7 . 某溶液中含有 、Na+、
、Na+、 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
(1)离子浓度保持不变的是___________ ;
(2)离子浓度减小的是___________ ;
(3)离子浓度增大的是___________ ;
(4)其中发生的非氧化还原反应有___________ (用离子方程式表示);
(5)发生的氧化还原反应的有___________ (用离子方程式表示);。
 、Na+、
、Na+、 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:(1)离子浓度保持不变的是
(2)离子浓度减小的是
(3)离子浓度增大的是
(4)其中发生的非氧化还原反应有
(5)发生的氧化还原反应的有
您最近半年使用:0次
8 . I.利用下图装置制备 ,并研究
,并研究 的性质。
的性质。
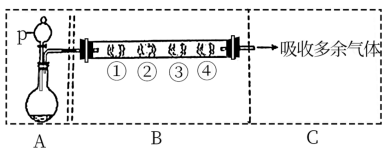
(1)A装置利用亚硫酸钠和硫酸反应制备 ,写出化学方程式
,写出化学方程式_______ 。
(2)填写下表
(3) 和氯气按照体积比
和氯气按照体积比 通入水中,溶液的漂白性
通入水中,溶液的漂白性_______ (填“增强”“减弱”“不变”)原因是_______ (用化学方程式表示)。
II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(4)上述流程中,加入 后,发生反应的化学方程式为
后,发生反应的化学方程式为_______ 。
(5)亚硫酸钠粗品中含有少量 ,原因是
,原因是_______ 。
 ,并研究
,并研究 的性质。
的性质。
(1)A装置利用亚硫酸钠和硫酸反应制备
 ,写出化学方程式
,写出化学方程式(2)填写下表
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 褪色 | 浅黄色 | ||
体现 的性质 的性质 |
(3)
 和氯气按照体积比
和氯气按照体积比 通入水中,溶液的漂白性
通入水中,溶液的漂白性II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为
 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
(4)上述流程中,加入
 后,发生反应的化学方程式为
后,发生反应的化学方程式为(5)亚硫酸钠粗品中含有少量
 ,原因是
,原因是
您最近半年使用:0次
9 . 酸雨的危害很大,能直接破坏农作物、腐蚀建筑物,还会危害人体健康。SO2、NOx是形成酸雨的主要物质,研究SO2、NOx等对减少酸雨,改善空气质量具有重要意义。请回答下列问题:
(1)酸雨是指pH_______ 的雨水。
(2)NOx主要来源于汽车尾气。硝酸型酸雨的形成过程中涉及的化学方程式有:① ;②
;②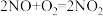 ;③
;③_______ 。
(3)SO2主要是煤、石油等燃烧产生,为减少SO2的排放,可采取下列有效措施:
①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是_______ 。
②在一定条件下用CO还原SO2得到单质硫的方法来除去SO2,该反应的化学方程式为_______ 。
③用氨水将SO2转化为NH4HSO3,再氧化成 来脱除烟气中的SO2,原理是
来脱除烟气中的SO2,原理是_______ 、_______ (用离子方程式表示)。
(1)酸雨是指pH
(2)NOx主要来源于汽车尾气。硝酸型酸雨的形成过程中涉及的化学方程式有:①
 ;②
;②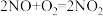 ;③
;③(3)SO2主要是煤、石油等燃烧产生,为减少SO2的排放,可采取下列有效措施:
①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是
②在一定条件下用CO还原SO2得到单质硫的方法来除去SO2,该反应的化学方程式为
③用氨水将SO2转化为NH4HSO3,再氧化成
 来脱除烟气中的SO2,原理是
来脱除烟气中的SO2,原理是
您最近半年使用:0次
2021-02-07更新
|
171次组卷
|
2卷引用:山西省大同市灵丘一中、广灵一中2020-2021学年高一下学期期中联考化学试题
解题方法
10 . (1)在一定条件下,可以用H2O2氧化H2S。随着参加反应的 变化,氧化产物不同,当
变化,氧化产物不同,当 =4时,氧化产物的分子式为
=4时,氧化产物的分子式为________ 。
(2)利用废铁屑制备聚合硫酸铁的过程中,需要向反应釜中加入氧化剂氧化Fe2+,最合适的是________ 。
(3)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为______________ 。
(4)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_____________ 。
(5)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式___________ 。
(6)NH3在催化剂条件下还原NO2生成N2和H2O的化学方程式:_________________ 。
 变化,氧化产物不同,当
变化,氧化产物不同,当 =4时,氧化产物的分子式为
=4时,氧化产物的分子式为(2)利用废铁屑制备聚合硫酸铁的过程中,需要向反应釜中加入氧化剂氧化Fe2+,最合适的是
(3)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO
 ,常用作脱氯剂,该反应的离子方程式为
,常用作脱氯剂,该反应的离子方程式为(4)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
(5)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式
(6)NH3在催化剂条件下还原NO2生成N2和H2O的化学方程式:
您最近半年使用:0次



