名校
1 . “以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:___________ (写出一种即可)。
(2)将碳酸钠溶液吸收烟气中的SO2的化学方程式补充完整:___________ 。
SO2+Na2CO3+______=NaHSO3+CO2
(3)上述流程中,加入NaOH后,发生反应的化学方程式为___________ 。
(4)亚硫酸钠(Na2SO3)中硫的化合价是___________ 。亚硫酸钠粗品中常含有少量的硫酸钠,可能的原因是___________ 。

(2)将碳酸钠溶液吸收烟气中的SO2的化学方程式补充完整:
SO2+Na2CO3+______=NaHSO3+CO2
(3)上述流程中,加入NaOH后,发生反应的化学方程式为
(4)亚硫酸钠(Na2SO3)中硫的化合价是
您最近一年使用:0次
2023-12-27更新
|
106次组卷
|
2卷引用:北京市北京师范大学附属实验中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
2 . 填空。
(1)硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:
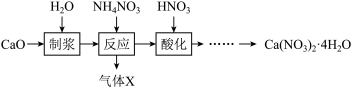
①“制浆”过程中发生反应的化学方程式是___________ 。
②“气体X”的化学式是___________ 。
③Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。
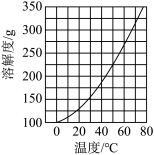
“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、___________ 、过滤、洗涤、干燥。实验室过滤操作必须用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。
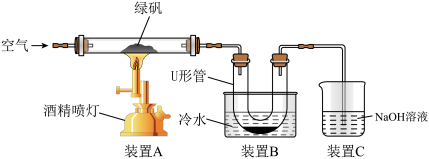
①实验过程中,装置A玻璃管中可观察到的实验现象是___________ 。
②装置C的作用是___________ 。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入___________ (填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有 的方法是
的方法是___________ 。
④某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,反应原理为:2(FeSO4•7H2O) Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程___________ 。
(1)硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:

①“制浆”过程中发生反应的化学方程式是
②“气体X”的化学式是
③Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。

“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、
(2)绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。

①实验过程中,装置A玻璃管中可观察到的实验现象是
②装置C的作用是
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入
 的方法是
的方法是④某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,反应原理为:2(FeSO4•7H2O)
 Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
您最近一年使用:0次
名校
解题方法
3 . 已知: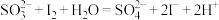 。某溶液中可能含有
。某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 ,且所有离子的物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
,且所有离子的物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
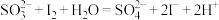 。某溶液中可能含有
。某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 ,且所有离子的物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
,且所有离子的物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是A.肯定不含 | B.肯定含有 |
C.肯定含有 | D.肯定含有 |
您最近一年使用:0次
2023-03-05更新
|
702次组卷
|
11卷引用:黑龙江省哈尔滨市第六中学2020-2021学年高一4月月考化学试题
黑龙江省哈尔滨市第六中学2020-2021学年高一4月月考化学试题人教版(2019)高一必修第一册 模块综合测评-B卷黑龙江省大庆实验中学2020-2021学年高一上学期第一次线上教学质量检测(1月)化学试题江西宜春市铜鼓中学2022-2023学年高一下学期第一次段考化学试题辽宁省沈阳市第一二〇中学2022-2023学年高一下学期期初质量监测化学试题山西省太原市第五中学校2022-2023学年高一下学期3月月考试题化学试题安徽省当涂第一中学2022-2023学年高一下学期4月期中化学试题四川省射洪中学校2022-2023学年高一下学期期中考试化学试题四川省华蓥中学2022-2023学年高一下学期5月月考化学试题河北省石家庄市2023-2024学年高一上学期期末教学质量检测化学试题(已下线)热点02 氮及其化合物
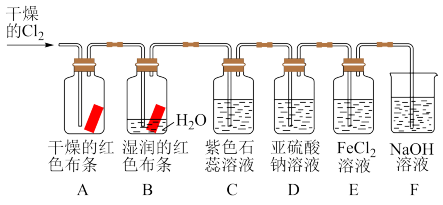
4 . 根据下列装置图回答问题: 后,观察到的现象是
后,观察到的现象是_______ ,根据现象可得出的结论是_______ 。
(2)装置B中发生反应的离子方程式是_______ 。
(3)实验开始后,观察装置C中的现象是_______ 。
(4)通入 时装置D中发生反应的离子方程式是
时装置D中发生反应的离子方程式是_______ 。
(5)装置E中发生反应的离子方程式是_______ 。
(6)装置F的作用是_______ 。
 后,观察到的现象是
后,观察到的现象是(2)装置B中发生反应的离子方程式是
(3)实验开始后,观察装置C中的现象是
(4)通入
 时装置D中发生反应的离子方程式是
时装置D中发生反应的离子方程式是(5)装置E中发生反应的离子方程式是
(6)装置F的作用是
您最近一年使用:0次
2023-02-09更新
|
356次组卷
|
8卷引用:2.2.1 氯气的性质-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)(附参考答案)
(已下线)2.2.1 氯气的性质-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)(附参考答案)福建省厦门外国语学校2021-2022学年高一上学期第一次月考(10月)化学试题江西省南昌市知行中学2021-2022学年高一上学期期中化学试题(已下线)2.2.1 氯气的性质-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)安徽省霍邱县第二中学2019-2020学年高一下学期段考化学试题吉林省长春市长春外国语学校2020-2021学年高一上学期期中考试化学(理科)试题第四章 非金属及其化合物 第18讲 氯及其化合物(已下线)知识清单09 氯及其重要化合物-【上好课】2025年高考化学一轮复习知识清单(新高考专用)
5 . 某溶液中可能含有K+、Na+、Mg2+、 、Fe2+、Br-、
、Fe2+、Br-、 、
、 、
、 中的若干种离子。某同学做了如下实验:①取少量溶液,滴加足量氯水,有气泡产生且溶液颜色变成黄色②另取少量溶液,滴加盐酸酸化的氯化钡溶液,无沉淀生成③蘸取原溶液,做焰色试验,透过蓝色钴玻璃观察到火焰呈紫色。为进一步确定该溶液的组成,无需进行的实验是
中的若干种离子。某同学做了如下实验:①取少量溶液,滴加足量氯水,有气泡产生且溶液颜色变成黄色②另取少量溶液,滴加盐酸酸化的氯化钡溶液,无沉淀生成③蘸取原溶液,做焰色试验,透过蓝色钴玻璃观察到火焰呈紫色。为进一步确定该溶液的组成,无需进行的实验是
 、Fe2+、Br-、
、Fe2+、Br-、 、
、 、
、 中的若干种离子。某同学做了如下实验:①取少量溶液,滴加足量氯水,有气泡产生且溶液颜色变成黄色②另取少量溶液,滴加盐酸酸化的氯化钡溶液,无沉淀生成③蘸取原溶液,做焰色试验,透过蓝色钴玻璃观察到火焰呈紫色。为进一步确定该溶液的组成,无需进行的实验是
中的若干种离子。某同学做了如下实验:①取少量溶液,滴加足量氯水,有气泡产生且溶液颜色变成黄色②另取少量溶液,滴加盐酸酸化的氯化钡溶液,无沉淀生成③蘸取原溶液,做焰色试验,透过蓝色钴玻璃观察到火焰呈紫色。为进一步确定该溶液的组成,无需进行的实验是| A.取少量溶液,滴加氯水和CCl4,振荡、静置 |
| B.上述实验③不透过蓝色钴玻璃观察火焰颜色 |
| C.取少量溶液,滴加适量的稀硫酸和品红溶液 |
| D.取少量溶液,滴加适量浓NaOH溶液,加热,用湿润的红色石蕊试纸检验气体 |
您最近一年使用:0次
2023-01-31更新
|
567次组卷
|
13卷引用:辽宁省兴城市高级中学2021-2022学年高三上学期10月月考化学试题
辽宁省兴城市高级中学2021-2022学年高三上学期10月月考化学试题浙江省宁波市2018年3月新高考选考适应性考试化学试题【全国百强校】河北省邢台市第一中学2017-2018学年高二下学期第三次月考化学试题(已下线)2018年高考题及模拟题汇编 专题03 离子反应(已下线)学科网2019年高考化学一轮复习讲练测 2.2 离子反应 离子共存及检验 讲【全国百强校】浙江省嘉兴市第一中学2019届高三上学期期末考试化学试题浙江省“七彩阳光”新高考研究联盟2018-2019学年高一下学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——常见无机物及其性质应用——氮及其化合物(提升练习)河南省洛阳市2019-2020学年高三上学期尖子生第一次考试化学试题浙江省瑞安市上海新纪元高级中学2019-2020学年高一下学期期末考试化学试题(1)黑龙江省哈尔滨市第三中学校2021届高三上学期第二次验收考试化学试题(已下线)专题06 离子共存、检验和推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)黑龙江省齐齐哈尔三立高中2022-2023学年高一下学期期初考试化学试题
解题方法
6 . 工业上制取硫酸,回收尾气中的废气常选用的试剂是
| A.氨水 | B.NaOH | C.H2SO3 | D.H2SO4 |
您最近一年使用:0次
名校
解题方法
7 . 10mL某无色溶液中可能存在如下离子,取该溶液进行下述实验(不考虑水解),下列推理正确的是
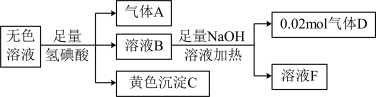
| 阳离子 | NH 、Na+、Ag+、Al3+ 、Na+、Ag+、Al3+ |
| 阴离子 | CO 、S2-、SO 、S2-、SO 、Cr2O 、Cr2O |

A.气体A通入澄清石灰水中,溶液变浑浊,不能确定无色溶液中含有CO |
B.溶液B与足量NaOH溶液加热生成0.02mol气体D,说明无色溶液含有NH 的浓度为2mol/L 的浓度为2mol/L |
| C.生成黄色沉淀C,说明无色溶液含有Ag+ |
| D.用洁净的铂丝蘸取溶液F在火焰上灼烧,火焰呈黄色,说明原无色溶液含有Na+ |
您最近一年使用:0次
2022-12-13更新
|
335次组卷
|
3卷引用:山东省济南市天桥区黄河双语实验学校2021-2022学年高三上学期10月月考化学试题
名校
解题方法
8 . 下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是
| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | 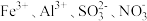 | 过量的盐酸 |  |
| B | 透明溶液中: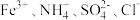 | 过量的铜粉 | 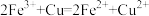 |
| C |  |  溶液 溶液 | 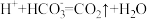 |
| D |  的溶液中: 的溶液中: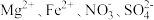 | 双氧水 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-10更新
|
204次组卷
|
14卷引用:黑龙江省哈尔滨市第六中学2020-2021学年高二下学期期末考试化学试题
黑龙江省哈尔滨市第六中学2020-2021学年高二下学期期末考试化学试题(已下线)第05讲 离子共存 离子的检验和推断(精练)-2022年高考化学一轮复习讲练测山西省太原市第五中学2021-2022学年高三上学期11月化学月考试题陕西省西安市长安区第五中学2019届高三上学期期中考试化学试题河北省衡水市衡水中学2019届高三上学期期中考试化学试题宁夏石嘴山市第三中学2020届高三上学期期中考试化学试题福建省三明第一中学2020届高三上学期第二次月考化学试题四川省宜宾市叙州区第二中学2020届高三下学期第二次高考适应性考试理综化学试题(已下线)小题必刷04 离子共存——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷06 与量有关的离子方程式书写——2021年高考化学一轮复习小题必刷(通用版)山西省运城市永济涑北中学2020-2021学年高三上学期10月月考化学试题四川省内江市第六中学2022-2023学年高三上学期入学考试化学试题 广东省梅州市兴宁市齐昌中学2022-2023学年高三上学期第二次质检考试化学试题陕西省渭南市2023-2024学年高三上学期期中检测化学试题
9 . 某溶液主要含有Na+、HCO 、SO
、SO 、NO
、NO 四种离子,向其中加入足量的Na2O2粉末后,溶液中离子浓度几乎不变的是
四种离子,向其中加入足量的Na2O2粉末后,溶液中离子浓度几乎不变的是
 、SO
、SO 、NO
、NO 四种离子,向其中加入足量的Na2O2粉末后,溶液中离子浓度几乎不变的是
四种离子,向其中加入足量的Na2O2粉末后,溶液中离子浓度几乎不变的是| A.Na+ | B.HCO | C.SO | D.NO |
您最近一年使用:0次
10 . 下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素,回答(1)(2)两小问
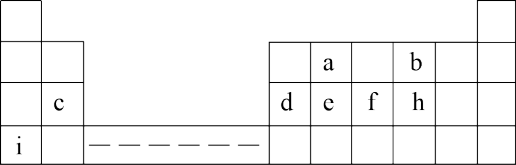
(1)a、b、c三种元素的原子半径由大到小的顺序是___________ (填元素符号);
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是_____ (填水化物的化学式)。
(3)配平下列离子方程式___ __MnO + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:___________ 。

(1)a、b、c三种元素的原子半径由大到小的顺序是
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是
(3)配平下列离子方程式
 + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:
您最近一年使用:0次



