名校
1 . 请完成下列填空。
(1)写出下列物质的电子式: :
:________ ,
_________ 。
(2)磷能形成多种具有独特性质的物质。
①磷在元素周期表中的位置_____ 。
②磷能形成红磷、白磷、黑磷等多种单质,它们互为_____ 。
③磷的一种组成为 的盐,能与盐酸反应但不能与NaOH溶液反应,下列有关
的盐,能与盐酸反应但不能与NaOH溶液反应,下列有关 、
、 的分析中正确的是
的分析中正确的是_____ (填字母)。
A. 是酸式盐 B.
是酸式盐 B. 是正盐
是正盐
C.均具有较强的还原性 D. 是三元弱酸
是三元弱酸
(3)实验室制氨气的原理_____ 。
(4)自然界中Cr主要以+3价和+6价形式存在。 中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将
中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将 还原,其离子方程式为
还原,其离子方程式为______ 。
(1)写出下列物质的电子式:
 :
:
(2)磷能形成多种具有独特性质的物质。
①磷在元素周期表中的位置
②磷能形成红磷、白磷、黑磷等多种单质,它们互为
③磷的一种组成为
 的盐,能与盐酸反应但不能与NaOH溶液反应,下列有关
的盐,能与盐酸反应但不能与NaOH溶液反应,下列有关 、
、 的分析中正确的是
的分析中正确的是A.
 是酸式盐 B.
是酸式盐 B. 是正盐
是正盐C.均具有较强的还原性 D.
 是三元弱酸
是三元弱酸(3)实验室制氨气的原理
(4)自然界中Cr主要以+3价和+6价形式存在。
 中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将
中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将 还原,其离子方程式为
还原,其离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 我国磷资源储量丰富。回答下列问题:
(1)已知亚磷酸(H3PO3)为二元弱酸,写出亚磷酸与过量 反应的化学方程式
反应的化学方程式___________ ;
(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:
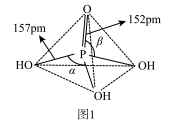
①键能大小比较:磷氧双键___________ (填“大于”“等于”或“小于”)磷氧单键。
②键角大小比较:
___________  (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是___________ 。
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示
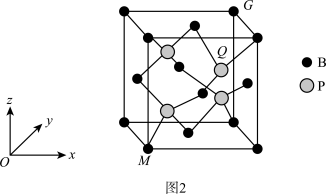
①固态磷化硼属于___________ (填“分子”“离子”或“共价”)晶体。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为___________ 。
③若晶胞参数为acm,则B与P之间的最短距离为___________ cm(用含a的代数式表示)。
(1)已知亚磷酸(H3PO3)为二元弱酸,写出亚磷酸与过量
 反应的化学方程式
反应的化学方程式(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:

①键能大小比较:磷氧双键
②键角大小比较:

 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示

①固态磷化硼属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为
③若晶胞参数为acm,则B与P之间的最短距离为
您最近一年使用:0次
名校
3 . I、高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾、次氯酸等还强。工业上制取高铁酸钠的化学方程式是(未配平):Fe(NO3)3+ NaOH + Cl2→ Na2FeO4+ NaNO3+ NaCl + H2O
(1)高铁酸钠中,铁元素的化合价是_______ ;上述制取铁酸钠的反应中,铁元素被_______ (填“还原”或“氧化”)。
(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体。用饱和氯化铁溶液制备Fe(OH)3胶体方法_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔,制造印刷电路板。
①少量的铜可以完全溶解在FeCl3溶液中,所发生反应的离子方程式为_______ 。
②除去FeCl3溶液中混有的FeCl2可加入或通入_______ 。
A、硝酸 B、稀硫酸 C、氯气 D、氢氧化钠
II、次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。回答下列问题:
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4∶1,则氧化产物为_______ (填化学式)。
②从分类来看,NaH2PO2属于_______ 。
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。配平白磷与Ba(OH)2溶液反应的化学方程式_______ 。
_______P4 +_______Ba(OH)2 + _______H2O —— _______Ba(H2PO2)2+_______PH3↑
(1)高铁酸钠中,铁元素的化合价是
(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体。用饱和氯化铁溶液制备Fe(OH)3胶体方法
(3)电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔,制造印刷电路板。
①少量的铜可以完全溶解在FeCl3溶液中,所发生反应的离子方程式为
②除去FeCl3溶液中混有的FeCl2可加入或通入
A、硝酸 B、稀硫酸 C、氯气 D、氢氧化钠
II、次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。回答下列问题:
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4∶1,则氧化产物为
②从分类来看,NaH2PO2属于
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。配平白磷与Ba(OH)2溶液反应的化学方程式
_______P4 +_______Ba(OH)2 + _______H2O —— _______Ba(H2PO2)2+_______PH3↑
您最近一年使用:0次
2022-10-31更新
|
145次组卷
|
2卷引用:湖南省邵阳市第二中学2021-2022学年高一上学期第一次月考化学试题



