名校
1 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是____ ,用电子式表示Y的最高价氧化物的形成过程:_____ 。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示)_______ 。
(3)在 与
与 的混合液中通入足量
的混合液中通入足量 ,是工业制取
,是工业制取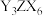 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:_______ 。
(4) 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
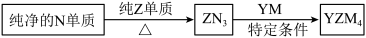
利用 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。
①其反应的化学方程式为_______ 。
②现设计如图四种装置测定 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是_______ (填编号)。
③取样品ag,若实验测得氢气的体积为 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为_______ (用代数式表示)。
(1)Y在周期表中的位置是
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示)
(3)在
 与
与 的混合液中通入足量
的混合液中通入足量 ,是工业制取
,是工业制取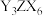 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:(4)
 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
利用
 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。①其反应的化学方程式为
②现设计如图四种装置测定
 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。
从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为
 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为
您最近一年使用:0次
2 . 药物合成在有机合成中具有重要作用。某种药物H是一种具有抗菌作用的化合物,实验室由芳香族化合物A制备的一种合成路线如下:

已知:①RCH2Br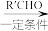 R-CH=CH-R′
R-CH=CH-R′
②2R-CH=CH-R′
 (以上R、R′代表氢或烃基等)
(以上R、R′代表氢或烃基等)
(1)A的化学名称是_______ ;C中所含官能团的名称为_______ 。
(2)试剂a是_______ ,G生成H的反应类型是_______ 。
(3)由F生成G化学方程式是_______ 。
(4)能同时满足下列条件的D的同分异构体共有_______ 种(不考虑立体异构),其中核磁共振氢谱为五组峰的有机物结构简式为_______ 。
①苯环上只有两个取代基
②除苯环外不含其他环状结构
③既能发生银镜反应又能发生水解反应且水解产物之一能与氯化铁溶液发生显色反应
(5)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成 ,写出合成路线
,写出合成路线_______ 。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)

已知:①RCH2Br
 R-CH=CH-R′
R-CH=CH-R′②2R-CH=CH-R′

 (以上R、R′代表氢或烃基等)
(以上R、R′代表氢或烃基等)(1)A的化学名称是
(2)试剂a是
(3)由F生成G化学方程式是
(4)能同时满足下列条件的D的同分异构体共有
①苯环上只有两个取代基
②除苯环外不含其他环状结构
③既能发生银镜反应又能发生水解反应且水解产物之一能与氯化铁溶液发生显色反应
(5)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成
 ,写出合成路线
,写出合成路线
您最近一年使用:0次
名校
3 . A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。请用化学用语回答下列问题:
(1)F在元素周期表中的位置为_________ 。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为______________ 。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为_________ 。写出在空气中长期放置生成H的化学反应方程式为:____________ 。H的溶液与稀硫酸反应产生的现象为_________________ 。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为______________ 。
(5)B2A4 常用做火箭推进的燃料,写出负极的电极反应:_____________ 。
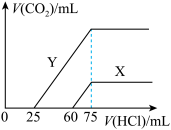
(6)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为______ ;原NaOH溶液的物质的量浓度为____ ;由曲线X、Y可知,两次实验通入的CO2的体积比为______ 。
(1)F在元素周期表中的位置为
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为
(5)B2A4 常用做火箭推进的燃料,写出负极的电极反应:
(6)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为

您最近一年使用:0次



