名校
解题方法
1 . 用下列装置制备并检验 的性质:
的性质:

下列说法错误的是
 的性质:
的性质:
下列说法错误的是
A.Ⅰ图中:若 过量,充分反应后的溶液中盐酸会有剩余 过量,充分反应后的溶液中盐酸会有剩余 |
| B.Ⅱ图中:剧烈燃烧,生成棕黄色的烟 |
| C.Ⅲ图中:经阳光照射最终水会充满试管 |
| D.Ⅳ图中:干燥的有色布条不褪色,湿润的有色布条褪色,证明氯气本身无漂白性 |
您最近一年使用:0次
2022-09-02更新
|
270次组卷
|
2卷引用:内蒙古包头市2021-2022学年高一上学期期末考试化学试题
名校
2 . 下列说法中正确的是
| A.某无色溶液中可能含有下列离子:H+、Cl-、Na+、Fe2+ |
B.能使石蕊变红的溶液中可能含有Cl-、K+、Na+、NO |
C.取少量某溶液,向其中加入BaCl2溶液,通过观察是否有白色沉淀生成,可证明该溶液中是否含有SO |
| D.H++OH-=H2O可描述所有酸碱中和反应的实质 |
您最近一年使用:0次
3 . 阅读短文,回答问题。
世界卫生组织(WHO)和中国卫健委公认二氧化氯( )为新时代绿色消毒剂,其特点是无三致(致癌、致畸、致突变),有三效(广谱、高效、快速)。国家疾病控制中心建议,为了避免传染病的传播餐饮用具可用
)为新时代绿色消毒剂,其特点是无三致(致癌、致畸、致突变),有三效(广谱、高效、快速)。国家疾病控制中心建议,为了避免传染病的传播餐饮用具可用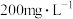 的
的 溶液浸泡游泳池水可按
溶液浸泡游泳池水可按 的
的 进行消毒。常温下,
进行消毒。常温下, 气体与
气体与 具有相似的颜色与气味,在水中的溶解度是
具有相似的颜色与气味,在水中的溶解度是 的5~8倍。
的5~8倍。 是强氧化剂,不与冷水反应,遇热水则分解成HClO、
是强氧化剂,不与冷水反应,遇热水则分解成HClO、 和
和 。研究表明,
。研究表明, 在浓度低于
在浓度低于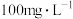 时不会对人体产生任何的影响。我国卫健委提出,逐步用
时不会对人体产生任何的影响。我国卫健委提出,逐步用 替代
替代 进行饮用水消毒。相信在不久的将来,
进行饮用水消毒。相信在不久的将来, 将广泛应用到杀菌消毒领域。
将广泛应用到杀菌消毒领域。
(1)请依据以上短文,下列说法不正确的是___________ 。
A.可以用等浓度的 溶液对餐饮用具和游泳池进行消毒
溶液对餐饮用具和游泳池进行消毒
B. 是有刺激性气味的气体
是有刺激性气味的气体
C. 杀菌力强、属于广谱高效消毒剂
杀菌力强、属于广谱高效消毒剂
D.配制 的水溶液时,应选用热水较为适宜
的水溶液时,应选用热水较为适宜
E.未来 在生产生活中更广泛的使用,是我国发展绿色消毒剂的方向。
在生产生活中更广泛的使用,是我国发展绿色消毒剂的方向。
(2)某同学推测 能与
能与 溶液反应,你认为他的推测是否合理
溶液反应,你认为他的推测是否合理___________ (填“合理”或“不合理”),用简要的文字说明理由___________ 。
(3)制备的反应原理为: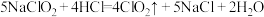 。
。
①按物质分类,上述反应中各物质未涉及的类别是___________ (填序号)。
A.酸 B.碱 C.盐 D.非金属氧化物 E.金属氧化物
②请用单线桥标出此反应的电子转移方向和数目:__________
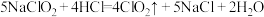
③ 的还原产物是
的还原产物是___________ ;检验反应后的溶液中含有 的常用试剂是
的常用试剂是___________ 。
④上述反应中___________ (填“能”或“不能”)用稀硫酸代替盐酸,说明理由__________
(4)请设计简易方案证明 具有永久漂白性
具有永久漂白性___________ 。
(5)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义:从HI中氧化出相同量的 所需
所需 的质量与指定含氯消毒剂的质量之比,常用百分数表示。则
的质量与指定含氯消毒剂的质量之比,常用百分数表示。则 的有效氯含量是
的有效氯含量是___________ 。
世界卫生组织(WHO)和中国卫健委公认二氧化氯(
 )为新时代绿色消毒剂,其特点是无三致(致癌、致畸、致突变),有三效(广谱、高效、快速)。国家疾病控制中心建议,为了避免传染病的传播餐饮用具可用
)为新时代绿色消毒剂,其特点是无三致(致癌、致畸、致突变),有三效(广谱、高效、快速)。国家疾病控制中心建议,为了避免传染病的传播餐饮用具可用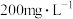 的
的 溶液浸泡游泳池水可按
溶液浸泡游泳池水可按 的
的 进行消毒。常温下,
进行消毒。常温下, 气体与
气体与 具有相似的颜色与气味,在水中的溶解度是
具有相似的颜色与气味,在水中的溶解度是 的5~8倍。
的5~8倍。 是强氧化剂,不与冷水反应,遇热水则分解成HClO、
是强氧化剂,不与冷水反应,遇热水则分解成HClO、 和
和 。研究表明,
。研究表明, 在浓度低于
在浓度低于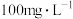 时不会对人体产生任何的影响。我国卫健委提出,逐步用
时不会对人体产生任何的影响。我国卫健委提出,逐步用 替代
替代 进行饮用水消毒。相信在不久的将来,
进行饮用水消毒。相信在不久的将来, 将广泛应用到杀菌消毒领域。
将广泛应用到杀菌消毒领域。(1)请依据以上短文,下列说法不正确的是
A.可以用等浓度的
 溶液对餐饮用具和游泳池进行消毒
溶液对餐饮用具和游泳池进行消毒B.
 是有刺激性气味的气体
是有刺激性气味的气体C.
 杀菌力强、属于广谱高效消毒剂
杀菌力强、属于广谱高效消毒剂D.配制
 的水溶液时,应选用热水较为适宜
的水溶液时,应选用热水较为适宜E.未来
 在生产生活中更广泛的使用,是我国发展绿色消毒剂的方向。
在生产生活中更广泛的使用,是我国发展绿色消毒剂的方向。(2)某同学推测
 能与
能与 溶液反应,你认为他的推测是否合理
溶液反应,你认为他的推测是否合理(3)制备的反应原理为:
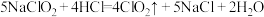 。
。①按物质分类,上述反应中各物质未涉及的类别是
A.酸 B.碱 C.盐 D.非金属氧化物 E.金属氧化物
②请用单线桥标出此反应的电子转移方向和数目:
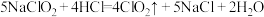
③
 的还原产物是
的还原产物是 的常用试剂是
的常用试剂是④上述反应中
(4)请设计简易方案证明
 具有永久漂白性
具有永久漂白性(5)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义:从HI中氧化出相同量的
 所需
所需 的质量与指定含氯消毒剂的质量之比,常用百分数表示。则
的质量与指定含氯消毒剂的质量之比,常用百分数表示。则 的有效氯含量是
的有效氯含量是
您最近一年使用:0次
名校
解题方法
4 . 下列有关Fe(OH)3胶体的说法正确的是( )
| A.取2 mol/L的FeCl3饱和溶液5 mL制成氢氧化铁胶体后,其中含有氢氧化铁胶粒数为0.01NA |
| B.在Fe(OH)3胶体中滴入稀硫酸至过量的过程中伴随的实验现象是先有红褐色沉淀产生,然后沉淀溶解得到棕黄色溶液 |
| C.通过电泳实验可以证明Fe(OH)3胶体带正电荷 |
| D.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,制备Fe(OH)3胶体 |
您最近一年使用:0次
2020-03-18更新
|
261次组卷
|
4卷引用:内蒙古包钢第一中学2019-2020学年高一上学期期中考试化学试题
5 . 工业合成氨反应的化学方程式为:N2(g)+3H2(g) 2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
(1)2min 内H2的反应速率v(H2)=__________________ ;
(2)充分反应并达到平衡时,放出的热量___________ 92.3kJ(填“大于”、“小于”或“等于”)。
原因是___________________________ 。
(3)下列说法可证明反应达到平衡状态的_______________ 。
(4)氨的一个重要用途是用于制备火箭发射原料N2H4(肼),已知:火箭发射的原理是N2H4(肼)在NO2中燃烧,生成N2、水蒸气。根据如下反应:
N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534.0kJ/mol
写出在相同状态下,发射火箭反应的热化学方程式______________________ 。
 2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。(1)2min 内H2的反应速率v(H2)=
(2)充分反应并达到平衡时,放出的热量
原因是
(3)下列说法可证明反应达到平衡状态的
| A.单位时间内,断开1mol N≡N,同时断开3mol H—H |
| B.单位时间内,形成1mol N≡N,同时形成3mol N—H |
| C.单位时间内,断开1mol N≡N,同时断开6mol N—H |
| D.单位时间内,形成1mol N≡N,同时断开3mol H—H |
(4)氨的一个重要用途是用于制备火箭发射原料N2H4(肼),已知:火箭发射的原理是N2H4(肼)在NO2中燃烧,生成N2、水蒸气。根据如下反应:
N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534.0kJ/mol
写出在相同状态下,发射火箭反应的热化学方程式
您最近一年使用:0次
6 . 下列有关说法正确的是
| A.常温下,向醋酸溶液中加入少量的水,溶液中c(H+) 将增大 |
B.常温下, 2NO(g)+2CO(g)  N2(g)+2CO2(g)能自发进行,则该反应的△H<0 N2(g)+2CO2(g)能自发进行,则该反应的△H<0 |
| C.硫酸铜饱和溶液降低温度时有晶体析出,可用熵判据来解释 |
| D.用CH3COOH溶液做导电实验,灯泡很暗,一定能证明CH3COOH是弱电解质 |
您最近一年使用:0次
解题方法
7 . 我国空间站“天和”核心舱太阳翼电池采用自主研发的砷化镓器件,能量转化效率大大提高。已知:砷( )与镓(
)与镓( )同位于第四周期;
)同位于第四周期; 与
与 同主族,
同主族, 与P同主族。
与P同主族。
(1)P在元素周期表中的位置是___________ ,镓的原子结构示意图为___________ 。
(2)非金属性强弱S___________ P(填“大于”或“小于”),下列表述中能证明这一事实的是___________ (填字母)。
a.S的简单氢化物的水溶液比P的简单氢化物的水溶液酸性强
b.S最高价氧化物对应的水化物的酸性强于P最高价氧化物对应的水化物的酸性
c.在反应中,P原子得电子数比S原子得电子数多
d.S的简单阴离子的还原性比P的简单阴离子的还原性弱
(3)下列关于 的推断正确的是
的推断正确的是___________ (填序号)。
① 的最高正价为+5;②原子半径:
的最高正价为+5;②原子半径: ;③元素的金属性:
;③元素的金属性:
(4) ,的酸性由强到弱的关系是
,的酸性由强到弱的关系是___________ 。
(5) 与
与 在一定条件下化合为
在一定条件下化合为 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:___________ 。
 )与镓(
)与镓( )同位于第四周期;
)同位于第四周期; 与
与 同主族,
同主族, 与P同主族。
与P同主族。(1)P在元素周期表中的位置是
(2)非金属性强弱S
a.S的简单氢化物的水溶液比P的简单氢化物的水溶液酸性强
b.S最高价氧化物对应的水化物的酸性强于P最高价氧化物对应的水化物的酸性
c.在反应中,P原子得电子数比S原子得电子数多
d.S的简单阴离子的还原性比P的简单阴离子的还原性弱
(3)下列关于
 的推断正确的是
的推断正确的是①
 的最高正价为+5;②原子半径:
的最高正价为+5;②原子半径: ;③元素的金属性:
;③元素的金属性:
(4)
 ,的酸性由强到弱的关系是
,的酸性由强到弱的关系是(5)
 与
与 在一定条件下化合为
在一定条件下化合为 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:
您最近一年使用:0次
8 . 下列实验装置中所进行的实验,能达到相应实验目的的是
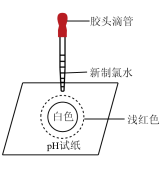 | 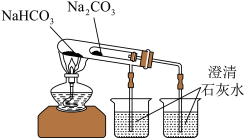 | 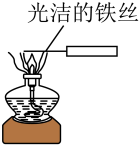 |  |
| A.该实验说明H+扩散速度比HClO分子快 | B.比较Na2CO3、NaHCO3的稳定性 | C.观察K2CO3的焰色,判断是否含有钾盐 | D.可证明氯气分子具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列实验现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向 溶液中滴入硫酸酸化的 溶液中滴入硫酸酸化的 溶液 溶液 | 溶液变为黄色 | 验证氧化性: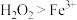 |
| B | 向某溶液中滴加 溶液 溶液 | 溶液显红色 | 原溶液中有 |
| C | 将稀盐酸滴入碳酸钠溶液中产生的气体直接通入硅酸钠溶液 | 有白色沉淀生成 | 证明非金属性 |
| D | 滴加稀 溶液,将湿润的红色石蕊试纸置于试管口 溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 实验小组制备高铁酸钾 并探究其性质。
并探究其性质。
资料: 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备 (夹持装置略)
(夹持装置略)
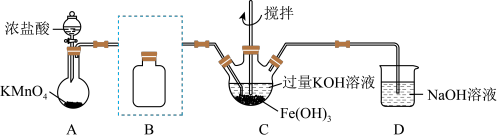
①A为氯气发生装置,写出A中反应的离子反应方程式,并用单线桥表示电子转移_______ 。
②将除杂装置B补充完整;并标明所用试剂_______ 。
③C中得到紫色固体和溶液。C中 发生的反应有
发生的反应有_______ 、_______ 。
(2)探究 的性质
的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 ,为证明是否
,为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
i.由方案I中溶液变红可知a中含有_______ 离子,但该离子的产生不能判断一定 将
将 氧化,还可能由
氧化,还可能由_______ 产生(用离子方程式表示)。
ii.方案II可证明 氧化了
氧化了 。用
。用 溶液洗涤的目的是
溶液洗涤的目的是_______ 。
根据 的制备实验得出:氧化性
的制备实验得出:氧化性
_______  (填“>””或“<”),而方案II实验表明,
(填“>””或“<”),而方案II实验表明, 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是_______ 。
 并探究其性质。
并探究其性质。资料:
 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)制备
 (夹持装置略)
(夹持装置略)
①A为氯气发生装置,写出A中反应的离子反应方程式,并用单线桥表示电子转移
②将除杂装置B补充完整;并标明所用试剂
③C中得到紫色固体和溶液。C中
 发生的反应有
发生的反应有(2)探究
 的性质
的性质取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有
 ,为证明是否
,为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:| 方案I | 取少量a,滴加 溶液至过量,溶液呈红色 溶液至过量,溶液呈红色 |
| 方案II | 用 溶液充分洗涤C中所得固体,再用 溶液充分洗涤C中所得固体,再用 溶液将 溶液将 溶出,得到紫色溶液b,取少量b,滴加盐酸,有 溶出,得到紫色溶液b,取少量b,滴加盐酸,有 产生。 产生。 |
 将
将 氧化,还可能由
氧化,还可能由ii.方案II可证明
 氧化了
氧化了 。用
。用 溶液洗涤的目的是
溶液洗涤的目的是根据
 的制备实验得出:氧化性
的制备实验得出:氧化性
 (填“>””或“<”),而方案II实验表明,
(填“>””或“<”),而方案II实验表明, 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是
您最近一年使用:0次



