1 . 化合物A中含有三种元素,3.68gA在氧气中充分煅烧后生成1.28gB、1.60gC和气体D,物质A~H存在如图转化关系。
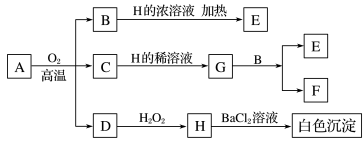
已知B是一种红色金属单质,C是金属氧化物,D是非金属氧化物,E、F、G是盐。请回答:
(1)化合物A中非金属元素在元素周期表中的位置为:___ ;
(2)检验气体D的实验方法:___ ;
(3)写出B与H的浓溶液反应的化学方程式:___ ;
(4)写出A在氧气中充分煅烧的化学方程式:___ 。

已知B是一种红色金属单质,C是金属氧化物,D是非金属氧化物,E、F、G是盐。请回答:
(1)化合物A中非金属元素在元素周期表中的位置为:
(2)检验气体D的实验方法:
(3)写出B与H的浓溶液反应的化学方程式:
(4)写出A在氧气中充分煅烧的化学方程式:
您最近一年使用:0次
2 . X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如图所示的转化关系(其他物质省略):

(1)若X是一种生活中使用量最大的金属单质
①写出Z与Cu反应的离子方程式:_____
②如何设计实验检验Z中阳离子:_____
(2)若X是一种非金属单质,常温下为固体,Y是一种能使品红溶液褪色且加热后又能恢复原来颜色的化合物。
①写出构成X单质的元素在元素周期表中的位置:_____
②写出Z与Cu反应的化学方程式_____

(1)若X是一种生活中使用量最大的金属单质
①写出Z与Cu反应的离子方程式:
②如何设计实验检验Z中阳离子:
(2)若X是一种非金属单质,常温下为固体,Y是一种能使品红溶液褪色且加热后又能恢复原来颜色的化合物。
①写出构成X单质的元素在元素周期表中的位置:
②写出Z与Cu反应的化学方程式
您最近一年使用:0次
3 . 甲、乙、丙三种物质均由短周期元素组成,一定条件下,存在下列转化关系:甲+乙→丙+H20
(1)若丙为Na2C03,反应的化学方程式为______ (任写一个)。
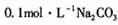 溶液中,所含的离子按物质的量浓度由大到小的顺序排列为
溶液中,所含的离子按物质的量浓度由大到小的顺序排列为______ 。
(2)若甲是石油裂解气的主要成分之一,乙为O2,且甲分子和乙分子具有相同的电子数。25℃、101 kPa时,1g甲完全燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为_________ ;利用该反应设计的燃料电池中,通入甲的电极为电池的_____ (填“正极”或“负极”)。
(3)若甲、乙是同主族元素的化合物,丙为单质。
①丙所含元素在元素周期表中的位置为_______ ;
②甲与水相比,热稳定性较强的是________ (填化学式)。
(1)若丙为Na2C03,反应的化学方程式为
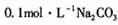 溶液中,所含的离子按物质的量浓度由大到小的顺序排列为
溶液中,所含的离子按物质的量浓度由大到小的顺序排列为(2)若甲是石油裂解气的主要成分之一,乙为O2,且甲分子和乙分子具有相同的电子数。25℃、101 kPa时,1g甲完全燃烧生成CO2气体与液态水,放出50.5 kJ的热量,该反应的热化学方程式为
(3)若甲、乙是同主族元素的化合物,丙为单质。
①丙所含元素在元素周期表中的位置为
②甲与水相比,热稳定性较强的是
您最近一年使用:0次
2016-12-09更新
|
304次组卷
|
3卷引用:2014-2015学年浙江省杭州市五校联盟高二统测模拟考化学试卷
名校
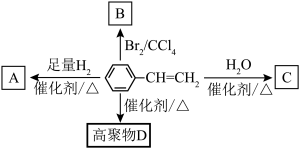
4 . 苯乙烯在一定条件下有如图转化关系,根据框图回答下列问题:___________ 。
(2)产物C的结构不止一种,其中分子中含有“-CH3”的结构简式为___________ ,该有机物在铜作催化剂和加热的条件下发生氧化反应的化学方程式为___________ 。
(3)以下是合成苯乙烯的一种路线:___________ ,反应②的化学方程式为___________ 。
(4)已知: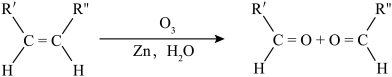 ,该反应为烯烃的臭氧化反应,
,该反应为烯烃的臭氧化反应,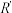 和
和 可以为任意烃基或者H原子。由此推断分子式为C4H8的烯烃发生臭氧化反应最多有
可以为任意烃基或者H原子。由此推断分子式为C4H8的烯烃发生臭氧化反应最多有___________ 种产物。
(2)产物C的结构不止一种,其中分子中含有“-CH3”的结构简式为
(3)以下是合成苯乙烯的一种路线:

(4)已知:
 ,该反应为烯烃的臭氧化反应,
,该反应为烯烃的臭氧化反应,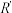 和
和 可以为任意烃基或者H原子。由此推断分子式为C4H8的烯烃发生臭氧化反应最多有
可以为任意烃基或者H原子。由此推断分子式为C4H8的烯烃发生臭氧化反应最多有
您最近一年使用:0次
解题方法
5 . 下图是部分短周期主族元素原子半径与原子序数的关系。
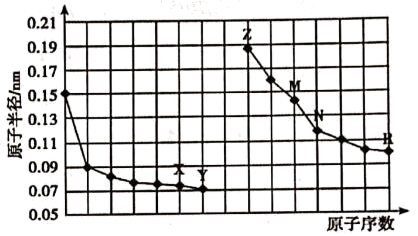
(1)X元素在元素周期表中的位置:___________ 。
(2)Y与Z形成的是___________ 化合物。(填“离子”或“共价”)
(3)上述元素中,最高价氧化物的水化物碱性最强的是___________ (填化学式)。
(4)下列关于元素及其化合物性质的判断中,正确的是___________ (填序号)
A.元素Z最外层只有1个电子,而M最外层有3个电子,所以金属性:
B.可通过Z与W的单质与水反应的剧烈程度的实验,判断金属性
C.Z、M、R三种元素的简单离子半径的大小: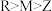
D.X、Y两种元素的气态氢化物的稳定性:
(5)某小组为证明N和R的非金属性强弱,设计实验方案如下,取N的最高价含氧酸正盐溶液,滴加含R的某溶液,通过观察实验现象来证明,其化学方程式为___________ 。

(1)X元素在元素周期表中的位置:
(2)Y与Z形成的是
(3)上述元素中,最高价氧化物的水化物碱性最强的是
(4)下列关于元素及其化合物性质的判断中,正确的是
A.元素Z最外层只有1个电子,而M最外层有3个电子,所以金属性:

B.可通过Z与W的单质与水反应的剧烈程度的实验,判断金属性

C.Z、M、R三种元素的简单离子半径的大小:
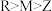
D.X、Y两种元素的气态氢化物的稳定性:

(5)某小组为证明N和R的非金属性强弱,设计实验方案如下,取N的最高价含氧酸正盐溶液,滴加含R的某溶液,通过观察实验现象来证明,其化学方程式为
您最近一年使用:0次
名校
6 . 食品防腐剂J 的合成路线如下:

请回答下列问题:
(1)A 属于芳香烃,其结构简式是_____ ,H 的结构简式是_______ 。
(2) 反应②、③中试剂 ii 和试剂 iii 依次是_______ 。(填序号)
a 高锰酸钾酸性溶液、氢氧化钠溶液 b 氢氧化钠溶液、高锰酸钾酸性溶液
(3)J 有多种同分异构体:其中符合下列条件的同分异构体有_______ 种,写出符合下列条件、且核磁共振氢谱有 6 组峰的同分异构体的结构简式:_______ 。
a 为苯的二元取代物,且遇 FeCl3溶液显紫色
b 与J 具有相同的官能团,且能发生银镜反应
(4)以 A 为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(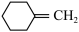 ),写出合成路线
),写出合成路线_____ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
例如:由氯乙烷制备 1,2-二溴乙烷的合成路线:CH3CH2Cl CH2CH2
CH2CH2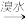 CH2BrCH2Br
CH2BrCH2Br

请回答下列问题:
(1)A 属于芳香烃,其结构简式是
(2) 反应②、③中试剂 ii 和试剂 iii 依次是
a 高锰酸钾酸性溶液、氢氧化钠溶液 b 氢氧化钠溶液、高锰酸钾酸性溶液
(3)J 有多种同分异构体:其中符合下列条件的同分异构体有
a 为苯的二元取代物,且遇 FeCl3溶液显紫色
b 与J 具有相同的官能团,且能发生银镜反应
(4)以 A 为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(
 ),写出合成路线
),写出合成路线例如:由氯乙烷制备 1,2-二溴乙烷的合成路线:CH3CH2Cl
 CH2CH2
CH2CH2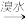 CH2BrCH2Br
CH2BrCH2Br
您最近一年使用:0次
2020-03-24更新
|
111次组卷
|
2卷引用:浙江杭州萧山区萧山中学2019-2020学年高二3月月考化学试题
名校
7 . 元素周期表短周期中六种元素的原子序数与主要化合价的关系如图:
(1)元素F在周期表中的位置是______ 。
(2)元素C、D、E原子半径由大到小的顺序是______ (填元素符号)。
(3)A、B、C的单质与氢气反应的剧烈程度由强到弱的顺序_____ (用单质的化学式表示)。
(4)应用元素周期律和元素周期表的知识,写出D和E所形成的化合物的化学式______ 、__ (写2种)。
(5)根据氯、溴、碘单质间的置换反应,判断F的单质和E的最简单氢化物之间能否发生反应_____ (填“能”或“不能”), 若能则写出反应的化学方程式 ______ 。
(6)一定温度下,在体积恒定的密闭容器中发生反应:2AB(g)+B2(g) ⇌2AB2(g)。可以作为达到平衡状态的标志是______ 。
A. 单位时间内生成nmolB2的同时生成2nmolAB B. 2 ν正(B2)=ν逆(AB2)
C. 混合气体的颜色不再改变(AB2为有色气体) D. 混合气体的密度不变

(1)元素F在周期表中的位置是
(2)元素C、D、E原子半径由大到小的顺序是
(3)A、B、C的单质与氢气反应的剧烈程度由强到弱的顺序
(4)应用元素周期律和元素周期表的知识,写出D和E所形成的化合物的化学式
(5)根据氯、溴、碘单质间的置换反应,判断F的单质和E的最简单氢化物之间能否发生反应
(6)一定温度下,在体积恒定的密闭容器中发生反应:2AB(g)+B2(g) ⇌2AB2(g)。可以作为达到平衡状态的标志是
A. 单位时间内生成nmolB2的同时生成2nmolAB B. 2 ν正(B2)=ν逆(AB2)
C. 混合气体的颜色不再改变(AB2为有色气体) D. 混合气体的密度不变
您最近一年使用:0次
2019-06-29更新
|
605次组卷
|
3卷引用:浙江省杭州市长征中学2019-2020学年高二上学期期中考试化学试题
真题
解题方法
8 . 已知A—O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。请回答下列问题:

⑴组成B单质的元素位于周期表位置________________ 。化合物C电子式为____________ 。
⑵J的熔沸点比硒化氢(H2Se)的熔沸点高,其原因是_________________ 。
⑶I与H在一定条件下也可直接反应生成L和J, 写出化学方程式:_______________ 。
⑷写出D与水反应的化学方程式:_____________________ 。
⑸红棕色污染气体M的处理具有实际意义。现在常利用反应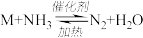 (方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是
(方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是_______ L。

⑴组成B单质的元素位于周期表位置
⑵J的熔沸点比硒化氢(H2Se)的熔沸点高,其原因是
⑶I与H在一定条件下也可直接反应生成L和J, 写出化学方程式:
⑷写出D与水反应的化学方程式:
⑸红棕色污染气体M的处理具有实际意义。现在常利用反应
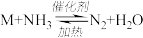 (方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是
(方程没配平)来处理M。当转移0.4mol电子时,消耗的M在标准状况下是
您最近一年使用:0次
2016-12-09更新
|
87次组卷
|
6卷引用:2010—2011学年浙江省杭州二中高一下学期期中考试化学试卷
(已下线)2010—2011学年浙江省杭州二中高一下学期期中考试化学试卷2009年普通高等学校招生统一考试理综试题化学部分(四川卷)2009年高考真题汇编-氮族元素(已下线)2012届四川省成都外国语学校高三3月月考理综部分(已下线)2011-2012学年浙江省嘉兴一中高一下学期期中考试化学试卷2020年安徽省全省教学质量检测统一考试(练习检测一)



