1 . 下列关于钠及其化合物的叙述错误的是
| A.取用金属钠时,所需用品一般有小刀、镊子、滤纸、玻璃片 |
| B.金属钠与Ca(HCO3)2溶液反应时,既有白色沉淀又有气体逸出 |
| C.质量相同的两块钠,分别与氧气完全反应生成Na2O和Na2O2,生成Na2O的钠失去的电子更多 |
| D.生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl |
您最近一年使用:0次
解题方法
2 . 印刷电路板(PCB)是用腐蚀液将覆铜板上的部分铜腐蚀掉而制得。电子工业中常用 溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:
溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:

下列说法不正确 的是
 溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:
溶液制作PCB并将腐蚀后废液回收再生,其工艺流程如图:
下列说法
A.腐蚀后的废液中,主要的金属阳离子有 、 、 、 、 |
B.过程②中发生的主要反应为: 和 和 |
C.若过程④中加入过量的试剂B为酸化的 ,则反应过程中酸性增强 ,则反应过程中酸性增强 |
D.若在10g滤渣中加入足量盐酸,放出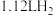 (标准状况),则滤渣中Cu的质量分数是72% (标准状况),则滤渣中Cu的质量分数是72% |
您最近一年使用:0次
3 . 病人输液用的葡萄糖注射液是葡萄糖的水溶液,已知葡萄糖的相对分子量为180,其标签上的部分内容如图所示.
根据标签所提供的信息,判断下列说法不正确的是
5%葡萄糖注射液 【性状】本品为无色或几乎无色的透明液体,味甜. 【规格】 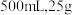 【贮藏】密闭保存. |
| A.该注射液属于一种分散系 | B.该注射液中葡萄糖的质量分数为5% |
C. 该注射液质量为 该注射液质量为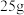 | D.该注射液中葡萄糖的物质的量浓度约为 |
您最近一年使用:0次
名校
解题方法
4 . 将10.6gNa2CO3与盐酸完全反应生成CO2气体,则至少需要质量分数为36.5%的 盐酸___________ g,生成CO2的质量是___________ g。
您最近一年使用:0次
解题方法
5 . 下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制
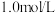 的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:
的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:
(1)配制上述稀硫酸时,还缺少的仪器有___________ (写仪器名称);
(2)配制
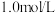 的稀硫酸需要用量筒量取上述浓硫酸的体积为
的稀硫酸需要用量筒量取上述浓硫酸的体积为___________ mL,量取硫酸时应选用以下___________ 规格的量筒(填选项)。
A. B.
B. C.
C. D.
D.
(3)根据计算结果,进行如下实验操作:
①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;
③待溶液冷却到室温,转移入容量瓶中;
④然后将蒸馏水沿玻璃棒注入容量瓶直至刻度线;
⑤把容量瓶盖盖紧,上下颠倒摇匀
你认为上述实验中错误的操作是___________ (填序号)
(4)若遇到下列情况,对配制硫酸的物质的量浓度有何影响(填“偏高”“偏低”或“不变”)
①用于稀释硫酸的烧杯未洗涤___________ ;
②容量瓶中有少量的蒸馏水___________ 。

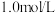 的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:
的稀硫酸。可供选用的仪器有:①玻璃棒;②烧杯;③药匙;④量筒;⑤托盘天平。请回答下列问题:| 硫酸 化学纯(CP)(  ) )品名:硫酸 化学式:  相对分子质量:98 密度:  质量分数:98%(  ) ) |
(2)配制

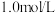 的稀硫酸需要用量筒量取上述浓硫酸的体积为
的稀硫酸需要用量筒量取上述浓硫酸的体积为A.
 B.
B. C.
C. D.
D.
(3)根据计算结果,进行如下实验操作:
①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;
③待溶液冷却到室温,转移入容量瓶中;
④然后将蒸馏水沿玻璃棒注入容量瓶直至刻度线;
⑤把容量瓶盖盖紧,上下颠倒摇匀
你认为上述实验中错误的操作是
(4)若遇到下列情况,对配制硫酸的物质的量浓度有何影响(填“偏高”“偏低”或“不变”)
①用于稀释硫酸的烧杯未洗涤
②容量瓶中有少量的蒸馏水
您最近一年使用:0次
2023-08-11更新
|
203次组卷
|
2卷引用:浙江省杭州市“六县九校”联盟2022-2023学年高一上学期期中联考化学试题
名校
解题方法
6 . 将一块质量为 表面(常温时)已被氧化的金属钠投入
表面(常温时)已被氧化的金属钠投入 水中,产生
水中,产生 气体,计算:
气体,计算:
(1)氧化钠的质量___________ g;
(2)所得溶液的质量分数___________ 。
 表面(常温时)已被氧化的金属钠投入
表面(常温时)已被氧化的金属钠投入 水中,产生
水中,产生 气体,计算:
气体,计算:(1)氧化钠的质量
(2)所得溶液的质量分数
您最近一年使用:0次
解题方法
7 . 化学与生活息息相关。根据你的认知和体验,下列说法或做法正确的
| A.绿色食品就是不使用化肥、农药,不含任何化学物质的食品 |
| B.酸雨是pH<5.6的雨水,主要是由大气中的SO2、NOx等造成的 |
| C.医用酒精使用质量分数为75%酒精溶液 |
| D.为了防止某些富脂食物因被氧化而变质,常在包装袋里放生石灰 |
您最近一年使用:0次
21-22高一上·浙江·阶段练习
8 . 染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此,科学界告诫我们:慎用染发剂,少染发为好。
(1)一个对苯二胺分子中碳氢元素质量比_____ 。
(2)在对苯二胺中,所含元素的质量分数最大的元素是_____ (填元素名称)。
(1)一个对苯二胺分子中碳氢元素质量比
(2)在对苯二胺中,所含元素的质量分数最大的元素是
您最近一年使用:0次
9 . 某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐渐加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量_______ g。
(2)反应至A点时,溶液中钠元素的质量是_______ g。

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量
(2)反应至A点时,溶液中钠元素的质量是
您最近一年使用:0次
解题方法
10 . 按下列要求填空:
(1)写出漂白粉的有效成分的化学式:_______ 。
(2)钠与水反应的离子方程式_______ 。
(3)2.8g氮气含有的分子数约为_______ 个。
(4)质量分数为36.5%的HCl溶液,密度为1.17g/cm3,求其物质的量浓度为_______ mol/L。
(5)固体NaHSO4的性质:_______ (填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电;⑦不导电
(1)写出漂白粉的有效成分的化学式:
(2)钠与水反应的离子方程式
(3)2.8g氮气含有的分子数约为
(4)质量分数为36.5%的HCl溶液,密度为1.17g/cm3,求其物质的量浓度为
(5)固体NaHSO4的性质:
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电;⑦不导电
您最近一年使用:0次



