名校
1 . 已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈-1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
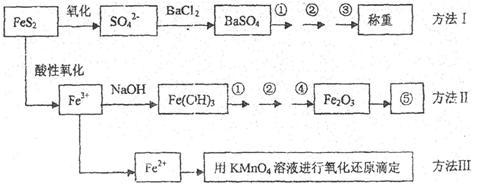
请回答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________ 、②___________ 、③________ 。
操作④、⑤用到的主要仪器是:④_________ 、⑤__________ (每空填1~2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_______________________________ 。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有_______
A.砝码生锈 B.定容时俯视
C.称量时物质和砝码位置反了(需要游码) D.容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________ 。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________ 。

请回答下列问题:
(1)流程图中操作①、②、③分别指的是:①
操作④、⑤用到的主要仪器是:④
(2)判断溶液中SO42-离子已沉淀完全的方法是
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
A.砝码生锈 B.定容时俯视
C.称量时物质和砝码位置反了(需要游码) D.容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是
您最近一年使用:0次
名校
解题方法
2 . 金属材料在人类文明的发展历程中起到重要的作用。
(1)含铜矿物孔雀石的主要成分为 ,古代人们发现孔雀石在森林大火中会变成红色的铜,该过程中含铜物质发生的主要反应的化学方程式为
,古代人们发现孔雀石在森林大火中会变成红色的铜,该过程中含铜物质发生的主要反应的化学方程式为_____________________ 。
(2)《天工开物》中记载了中国古代火法炼锌的工艺,将炉甘石(主要成分为 )和煤炭饼在高温条件下反应可制得倭铅(即锌单质),反应的化学方程式为
)和煤炭饼在高温条件下反应可制得倭铅(即锌单质),反应的化学方程式为 。该反应中的还原产物为
。该反应中的还原产物为_________ (填化学式),生成1mol锌单质时转移_________ mol电子。
(3)赤铁矿可用于高炉炼铁,其主要成分为______ (填化学名称),若赤铁矿中含有杂质 ,可以向高炉中加入适量
,可以向高炉中加入适量_________ 以除去杂质。某赤铁矿中含有其主要成分的质量分数为60%,100t该赤铁矿理论上可冶炼出纯铁的质量为_________ 。
(4)金属钛有“未来金属”之称,具有低密度、高硬度等性能。下列关于金属钛的说法错误的是________(填标号)。
(1)含铜矿物孔雀石的主要成分为
 ,古代人们发现孔雀石在森林大火中会变成红色的铜,该过程中含铜物质发生的主要反应的化学方程式为
,古代人们发现孔雀石在森林大火中会变成红色的铜,该过程中含铜物质发生的主要反应的化学方程式为(2)《天工开物》中记载了中国古代火法炼锌的工艺,将炉甘石(主要成分为
 )和煤炭饼在高温条件下反应可制得倭铅(即锌单质),反应的化学方程式为
)和煤炭饼在高温条件下反应可制得倭铅(即锌单质),反应的化学方程式为 。该反应中的还原产物为
。该反应中的还原产物为(3)赤铁矿可用于高炉炼铁,其主要成分为
 ,可以向高炉中加入适量
,可以向高炉中加入适量(4)金属钛有“未来金属”之称,具有低密度、高硬度等性能。下列关于金属钛的说法错误的是________(填标号)。
| A.工业上用钠单质高温还原二氧化钛的方法冶炼钛单质 |
| B.钛合金的熔点高于钛单质 |
| C.钛合金可作人体的植入物,制造股骨头和各种关节等 |
| D.压电陶瓷的主要成分是钛酸钡和钛酸铅 |
您最近一年使用:0次
2024-06-20更新
|
63次组卷
|
2卷引用:河北省邯郸市涉县第一中学2023-2024学年高一下学期6月月考考试 化学试题
解题方法
3 . 实验室需使用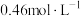 的稀硫酸480mL,现欲用质量分数为98%的浓硫酸(密度为
的稀硫酸480mL,现欲用质量分数为98%的浓硫酸(密度为 )进行配制。回答下列问题:
)进行配制。回答下列问题:_______ (填序号),配制上述溶液还需用到的玻璃仪器是_______ 和_______ (填仪器名称)。
(2)需用量筒量取98%的浓硫酸的体积为_______ mL。
(3)若配制过程中的其他操作均准确,下列操作能使所配溶液浓度偏高的有_______ 。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未冷至室温就将其转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④定容时,俯视刻度线
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
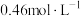 的稀硫酸480mL,现欲用质量分数为98%的浓硫酸(密度为
的稀硫酸480mL,现欲用质量分数为98%的浓硫酸(密度为 )进行配制。回答下列问题:
)进行配制。回答下列问题: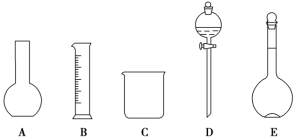
(2)需用量筒量取98%的浓硫酸的体积为
(3)若配制过程中的其他操作均准确,下列操作能使所配溶液浓度偏高的有
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未冷至室温就将其转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④定容时,俯视刻度线
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
您最近一年使用:0次
解题方法
4 . 月饼,又称月团、丰收饼、团圆饼等,是我国传统节日中秋节的节令食品和象征,在传统文化的传承和寄托上有着重要的作用。为了延长月饼的保鲜时间,市售月饼常会在包装袋内添加干燥剂和抗氧化剂,回答下列问题:

(1)月饼中添加的碳酸钾在水溶液中电离的电离方程式为___________ ,往碳酸钾溶液中滴加几滴无色酚酞,溶液变红,说明碳酸钾溶液呈___________ (填“酸”、“碱”或“中”)性。
(2)工业上常使用 作食品干燥剂,
作食品干燥剂, 的俗名为
的俗名为___________ , 与水反应的化学方程式为
与水反应的化学方程式为___________ ;社会上出现多起儿童将 型干燥剂扔进水中爆炸而造成受伤的事故,引起爆炸的原因是
型干燥剂扔进水中爆炸而造成受伤的事故,引起爆炸的原因是___________ 。
(3)铁系脱氧剂的主要成分是铁粉、二氧化硅、活性炭、水、食用盐等。铁粉与氧气接触会生成氧化铁,该反应的化学方程式为___________ 。
(4)维生素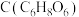 常用作食品的抗氧化剂,维生素
常用作食品的抗氧化剂,维生素 中碳元素的质量分数为
中碳元素的质量分数为___________  (保留小数点后一位),
(保留小数点后一位), 和
和 的质量比为
的质量比为___________ (用分数表示)。

(1)月饼中添加的碳酸钾在水溶液中电离的电离方程式为
(2)工业上常使用
 作食品干燥剂,
作食品干燥剂, 的俗名为
的俗名为 与水反应的化学方程式为
与水反应的化学方程式为 型干燥剂扔进水中爆炸而造成受伤的事故,引起爆炸的原因是
型干燥剂扔进水中爆炸而造成受伤的事故,引起爆炸的原因是(3)铁系脱氧剂的主要成分是铁粉、二氧化硅、活性炭、水、食用盐等。铁粉与氧气接触会生成氧化铁,该反应的化学方程式为
(4)维生素
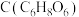 常用作食品的抗氧化剂,维生素
常用作食品的抗氧化剂,维生素 中碳元素的质量分数为
中碳元素的质量分数为 (保留小数点后一位),
(保留小数点后一位), 和
和 的质量比为
的质量比为
您最近一年使用:0次
解题方法
5 . 实验室需要0.5 mol·L-1硫酸溶液480 mL。回答下列问题:
(1)选取________ mL容量瓶,实验中需要质量分数为98%、密度为1.84 g·cm-3的浓硫酸________ mL,在量取时宜选用规格为________ (填序号)的量筒。
A.10 mL B.20 mL
C.50 mL D.100 mL
(2)如图所示的仪器中配制溶液肯定不需要的是________ (填序号),配制上述溶液还需用到的玻璃仪器是________ 、________ (填仪器名称)。
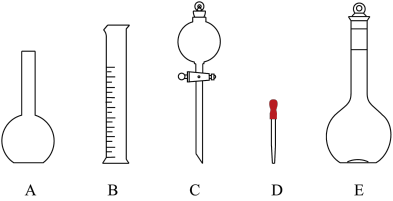
(3)在量取浓硫酸后,进行了下列操作:
①等稀释的浓硫酸的温度与室温一致后,将其沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水且边加边振荡摇匀,加蒸馏水至液面距容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的凹液面与瓶颈的刻度线相切。
③在盛有一定体积的蒸馏水的烧杯中沿杯壁注入浓硫酸,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是________ (填序号)。
(4)若实验过程中遇到下列情况,对硫酸物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未经冷却将溶液注入容量瓶中:________ ;
②定容时俯视液面:________ 。
(1)选取
A.10 mL B.20 mL
C.50 mL D.100 mL
(2)如图所示的仪器中配制溶液肯定不需要的是

(3)在量取浓硫酸后,进行了下列操作:
①等稀释的浓硫酸的温度与室温一致后,将其沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水且边加边振荡摇匀,加蒸馏水至液面距容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的凹液面与瓶颈的刻度线相切。
③在盛有一定体积的蒸馏水的烧杯中沿杯壁注入浓硫酸,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(4)若实验过程中遇到下列情况,对硫酸物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未经冷却将溶液注入容量瓶中:
②定容时俯视液面:
您最近一年使用:0次
2023-08-26更新
|
675次组卷
|
3卷引用:河北省衡水志华实验中学2023-2024学年高一上学期期中考试化学试题
解题方法
6 . 配制 溶液时,将
溶液时,将 溶于水,所得溶液的体积为
溶于水,所得溶液的体积为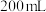 ,溶液的密度为
,溶液的密度为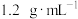 ,再将溶液稀释成
,再将溶液稀释成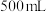 。下列说法正确的是
。下列说法正确的是
 溶液时,将
溶液时,将 溶于水,所得溶液的体积为
溶于水,所得溶液的体积为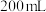 ,溶液的密度为
,溶液的密度为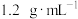 ,再将溶液稀释成
,再将溶液稀释成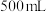 。下列说法正确的是
。下列说法正确的是A.稀释前溶液中 的物质的量浓度为 的物质的量浓度为 |
B.稀释前溶液中 的质量分数为 的质量分数为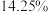 |
C.稀释后溶液中 的物质的量浓度为 的物质的量浓度为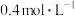 |
D.稀释后溶液中 的物质的量浓度为 的物质的量浓度为 |
您最近一年使用:0次
2023-07-14更新
|
92次组卷
|
2卷引用:河北省沧州市2022-2023学年高一上学期11月期中考试化学试题
名校
解题方法
7 . 某学校实验室从化学试剂商店买回的硫酸试剂瓶标签上的部分内容如图所示,据此下列说法正确的是
| 硫酸 化学纯(CP))(500mL) 品名:硫酸 化学式: H2SO4 相对分子质量: 98 密度: 1.84g/cm3 质量分数: 98% |
| A.常温下,1molFe与足量的该硫酸反应产生2g氢气 |
| B.进行稀释时,将水加入浓硫酸中,并用玻璃棒不断搅拌 |
| C.等质量的水与该硫酸混合所得溶液的物质的量浓度等于9.2mol·L-1 |
| D.配制200mL4.6mol·L-1的稀硫酸需取该硫酸50mL |
您最近一年使用:0次
8 . 2024年央视“3•15晚会”曝光了一些不法商家危害消费者权益的违法侵权行为,下列与化学有关的STSE热点问题的说法正确的是
A.“神乎其神的听花酒”添加的“高科技物质”凉味剂,实际是常见薄荷中的提取物薄荷脑,结构简式为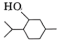 ,属于芳香族化合物 ,属于芳香族化合物 |
B.“不防火的防火玻璃”,就是普通的钢化玻璃贴个“防火玻璃”的标签,防火玻璃是在钢化玻璃中间灌注含有水玻璃的膨胀阻燃黏结剂,其中水玻璃为纯净物 |
C.“灭不了火的灭火器”,干粉灭火剂的成分为磷酸二氢铵、硫酸铵等,不法商家刻意降低磷酸二氢铵含量,降低生产成本非法牟利,其中 属于酸式盐 属于酸式盐 |
| D.“令人不安的宝马转动轴”,转动轴异响原因经技术核查发现,宝马部分车型选择钢质转动轴替代碳纤维材质转动轴,其中碳纤维材质属于有机高分子材料 |
您最近一年使用:0次
名校
9 . 高一入学体检时的血液化验单如图所示,该体检表中的物理量指的是
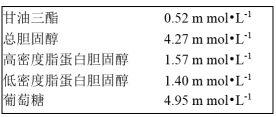

| A.溶解度 | B.物质的量浓度 | C.质量分数 | D.摩尔质量 |
您最近一年使用:0次
名校
解题方法
10 . 在一个不传热的固定容积的密闭容器中,可逆反应mA(g)+nB(g)  pC(g)+qD(g),当m、n、p、q为任意整数时,下列说法一定能说明反应已达到平衡的是
pC(g)+qD(g),当m、n、p、q为任意整数时,下列说法一定能说明反应已达到平衡的是
①体系的温度不再改变
②各组分的浓度相等
③各组分的质量分数不再改变
④反应速率v(A)∶v(B)=m∶n
⑤n·v正(A)=m·v逆(B)
⑥体系气体的平均相对分子质量不再改变
 pC(g)+qD(g),当m、n、p、q为任意整数时,下列说法一定能说明反应已达到平衡的是
pC(g)+qD(g),当m、n、p、q为任意整数时,下列说法一定能说明反应已达到平衡的是①体系的温度不再改变
②各组分的浓度相等
③各组分的质量分数不再改变
④反应速率v(A)∶v(B)=m∶n
⑤n·v正(A)=m·v逆(B)
⑥体系气体的平均相对分子质量不再改变
| A.①③⑤ | B.③⑤⑥ | C.①②⑤ | D.②⑤⑥ |
您最近一年使用:0次
2022-09-16更新
|
209次组卷
|
3卷引用:河北省邯郸市魏县第五中学2021-2022学年高二上学期期中考试化学试题



