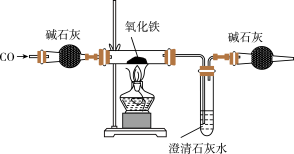
1 . 某化学小组在实验室模拟高炉炼铁,其部分装置如下:
回答下列问题:
(1)该实验在通入CO之前要对气体进行__________ 操作。
(2)判断上述装置中CO与氧化铁发生反应的现象为__________ ;发生反应的化学方程式为__________ 。
(3)该装置存在的缺陷是__________ 。
(4)已知受热不均时。可发生副反应 。为测定所得
。为测定所得 黑色产物(Fe和
黑色产物(Fe和 混合物)中铁的含量,进行如下实验。
混合物)中铁的含量,进行如下实验。
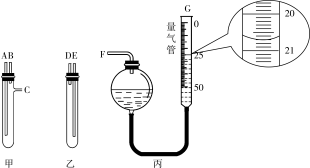
①甲、乙两试管中分别盛装样品和稀硫酸中的一种,样品应置于仪器______ (填“甲”或“乙”)中,用橡皮管连接对应接口后,倒置盛稀硫酸的试管,则A连接______ (填接口的字母)。
②当气体不再产生且恢复至室温时,正确摆放量气管后读数如丙图所示,量气管读数为______ mL。根据该读数并将产生的气体体积按标准状况计算(量气管原读数为0),产物中铁的质量分数为______ (保留一位小数)。

回答下列问题:
(1)该实验在通入CO之前要对气体进行
(2)判断上述装置中CO与氧化铁发生反应的现象为
(3)该装置存在的缺陷是
(4)已知受热不均时。可发生副反应
 。为测定所得
。为测定所得 黑色产物(Fe和
黑色产物(Fe和 混合物)中铁的含量,进行如下实验。
混合物)中铁的含量,进行如下实验。①甲、乙两试管中分别盛装样品和稀硫酸中的一种,样品应置于仪器
②当气体不再产生且恢复至室温时,正确摆放量气管后读数如丙图所示,量气管读数为

您最近一年使用:0次
2 . 防治环境污染,改善生态环境已成为全球共识。十九大报告提出“要像对待生命一样对待生态环境”。回答下列问题:
I.大气污染
(1)汽车尾气:空气中的 、
、 在高温条件下反应生成NO的化学方程式为
在高温条件下反应生成NO的化学方程式为__________ 。
(2)工业上消除氮氧化物的污染可用如下反应: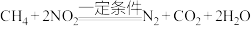 。反应中还原剂为
。反应中还原剂为__________ (填化学式);若反应中消耗 ,则转移电子的物质的量为
,则转移电子的物质的量为__________  。
。
Ⅱ.水体污染
(3)过量排放含氮元素的废水,会引起水华等水体污染问题。含有大量 的废水脱氮可以用
的废水脱氮可以用 氧化法。一定条件下,溶液pH对
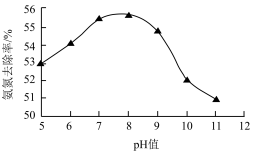
氧化法。一定条件下,溶液pH对 去除
去除 能力的影响如图所示。
能力的影响如图所示。
① 时,将
时,将 溶液氧化
溶液氧化 的离子方程式补充完整:
的离子方程式补充完整:_______ 。









②去除氨氮废水适宜的pH约为__________ 。
(4)测定废水中的氮含量:取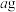 废水,将所含氮完全转化为
废水,将所含氮完全转化为 ,所得
,所得 用过量的
用过量的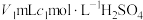 溶液吸收完全,剩余
溶液吸收完全,剩余 用
用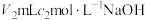 溶液恰好中和,则废水中氮元素的质量分数是
溶液恰好中和,则废水中氮元素的质量分数是__________ 。
I.大气污染
(1)汽车尾气:空气中的
 、
、 在高温条件下反应生成NO的化学方程式为
在高温条件下反应生成NO的化学方程式为(2)工业上消除氮氧化物的污染可用如下反应:
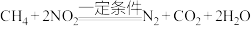 。反应中还原剂为
。反应中还原剂为 ,则转移电子的物质的量为
,则转移电子的物质的量为 。
。Ⅱ.水体污染
(3)过量排放含氮元素的废水,会引起水华等水体污染问题。含有大量
 的废水脱氮可以用
的废水脱氮可以用 氧化法。一定条件下,溶液pH对
氧化法。一定条件下,溶液pH对 去除
去除 能力的影响如图所示。
能力的影响如图所示。
①
 时,将
时,将 溶液氧化
溶液氧化 的离子方程式补充完整:
的离子方程式补充完整:








②去除氨氮废水适宜的pH约为
(4)测定废水中的氮含量:取
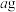 废水,将所含氮完全转化为
废水,将所含氮完全转化为 ,所得
,所得 用过量的
用过量的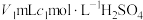 溶液吸收完全,剩余
溶液吸收完全,剩余 用
用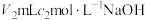 溶液恰好中和,则废水中氮元素的质量分数是
溶液恰好中和,则废水中氮元素的质量分数是
您最近一年使用:0次
解题方法
3 . 山梨酸钾是一种低毒、安全、高效的食品防腐剂,具有非常强的抑制霉菌与腐败菌的作用。一种制备方法如下:

I.制备山梨酸钾:
步骤1:在如图所示的反应装置中,加入5 g巴豆醛、10 g丙二酸和1 g吡啶,室温搅拌20分钟。
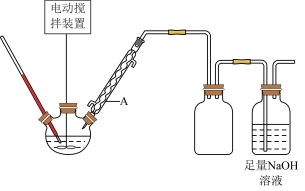
步骤2:缓慢升温至95 °C,保温95~100 °C反应3~4小时,待CO2放出后,用冰水浴降温至10°C以下,缓慢加入10%的稀硫酸,控制滴加速度使温度低于20°C,至pH约为4~5为止。
步骤3:冷冻过夜,抽滤,结晶用冰水洗涤,得山梨酸粗品。在95~100 °C水浴中,用60%乙醇溶解,抽滤,母液在-10~5°C下结晶,得山梨酸纯品。
步骤4:将山梨酸纯品、KOH、乙醇按2:1:8.6(质量比)倒入烧瓶中,并加入少量水,在60~70 °C水浴中搅拌,回流至反应液透明,迅速在冰水浴中冷却,所得晶体抽滤并烘干,即可得白色山梨酸钾晶体。
(1)仪器A的名称是_______ ;从平衡移动的角度解释“步骤1”中加入吡啶的作用_______ 。
(2)“步骤2”中的加热方式采用油浴,不采用水浴,原因是_______ ;加入稀硫酸将pH调至4~5的目的是_______ 。
(3)由山梨酸粗品制得纯品的提纯方法是_______ 。
(4)若最终制得3.0 g山梨酸钾晶体,则产率为_______ %。
II.测定食品中山梨酸钾含量(杂质不参与反应):
取待测食品m g,将其中的山梨酸钾浓缩、提取后,用盐酸酸化得白色晶体。将白色晶体用试剂X溶解后,配成250mL溶液。取25mL配好的溶液,以酚酞为指示剂,用cmol·L-1的标准NaOH溶液滴定,三次平行实验测得消耗标准液的平均体积为V mL。
(5)①溶解白色晶体的试剂X可选用_______ ;(填选项序号)
A.蒸馏水 B.乙醇 C.稀盐酸
②待测食品中山梨酸钾的质量分数为_______ %。(用含字母的代数式表示)

| 名称 | 分子式 | 分子量 | 熔点(°C) | 沸点(°C) | 性质 |
| 山梨酸钾 | C6H7O2 K | 150 | 270(分解) | — | 易溶于水和乙醇 |
| 山梨酸 | C6H8O2 | 112 | 132 | 228 | 微溶于水,易溶于有机溶剂 |
| 巴豆醛 | C4 H6O | 70 | -76.5 | 104 | 微溶于水,可溶于有机溶剂 |
| 丙二酸 | C3H4O4 | 104 | 135 | 140(分解) | 易溶于水,与有机物可混溶 |
| 吡啶 | C5H5N | 79 | -41.6 | 115.3 | 显碱性,可与山梨酸反应 |
步骤1:在如图所示的反应装置中,加入5 g巴豆醛、10 g丙二酸和1 g吡啶,室温搅拌20分钟。

步骤2:缓慢升温至95 °C,保温95~100 °C反应3~4小时,待CO2放出后,用冰水浴降温至10°C以下,缓慢加入10%的稀硫酸,控制滴加速度使温度低于20°C,至pH约为4~5为止。
步骤3:冷冻过夜,抽滤,结晶用冰水洗涤,得山梨酸粗品。在95~100 °C水浴中,用60%乙醇溶解,抽滤,母液在-10~5°C下结晶,得山梨酸纯品。
步骤4:将山梨酸纯品、KOH、乙醇按2:1:8.6(质量比)倒入烧瓶中,并加入少量水,在60~70 °C水浴中搅拌,回流至反应液透明,迅速在冰水浴中冷却,所得晶体抽滤并烘干,即可得白色山梨酸钾晶体。
(1)仪器A的名称是
(2)“步骤2”中的加热方式采用油浴,不采用水浴,原因是
(3)由山梨酸粗品制得纯品的提纯方法是
(4)若最终制得3.0 g山梨酸钾晶体,则产率为
II.测定食品中山梨酸钾含量(杂质不参与反应):
取待测食品m g,将其中的山梨酸钾浓缩、提取后,用盐酸酸化得白色晶体。将白色晶体用试剂X溶解后,配成250mL溶液。取25mL配好的溶液,以酚酞为指示剂,用cmol·L-1的标准NaOH溶液滴定,三次平行实验测得消耗标准液的平均体积为V mL。
(5)①溶解白色晶体的试剂X可选用
A.蒸馏水 B.乙醇 C.稀盐酸
②待测食品中山梨酸钾的质量分数为
您最近一年使用:0次
4 . 体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)⇌xC(g),符合图1所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图2中,Y轴是指
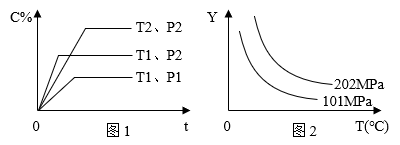

| A.反应物A的转化率 |
| B.平衡混合气中物质B的质量分数 |
| C.平衡混合气的密度 |
| D.平衡混合气中C的体积分数 |
您最近一年使用:0次
2020-11-17更新
|
154次组卷
|
2卷引用:河北省沧州市盐山中学2020-2021学年高二上学期期中考试化学试题
5 . 工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量.

(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若________________ ,说明装置不漏气.
(2)装置A的作用是____ ,装置C中的试剂为___ .
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?____ (选填“必要”或“不必要”),判断的理由是____________________ .
(4)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为_____ .

(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若
(2)装置A的作用是
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?
(4)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为
您最近一年使用:0次
6 . 过氧化氢是重要的氧化剂,也可作还原剂,它的水溶液称为双氧水,常用于消毒、杀菌、漂白等。某化学研究性学习小组取一定量的市售过氧化氢溶液测定其中H2O2的含量,并探究它的有关性质。
Ⅰ.测定市售过氧化氢溶液中H2O2的质量分数
(1)量取10.00 mL密度为ρ g/mL的市售过氧化氢溶液,应选用________ (填“酸式滴定管”或“碱式滴定管”);
(2)将上述溶液配制成250. 00 mL,配制过程需用到的玻璃仪器是烧杯、玻璃棒、________ (填名称);
(3)取25.00 mL(2)中的溶液于锥形瓶中,用稀H2SO4酸化,并加适量蒸馏水稀释,用高锰酸钾标准液滴定。
①完成反应的离子方程式:
____ MnO4-+____ H2O2+____ H+===_____ Mn2++____ H2O+____ _____
②重复滴定三次,平均消耗C mol/L KMnO4标准液V mL,则原过氧化氢溶液中H2O2的质量分数为_______ ;
Ⅱ.探究H2O2的性质
(1)上述测定原理,H2O2体现了________ 性;
(2)若要验证H2O2的不稳定性,操作是________________________________________ 。
Ⅰ.测定市售过氧化氢溶液中H2O2的质量分数
(1)量取10.00 mL密度为ρ g/mL的市售过氧化氢溶液,应选用
(2)将上述溶液配制成250. 00 mL,配制过程需用到的玻璃仪器是烧杯、玻璃棒、
(3)取25.00 mL(2)中的溶液于锥形瓶中,用稀H2SO4酸化,并加适量蒸馏水稀释,用高锰酸钾标准液滴定。
①完成反应的离子方程式:
②重复滴定三次,平均消耗C mol/L KMnO4标准液V mL,则原过氧化氢溶液中H2O2的质量分数为
Ⅱ.探究H2O2的性质
(1)上述测定原理,H2O2体现了
(2)若要验证H2O2的不稳定性,操作是
您最近一年使用:0次
9-10高二下·河北保定·期中
7 . 在测定硫酸铜晶体结晶水含量实验中,下列操作会引起晶体中结晶水的质量分数偏大的是( )
| A.加热后在空气中冷却称量 |
| B.粉末未完全变白就停止加热,进行称量计算 |
| C.加热时间过长,部分变黑 |
| D.两次称量结果相差0.2g就不再继续加热而进行计算 |
您最近一年使用:0次
解题方法
8 . 用草酸标准液滴定酸化后的 溶液的方法可测定
溶液的方法可测定 的质量分数,该过程中不需要使用到的是
的质量分数,该过程中不需要使用到的是
 溶液的方法可测定
溶液的方法可测定 的质量分数,该过程中不需要使用到的是
的质量分数,该过程中不需要使用到的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-01更新
|
42次组卷
|
2卷引用:河北省邯郸市六校联考2023-2024学年高二上学期11月月考化学试题
名校
解题方法
9 . 《黄帝九鼎神丹经诀》卷九中记载着“炼石胆取精华法”,即干馏石胆(胆矾)而获得硫酸。硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等,也广泛应用于净化石油、金属冶炼等工业中。请根据要求回答下列问题:
(1)纯净的液态硫酸______ (填“能”或“几乎不能”)导电,在硫酸不断稀释的过程中,溶液导电能力的变化情况为______ 。
(2)硫酸是强酸,具有酸的通性,如稀硫酸与氧化铁反应的化学方程式为______ ,但浓硫酸与氧化亚铁反应的化学方程式为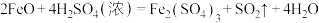 ,该反应属于
,该反应属于______ (填“氧化还原反应”或“非氧化还原反应”)。
(3)某浓硫酸的说明如图所示。该浓硫酸的物质的量浓度为______  ,从中取出100mL,则该100mL浓硫酸的物质的量浓度为
,从中取出100mL,则该100mL浓硫酸的物质的量浓度为______  ,含
,含 的物质的量为
的物质的量为______ mol。
(4)如果取5mL该浓硫酸,加水稀释至10mL,那么稀释后的硫酸的质量分数______ (填“大于”、“小于”或“等于”,下同)49%;如果取5mL该浓硫酸,加等质量的水稀释,那么稀释后的硫酸的物质的量浓度______ 原浓硫酸的物质的量浓度的一半。
(1)纯净的液态硫酸
(2)硫酸是强酸,具有酸的通性,如稀硫酸与氧化铁反应的化学方程式为
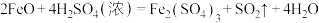 ,该反应属于
,该反应属于(3)某浓硫酸的说明如图所示。该浓硫酸的物质的量浓度为
 ,从中取出100mL,则该100mL浓硫酸的物质的量浓度为
,从中取出100mL,则该100mL浓硫酸的物质的量浓度为 ,含
,含 的物质的量为
的物质的量为| 硫酸 化学纯 CP 500mL 品名:硫酸 化学式:  相对分子质量:98 密度:1.84  质量分数:98% |
您最近一年使用:0次
名校
解题方法
10 . 邻苯二甲酸(分子式为 ,常用
,常用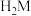 表示)是一种二元弱酸,
表示)是一种二元弱酸,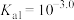 ,
,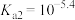 。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。
。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。
(1)用NaOH固体配制250mL 标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要
标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要___________ 。
(2)将NaOH标准溶液装入___________ (填“酸式”或“碱式”)滴定管中;滴定管在使用前,需要进行的操作是___________ 。
(3)盛放NaOH标准溶液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用___________ (填标号)中的操作。若滴定前尖嘴部分有气泡,滴定后尖嘴部分无气泡,则测得该样品中邻苯二甲酸的质量分数将___________ (填“偏高”、“偏低”或“无影响”)。
a.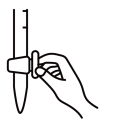 b.
b.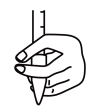 c.
c. d.
d.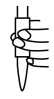
(4)称取2.50g邻苯二甲酸样品,配制成100mL溶液,取10.00mL待测液于锥形瓶中,并滴入2~3滴酚酞试液作为___________ 。
(5)有关数据记录如表:
第一次滴定前、后滴定管中液面的位置如图所示,则该次滴定所消耗NaOH标准溶液的体积为___________ mL。
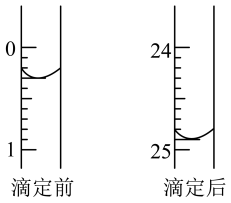
(6)到达滴定终点的现象是___________ 。
(7)根据所给数据,该邻苯二甲酸样品中邻苯二甲酸的质量分数为___________ (保留三位有效数字)。
 ,常用
,常用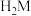 表示)是一种二元弱酸,
表示)是一种二元弱酸,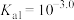 ,
,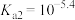 。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。
。邻苯二甲酸样品中含有少量杂质(不参与反应),某同学现用中和滴定的方法测定邻苯二甲酸样品中邻苯二甲酸的质量分数。(1)用NaOH固体配制250mL
 标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要
标准溶液,必须使用的仪器除天平、烧杯、玻璃棒、量筒外,还需要(2)将NaOH标准溶液装入
(3)盛放NaOH标准溶液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用
a.
 b.
b. c.
c. d.
d.
(4)称取2.50g邻苯二甲酸样品,配制成100mL溶液,取10.00mL待测液于锥形瓶中,并滴入2~3滴酚酞试液作为
(5)有关数据记录如表:
| 滴定序号 | 待测样品溶液体积/mL | NaOH标准溶液 | ||
| 滴定前的刻度/mL | 滴定后的刻度/mL | 消耗的体积/mL | ||
| 1 | 10.00 | |||
| 2 | 10.00 | 0.10 | 24.74 | 24.64 |
| 3 | 10.00 | 1.23 | 25.85 | 24.62 |

(6)到达滴定终点的现象是
(7)根据所给数据,该邻苯二甲酸样品中邻苯二甲酸的质量分数为
您最近一年使用:0次
2023-10-05更新
|
113次组卷
|
2卷引用:河北省邢台市四校质检联盟2023-2024学年高二上学期第一次月考化学试题







