名校
解题方法
1 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。某实验小组模拟工业制备硫氰化钾的方法,设计实验如图:
I.制备NH4SCN溶液
(1)装置A用于制备NH3,圆底烧瓶内的固体a是_______ (填名称)。
(2)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应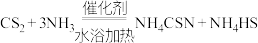 。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是
。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是_______ 。
(3)一段时间后,当观察到三颈烧瓶内_______ 时,停止通入气体,反应完成。
II.制备KSCN溶液
(4)关闭K1,将三颈烧瓶继续加热至100℃,待NH4HS完全分解后,再打开K3,继续保持水浴温度为100℃,缓缓滴入稍过量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为_______ ;酸性K2Cr2O7溶液除可以吸收NH3外,还能将H2S气体氧化成硫酸,其离子方程式为_______ 。
III.制备KSCN晶体
(5)先除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有_______ (填序号)。
①坩埚②蒸发皿③分液漏斗④玻璃棒⑤烧杯
(6)测定晶体中KSCN的含量:称取5.0g样品,配成500mL溶液。量取25.00mL溶液加入锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点,三次滴定平均消耗AgNO3标准溶液21.00mL。
①滴定时发生的反应: ,则指示剂的化学式为
,则指示剂的化学式为_______ (填序号)。
A. B.
B.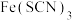 C.
C. D.
D.
②晶体中KSCN的质量分数为_______ (计算结果保留三位有效数字)。

I.制备NH4SCN溶液
(1)装置A用于制备NH3,圆底烧瓶内的固体a是
(2)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应
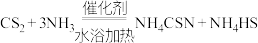 。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是
。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是(3)一段时间后,当观察到三颈烧瓶内
II.制备KSCN溶液
(4)关闭K1,将三颈烧瓶继续加热至100℃,待NH4HS完全分解后,再打开K3,继续保持水浴温度为100℃,缓缓滴入稍过量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为
III.制备KSCN晶体
(5)先除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有
①坩埚②蒸发皿③分液漏斗④玻璃棒⑤烧杯
(6)测定晶体中KSCN的含量:称取5.0g样品,配成500mL溶液。量取25.00mL溶液加入锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点,三次滴定平均消耗AgNO3标准溶液21.00mL。
①滴定时发生的反应:
 ,则指示剂的化学式为
,则指示剂的化学式为A.
 B.
B.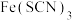 C.
C. D.
D.
②晶体中KSCN的质量分数为
您最近一年使用:0次
2024-02-29更新
|
90次组卷
|
2卷引用:四川省巴中中学2023-2024学年高二下学期3月月考化学试题
名校
2 . 劳动实践课上同学们用草木灰给农作物施肥。课后同学查阅资料,得知草木灰是一种重要的农家肥,碳酸钾含量高。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1.常见草木灰钾含量(以碳酸钾表示)如下表:
2.提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
(1)表格中钾含量最高的草木灰是_______ ,同学们选用这种秸秆灰提取碳酸钾。
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
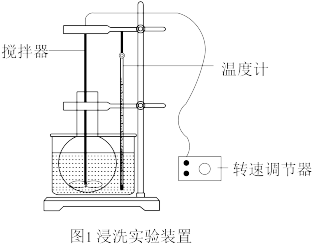
(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是_______ 。
(3)根据图2,搅拌器转速控制在每分钟_______ 转,浸取时间为_______ 分钟,比较适宜。
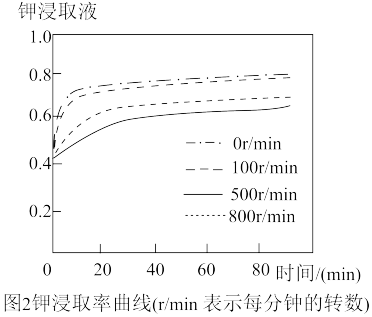
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。
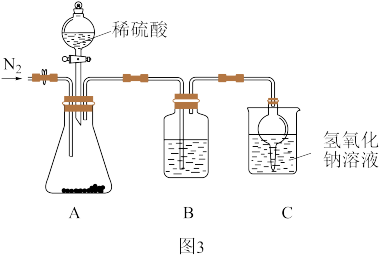
(4)实验中需缓慢滴入稀硫酸,原因是_______ 。
(5)装置B的作用是_______ 。
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为_______ %,与表格中数据相比明显偏低,原因可能是_______ (填序号)。
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有_______ (写一条)。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1.常见草木灰钾含量(以碳酸钾表示)如下表:
| 草木灰种类 | 小灌木灰 | 稻草灰 | 小麦秆灰 | 棉壳灰 | 棉秆灰 | 向日葵杆灰 |
 (%) (%) | 8.66 | 2.63 | 20.26 | 32.28 | 16.44 | 51.97 |
(1)表格中钾含量最高的草木灰是
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。

(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是
(3)根据图2,搅拌器转速控制在每分钟

实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。

(4)实验中需缓慢滴入稀硫酸,原因是
(5)装置B的作用是
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有
您最近一年使用:0次
名校
解题方法
3 . 乳酸亚铁晶体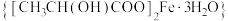 是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由
是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由 与乳酸(结构简式为:
与乳酸(结构简式为: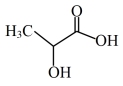 )反应制得。
)反应制得。
Ⅰ.制备

实验步骤如下:
ⅰ.检查气密性,按图示添加药品;
ⅱ.在装置B中制取硫酸亚铁,并将整个装置内的空气排净;
ⅲ.将B中溶液导入C中产生 沉淀;
沉淀;
ⅳ.将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)装置D的作用是_______ 。
(2)装置C中生成 的离子方程式是
的离子方程式是_______ 。
(3)步骤ⅱ和步骤ⅲ中应打开的开关分别是_______ (选填“ 和
和 ”或“
”或“ 和
和 ”)
”)
Ⅱ.制备乳酸亚铁晶体
将制得的 加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
(4)加入乙醇的目的是_______ 。
Ⅲ.探究乳酸亚铁晶体中铁元素的含量
乙同学称取g样品溶于水,用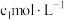 的酸性
的酸性 标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。
标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。
(5)乙同学方案是否正确?_______ (选填“是”或“否”),如填“是”,计算铁元素的质量分数(用含有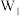 、
、 、
、 的代数式表示);如填“否”,说明偏高还是偏低,并写出理由
的代数式表示);如填“否”,说明偏高还是偏低,并写出理由_______ 。
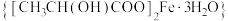 是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由
是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由 与乳酸(结构简式为:
与乳酸(结构简式为: )反应制得。
)反应制得。Ⅰ.制备


实验步骤如下:
ⅰ.检查气密性,按图示添加药品;
ⅱ.在装置B中制取硫酸亚铁,并将整个装置内的空气排净;
ⅲ.将B中溶液导入C中产生
 沉淀;
沉淀;ⅳ.将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)装置D的作用是
(2)装置C中生成
 的离子方程式是
的离子方程式是(3)步骤ⅱ和步骤ⅲ中应打开的开关分别是
 和
和 ”或“
”或“ 和
和 ”)
”) Ⅱ.制备乳酸亚铁晶体
将制得的
 加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。(4)加入乙醇的目的是
Ⅲ.探究乳酸亚铁晶体中铁元素的含量
乙同学称取g样品溶于水,用
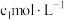 的酸性
的酸性 标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。
标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。(5)乙同学方案是否正确?
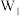 、
、 、
、 的代数式表示);如填“否”,说明偏高还是偏低,并写出理由
的代数式表示);如填“否”,说明偏高还是偏低,并写出理由
您最近一年使用:0次
2022-09-11更新
|
366次组卷
|
5卷引用:四川省绵阳南山中学2023-2024学年高三上学期第一次演练理科综合化学试题
解题方法
4 . 神舟十四号载人飞船于6月5日顺利发射升空,陈冬等三名航天员进入天和核心舱,中国空间站将于今年底建成。从化学角度回答下列问题:
(1)发射天和核心舱的运载火箭使用了煤油—液氧推进剂,煤油是通过石油_______ 得到的。另外,通过石油裂解可以得到的化工基本原料有_______ (填标号)。
A.汽油 B. 甲烷 C. 乙烯 D. 苯
(2)空间站利用太阳能电池电解水得到H2和O2实现贮能。该过程将太阳能最终转化为_______ 能,碱性氢氧燃料电池供电时,H2进入电池的_______ 极,正极的电极反应式为_______ 。
(3)空间站建造使用了铝合金。
①工业上铝的冶炼原理用化学方程式表示为_______ 。
②某铝合金样品中含有元素镁、铜、硅,用以下步骤测定该合金中铝的含量。
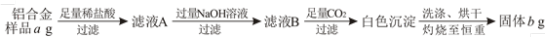
滤液B中含铝元素的离子是_______ ,用含a、b的式子表示样品中铝的质量分数为_______ 。
(1)发射天和核心舱的运载火箭使用了煤油—液氧推进剂,煤油是通过石油
A.汽油 B. 甲烷 C. 乙烯 D. 苯
(2)空间站利用太阳能电池电解水得到H2和O2实现贮能。该过程将太阳能最终转化为
(3)空间站建造使用了铝合金。
①工业上铝的冶炼原理用化学方程式表示为
②某铝合金样品中含有元素镁、铜、硅,用以下步骤测定该合金中铝的含量。
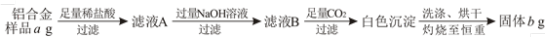
滤液B中含铝元素的离子是
您最近一年使用:0次
名校
解题方法
5 . 某铝合金中含有元素铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是_______ 。
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为_______ ,溶解、过滤用到的玻璃仪器是_______ 。
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 、_______ 。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 。
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是_______ 。原样品中铝的质量分数是_______ 。
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是
您最近一年使用:0次
6 . 水合肼(N2H4∙H2O)又名水合联氨,无色透明,是具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaClO=N2H4∙H2O+Na2CO3+NaCl。
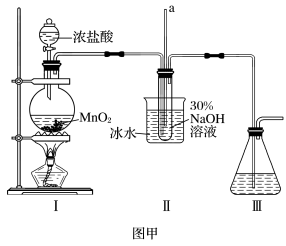
实验1:制备NaClO溶液。(已知:3NaClO 2NaCl+NaClO3)
2NaCl+NaClO3)
(1)图甲装置Ⅰ中烧瓶内发生反应的离子方程式为_____________________ 。
(2)用NaOH固体配制溶质质量分数 为30%的NaOH溶液时,所需玻璃仪器除量筒外还有______ (填字母,下同)。
a.烧杯 b.容量瓶 c.玻璃棒 d.胶头滴管
(3)图甲装置Ⅱ中用冰水浴控制温度的目的是_____ 。
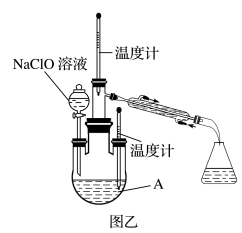
实验2:制取水合肼。
(4)图乙中若分液漏斗滴液速度过快,部分N2H4∙H2O会被氧化并产生大量氮气,降低产品产率。写出该过程反应生成氮气的化学方程式为____________________ ,该过程中产生标准状况下11.2L氮气转移电子的物质的量为_______ mol,充分反应后,蒸馏A中溶液即可得到水合肼的粗产品。
实验3:测定馏分中水合肼的含量。
(5)称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.15mol∙L-1的碘的标准溶液滴定(已知:N2H4∙H2O+2I2=N2↑+4HI+H2O)。
①滴定时,碘的标准溶液盛放在_____ (填“酸式”或“碱式”)滴定管中。判断滴定达到终点时的现象为_______________ 。
②下列能导致馏分中水合肼的含量测定结果偏高的是___________ 。
a.锥形瓶清洗干净后未干燥
b.滴定前滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后仰视
d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4∙H2O)的质量分数为___________ 。


实验1:制备NaClO溶液。(已知:3NaClO
 2NaCl+NaClO3)
2NaCl+NaClO3)(1)图甲装置Ⅰ中烧瓶内发生反应的离子方程式为
(2)用NaOH固体配制
a.烧杯 b.容量瓶 c.玻璃棒 d.胶头滴管
(3)图甲装置Ⅱ中用冰水浴控制温度的目的是
实验2:制取水合肼。
(4)图乙中若分液漏斗滴液速度过快,部分N2H4∙H2O会被氧化并产生大量氮气,降低产品产率。写出该过程反应生成氮气的化学方程式为
实验3:测定馏分中水合肼的含量。
(5)称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.15mol∙L-1的碘的标准溶液滴定(已知:N2H4∙H2O+2I2=N2↑+4HI+H2O)。
①滴定时,碘的标准溶液盛放在
②下列能导致馏分中水合肼的含量测定结果偏高的是
a.锥形瓶清洗干净后未干燥
b.滴定前滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后仰视
d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4∙H2O)的质量分数为
您最近一年使用:0次
名校
解题方法
7 . 聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3- )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。
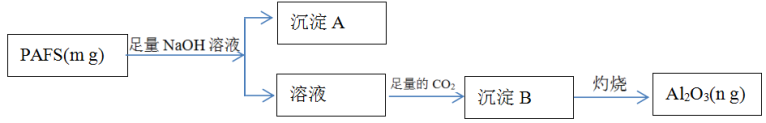
回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__ 。
(2)PAFS中铁元素的化合价为_______ ;沉淀A的化学式为_________ 。
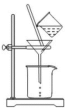
(3)如图所示,过滤操作中的一处错误是__________ 。
(4)生成沉淀B的离子方程式为______ 。
(5)PAFS中Al元素的质量分数为_______ (用同m、n的代数式表示)。
 )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。
回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为
(2)PAFS中铁元素的化合价为
(3)如图所示,过滤操作中的一处错误是

(4)生成沉淀B的离子方程式为
(5)PAFS中Al元素的质量分数为
您最近一年使用:0次
2020-06-04更新
|
165次组卷
|
2卷引用:四川省宜宾市第四中学校2022-2023学年高一上学期第三次月考试化学试题
名校
8 . 黄铜矿是一种铜铁硫化物,化学式为CuFeS2,它是工业上炼铜的主要原料。某化学小组对其中的硫、铁、铜的含量进行测定。
Ⅰ.硫的含量测定。
(1)采用装置A,在高温下将10.0g矿样中的硫转化为SO2。
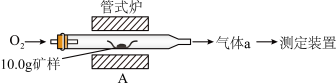
若在装置A反应中,氧化剂与还原剂的物质的量之比为19:6,灼烧后A中留下黑色固体,则反应的化学方程式为__________ 。
(2)将气体a通入测硫装置中(如图),然后采用沉淀法测定硫的含量。
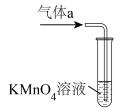
①KMnO4溶液氧化SO2的离子方程式为________________ 。
②向反应后的溶液中加入过量的BaCl2溶液,过滤,洗涤沉淀并干燥,称重为23.3g,则该矿样中硫的质量分数为__________ 。
Ⅱ.铁、铜的含量测定。
向A中灼烧后的固体中加入稀硫酸,加热溶解,过滤,将滤液分为两等份。
(3)取其中一份加入过量的氨水生成沉淀{已知Cu(OH)2能溶于氨水生成[Cu(NH3)4]2+},过滤、洗涤、灼烧、称重为1.5 g。实验过程中,加入过量的氨水得到的沉淀是___________ (填化学式);灼烧时除用到三脚架、酒精灯和玻璃棒外,还要用到________________ 。
(4)①将另一份溶液调至弱酸性,先加入NH4F,使Fe3+生成稳定的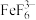 ,其目的是
,其目的是_____
②加入过量KI溶液,使Cu2+生成CuI沉淀,同时析出定量的I2。
③再用1.00 mol•L-1 Na2S2O3标准溶液滴定生成的I2,以___________ 作指示剂。若消耗的Na2S2O3标准溶液为25.00 mL,则矿样中铜的质量分数是_________ (已知I2 +2 Na2S2O3= Na2S4O6+2NaI)。
Ⅰ.硫的含量测定。
(1)采用装置A,在高温下将10.0g矿样中的硫转化为SO2。

若在装置A反应中,氧化剂与还原剂的物质的量之比为19:6,灼烧后A中留下黑色固体,则反应的化学方程式为
(2)将气体a通入测硫装置中(如图),然后采用沉淀法测定硫的含量。

①KMnO4溶液氧化SO2的离子方程式为
②向反应后的溶液中加入过量的BaCl2溶液,过滤,洗涤沉淀并干燥,称重为23.3g,则该矿样中硫的质量分数为
Ⅱ.铁、铜的含量测定。
向A中灼烧后的固体中加入稀硫酸,加热溶解,过滤,将滤液分为两等份。
(3)取其中一份加入过量的氨水生成沉淀{已知Cu(OH)2能溶于氨水生成[Cu(NH3)4]2+},过滤、洗涤、灼烧、称重为1.5 g。实验过程中,加入过量的氨水得到的沉淀是
(4)①将另一份溶液调至弱酸性,先加入NH4F,使Fe3+生成稳定的
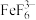 ,其目的是
,其目的是②加入过量KI溶液,使Cu2+生成CuI沉淀,同时析出定量的I2。
③再用1.00 mol•L-1 Na2S2O3标准溶液滴定生成的I2,以
您最近一年使用:0次
9 . 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
甲组:沉淀分析法:用托盘天平称取w克混合物溶解于蒸馏水后,加入过量CaCl2,然后将所得沉淀过滤、洗涤、干燥、称量得m克,写出该反应的离子方程式________________________ 。其混合物中Na2CO3的质量分数为(写出表达式):___________ 。
乙组:气体分析法:把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是_______ 。
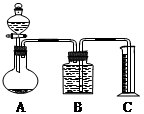
A.氢氧化钠溶液 B.饱和碳酸钠溶液 C.饱和碳酸氢钠溶液
选用该溶液后实验结果还是不准确,原因是_____________________________________
甲组:沉淀分析法:用托盘天平称取w克混合物溶解于蒸馏水后,加入过量CaCl2,然后将所得沉淀过滤、洗涤、干燥、称量得m克,写出该反应的离子方程式
乙组:气体分析法:把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是

A.氢氧化钠溶液 B.饱和碳酸钠溶液 C.饱和碳酸氢钠溶液
选用该溶液后实验结果还是不准确,原因是
您最近一年使用:0次
名校
解题方法
10 . 请按要求书写下列方程式。
(1)实验室常用热的氢氧化钠溶液洗去试管内壁附着的硫磺,其原理为___________ (用化学方程式表示)。
(2)实验室中可利用 粉末与质量分数为70%的硫酸反应制取少量
粉末与质量分数为70%的硫酸反应制取少量 反应的化学方程式为
反应的化学方程式为___________ 。
(3)写出氨气实验室制法的化学方程式___________ 。
(4)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:___________ 。
(5)铜与稀硝酸的离子方程式为:___________ 。
(1)实验室常用热的氢氧化钠溶液洗去试管内壁附着的硫磺,其原理为
(2)实验室中可利用
 粉末与质量分数为70%的硫酸反应制取少量
粉末与质量分数为70%的硫酸反应制取少量 反应的化学方程式为
反应的化学方程式为(3)写出氨气实验室制法的化学方程式
(4)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:
(5)铜与稀硝酸的离子方程式为:
您最近一年使用:0次



