1 . 下列实验方案中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 比较CH3COOH和HClO的酸性 | 用pH试纸测定同浓度的两溶液的pH值 |
| B | 检验Fe(NO3)2晶体是否变质 | 将样品溶于稀硫酸,滴入几滴KSCN溶液 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入过量饱和Na2CO3溶液洗涤后分液 |
| D | 除去乙烯中少量的二氧化硫 | 将混合气体通过足量酸性KMnO4溶液洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列说法或推理正确的是
| A.将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,溶液变红,则Fe(NO3)2晶体已氧化变质 |
| B.常温下,pH都为11的氢氧化钠溶液和氨水均加水稀释100倍,pH都变为9 |
| C.25℃时,Ksp(BaCO3)>Ksp(BaCrO4),则沉淀水体中的Ba2+选择Na2CrO4比Na2CO3好 |
| D.将CH3CH2Br与NaOH溶液共热,冷却后取出上层溶液,加入AgNO3溶液,产生沉淀,则CH3CH2Br在NaOH溶液中发生了水解 |
您最近一年使用:0次
2016-09-01更新
|
196次组卷
|
5卷引用:2016届四川省广元市高三下第二次高考适应性统考化学试卷
解题方法
3 . A~F六种物质的转化关系如图所示(部分反应物、产物和反应条件未写出),其中A为单质,B常用来作为潜水艇和呼吸面具中氧气来源,物质A到F的焰色试验均呈黄色。回答下列问题:
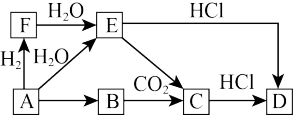
(1)该转化过程中A→B可以在热坩埚中进行,其现象为_______ ,化学反应方程式为_______ 。
(2)写出A→E的化学方程式并用单线桥标出电子转移的方向和数目_______ 。
(3)C的化学式为_______ ,向C的饱和溶液中通入足量 ,可观察到的现象是
,可观察到的现象是_______ 。
(4)F→E的化学方程式为_______ ,其中氧化剂是_______ (填化学式)。
(5)下列关于焰色试验说法错误的是_______(填标号)

(1)该转化过程中A→B可以在热坩埚中进行,其现象为
(2)写出A→E的化学方程式并用单线桥标出电子转移的方向和数目
(3)C的化学式为
 ,可观察到的现象是
,可观察到的现象是(4)F→E的化学方程式为
(5)下列关于焰色试验说法错误的是_______(填标号)
| A.焰色试验时可以用洁净的铜丝来代替铂丝进行实验 |
| B.某样品做焰色试验时,直接观察到火焰呈黄色,可以确定该样品中不含钾元素 |
| C.节日燃放的五彩缤纷的烟花,就是锂、钠、钾、锶、钡等金属化合物所呈现的各种艳丽的色彩 |
| D.焰色试验是元素的一种物理性质,属于物理变化 |
您最近一年使用:0次
2022-11-03更新
|
346次组卷
|
3卷引用:四川省成都市四县区(金堂、大邑、蒲江、新津)2022-2023学年高一上学期期中联考化学试题
4 . 亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,请回答:
[实验Ⅰ]NaClO2晶体按如下图装置进行制取。
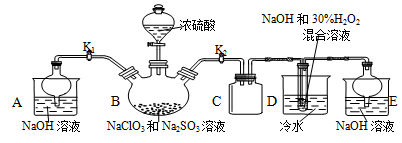
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,
高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C起的是______ 的作用。
(2)已知装置B中的产物有ClO2气体,装置D中生成NaClO2和一种助燃气体,其反应的化学方程式为__________________ 。
(3)从装置D反应后的溶液中获得NaClO2晶体的操作步骤为:①减压在55℃蒸发结晶;
②___________ ;③用38℃~60℃热水洗涤;④低于___ ℃干燥;得到成品。.
(4)反应结束后,打开K1,装置A起的作用是______ ;如果撤去D中的冷水浴,可能导致产品中混有的杂质是_________ 。
[实验Ⅱ]样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度:准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32﹣=2I﹣+S4O62﹣),则所称取的样品中NaClO2的物质的量为________________ 。
[实验Ⅰ]NaClO2晶体按如下图装置进行制取。

已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,
高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C起的是
(2)已知装置B中的产物有ClO2气体,装置D中生成NaClO2和一种助燃气体,其反应的化学方程式为
(3)从装置D反应后的溶液中获得NaClO2晶体的操作步骤为:①减压在55℃蒸发结晶;
②
(4)反应结束后,打开K1,装置A起的作用是
[实验Ⅱ]样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度:准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32﹣=2I﹣+S4O62﹣),则所称取的样品中NaClO2的物质的量为
您最近一年使用:0次



