16. 物质的量浓度是一种常用的溶液浓度表示方法,利用其进行定量分析计算比较方便。
Ⅰ.实验需要0.8

NaOH溶液475mL和0.4

硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
(1)若用质量分数为98%、密度为1.84g/mL的浓硫酸来配制0.4

硫酸溶液,需用量筒量取体积为
_______mL的浓硫酸来稀释。
(2)为配制上述稀硫酸,除了量筒、烧杯、玻璃棒外,还缺少的玻璃仪器是
_______、
_______。
(3)在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是
_______(填序号)。
A.定容时俯视观察
B.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
C.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
D.容量瓶未干燥即用来配制溶液
E.往容量瓶转移时,有少量液体溅出
F.未洗涤稀释浓硫酸的烧杯
(4)欲用NaOH固体配制0.8

NaOH 475mL。下列说法正确的是_______(填字母)。
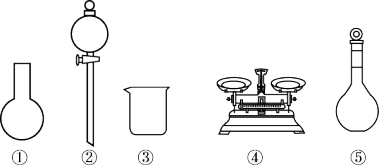
| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶使用前应检漏 |
| C.需要称量NaOH固体的质量为15.2g |
| D.称量NaOH固体时将NaOH放在纸上称 |
Ⅱ.在0.2L由NaCl、

、组成的混合液中,都分离子浓度大小如下图所示(不考虑溶液中

和

浓度)。请回答下列问题:

(5)该混合液中

的物质的量为
_______mol。