1 . 为测定某过氧化钠样品的纯度,将2g该样品与足量水发生反应(杂质不参与反应):2Na2O2+2H2O=4NaOH+O2↑,生成气体质量与时间的关系如图所示。
(1)生成氧气的质量是___________ g。
(2)列式计算该样品中过氧化钠的质量分数为___________ 。
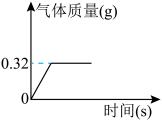
(1)生成氧气的质量是
(2)列式计算该样品中过氧化钠的质量分数为
您最近一年使用:0次
2 . 氢化钙(CaH2)是种白色细颗粒状固体,能与水发生剧烈反应,其反应的化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑,常用作登山运动员的能源提供剂。
(1)某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是___________ (填写化学式)。
为进步确定滤液中所含溶质的成分,他们进行了以下实验探究。
【提出猜想】
(2)猜想一:NaOH;
猜想二:NaOH和Na2CO3;
猜想三:___________ ;
猜想四:NaOH、Na2CO3、Ca(OH)2。
经过分析,大家一致认为上述猜想___________ 不需要验证,肯定是错误的,原因是___________ (用化学方程式表示)。
【实验探究】
(3)方案一:取一定量的滤液于试管中,往其中滴加少量稀盐酸,无明显实验现象。
方案二:取一定量的滤液于另一试管中,往其中滴加氯化钡溶液,观察到___________ 。
【讨论交流】
(4)根据实验现象,得出猜想___________ 是正确的。请解释方案一中无明显现象的原因是___________ 。
【拓展探究】
(5)上述小组同学将5g氢化钙样品(所含杂质不参与反应也不溶于水)加入到50g碳酸钠溶液中,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
①样品中CaH2的质量分数为___________ 。
②原碳酸钠溶液中溶质的质量为___________ 。
③反应后溶液中溶质的质量分数为___________ 。(计算结果保留一位小数)
(1)某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是
为进步确定滤液中所含溶质的成分,他们进行了以下实验探究。
【提出猜想】
(2)猜想一:NaOH;
猜想二:NaOH和Na2CO3;
猜想三:
猜想四:NaOH、Na2CO3、Ca(OH)2。
经过分析,大家一致认为上述猜想
【实验探究】
(3)方案一:取一定量的滤液于试管中,往其中滴加少量稀盐酸,无明显实验现象。
方案二:取一定量的滤液于另一试管中,往其中滴加氯化钡溶液,观察到
【讨论交流】
(4)根据实验现象,得出猜想
【拓展探究】
(5)上述小组同学将5g氢化钙样品(所含杂质不参与反应也不溶于水)加入到50g碳酸钠溶液中,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
①样品中CaH2的质量分数为
②原碳酸钠溶液中溶质的质量为
③反应后溶液中溶质的质量分数为
您最近一年使用:0次
3 . 根据如图实验装置,请回答:___________ 。
(2)检查装置A气密性的方法是夹紧止水夹,___________ ,则气密性良好。
(3)用H2O2制取氧气,选择的发生装置为___________ (填字母),反应的化学方程式为___________ 。
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为___________ ,在F中气体应从导管___________ (填“b”或“c”)端通入。
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为___________ (填字母)。用装置E收集甲烷,利用了甲烷___________ 的物理性质;用装置C而不用装置D收集甲烷,原因是___________ 。
②设计实验证明CH4中含有氢元素:检验其纯度后,___________ 。

(2)检查装置A气密性的方法是夹紧止水夹,
(3)用H2O2制取氧气,选择的发生装置为
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为
②设计实验证明CH4中含有氢元素:检验其纯度后,
您最近一年使用:0次
4 . 利用物质的性质能帮助我们开展科学探究。
(1)判断化学变化。如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是___________ 。
实验结论:稀盐酸和氢氧化钠溶液反应的化学方程式为___________ 。
(1)判断化学变化。如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是

| 编号 | 实验操作 | 实验现象 | 实验分析 |
| 实验一 | 取一定量稀盐酸于小烧杯中,加入氢氧化钠溶液 | 无明显现象 | 稀盐酸与氢氧化钠溶液混合后有新物质生成 |
| 实验二 | 取实验一所得溶液少量于试管中,滴入几滴无色酚酞溶液 | 无明显现象 | |
| 实验三 | 取实验一所得溶液少量, |
您最近一年使用:0次
5 . 含碳物质种类繁多。请回答下列问题:
(1)葡萄糖(C6H12O6)中C、H、O原子的数目之比是___________ 。
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是___________ (填字母序号)。
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C2H5OH)是___________ (填“可再生”或“不可再生”)能源,乙醇完成燃烧的化学方程式是___________ 。该反应中,化学能转变为___________ 能。
(1)葡萄糖(C6H12O6)中C、H、O原子的数目之比是
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C2H5OH)是
您最近一年使用:0次
6 . 化学与生产生活密切相关,回答下列问题:
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是___________ 。
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是___________ 。
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是___________ 。
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的___________ 。
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的
您最近一年使用:0次
7 . 甲、乙两种物质的溶解度曲线如图所示。下列说法错误的是

| A.80℃时,甲的饱和溶液中溶质与溶剂的质量比为4:5 |
| B.用蒸发结晶的方法可从乙的饱和溶液中获得大量的乙 |
| C.分别将60℃的甲、乙饱和溶液升温至80℃,此时甲溶液的溶质质量分数最大 |
| D.60℃时,向140g甲饱和溶液中先加50g水,再加20g甲,充分溶解后,溶液仍为饱和状态 |
您最近一年使用:0次
8 . 探究铁生锈的条件,有利于寻找防止铁制品锈蚀的方法。下列对比实验设计与所探究的条件(蒸馏水经煮沸并迅速冷却),对应关系正确的是

| A.甲和乙:水 | B.乙和丙:空气 | C.甲和丙:空气 | D.甲和丁:水 |
您最近一年使用:0次
9 . 异烟肼(化学式:C6H7N3O;相对分子质量:137)是治疗肺结核药物的有效成分。下列说法正确的是
| A.异烟肼属于氧化物 |
| B.异烟肼分子中 H、O 原子个数比为 7﹕1 |
| C.异烟肼中 C、H 两种元素的质量比为 36﹕7 |
D.异烟肼中 N 元素质量分数的计算式为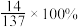 |
您最近一年使用:0次
10 . 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),反应过程的微观示意图如下。下列说法正确的是

| A.物质甲为甲醛,其分子由碳原子和水分子构成 |
| B.物质乙中氧元素的化合价为-2 价 |
| C.该反应前后原子种类和数目均发生改变 |
| D.该反应消耗物质甲和生成物质丁的质量比为 5﹕3 |
您最近一年使用:0次



