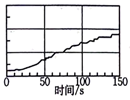
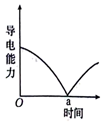
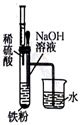
1 . 下列选项描述与对应图像不相符的是
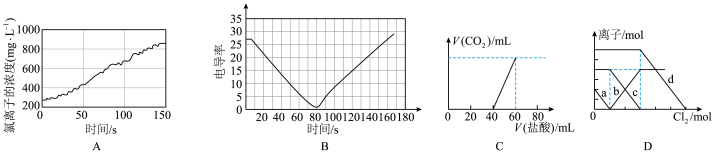
A.图A为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图B向某浓度的 溶液中滴入稀 溶液中滴入稀 ,溶液电导率随时间变化的曲线 ,溶液电导率随时间变化的曲线 |
C.图C为向等物质的量浓度的 、 、 混合液中滴加盐酸产生 混合液中滴加盐酸产生 的图像 的图像 |
D.图D为 、 、 混合液,各离子物质的量随氯气通入的变化图像,b代表的是 混合液,各离子物质的量随氯气通入的变化图像,b代表的是 |
您最近一年使用:0次
解题方法
2 . 将一定量的 通入一定浓度的
通入一定浓度的 溶液中,二者恰好完全反应,生成物中有三种含氯元素的离子,其中
溶液中,二者恰好完全反应,生成物中有三种含氯元素的离子,其中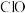 和
和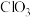 两种离子的物质的量
两种离子的物质的量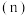 与反应时间
与反应时间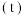 的变化关系如图所示。下列说法错误的是
的变化关系如图所示。下列说法错误的是
 通入一定浓度的
通入一定浓度的 溶液中,二者恰好完全反应,生成物中有三种含氯元素的离子,其中
溶液中,二者恰好完全反应,生成物中有三种含氯元素的离子,其中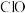 和
和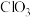 两种离子的物质的量
两种离子的物质的量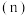 与反应时间
与反应时间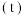 的变化关系如图所示。下列说法错误的是
的变化关系如图所示。下列说法错误的是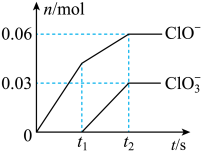
A.参加反应的 与氯气的物质的量之比为 与氯气的物质的量之比为 |
B.反应中转移电子的物质的量为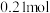 |
C.该 溶液中 溶液中 的质量为 的质量为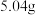 |
D.被氧化和被还原的氯原子的质量之比为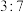 |
您最近一年使用:0次
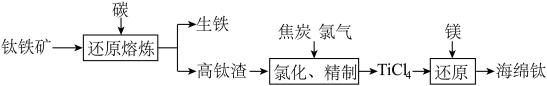
3 . I.一种从钛铁矿中提取金属钛的主要工艺过程如下: (钛酸亚铁),其中钛的化合价为
(钛酸亚铁),其中钛的化合价为___________ 。
(2)第一步:还原熔炼,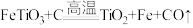 。
。
第二步:氯化精制,二氧化钛在高温下与氯气、焦炭反应生成四氯化钛和一种可燃性气体,请写出该反应的化学方程式:________________ 。
第三步:还原精炼,镁还原四氯化钛的反应类型为___________ (填四大基本反应类型)。
Ⅱ. (高铁酸钾)是一种新型、高效、多功能绿色水处理剂,比
(高铁酸钾)是一种新型、高效、多功能绿色水处理剂,比 氧化性更强,无二次污染。
氧化性更强,无二次污染。
(3)湿法制备高铁酸钾:在碱性环境下,反应体系中有六种微粒: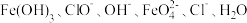 。
。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______________ 。
②若反应过程中转移了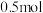 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________ 。
(4)高铁酸钾可用于水的杀菌消毒的原因是_____________ 。
(5)干法制备高铁酸钾:先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。由此可知高铁酸钾的溶解度比高铁酸钠的
至饱和,使高铁酸钾析出。由此可知高铁酸钾的溶解度比高铁酸钠的___________ (填“大”或“小”)。
(6)室温下,现有 浓度均为
浓度均为 的试样,分别在
的试样,分别在 为4.74、7.00、11.50的条件下静置,结果见图,说明高铁酸钾溶液在
为4.74、7.00、11.50的条件下静置,结果见图,说明高铁酸钾溶液在___________ (填“酸”“中”或“碱"”)性环境下更稳定。
 (钛酸亚铁),其中钛的化合价为
(钛酸亚铁),其中钛的化合价为(2)第一步:还原熔炼,
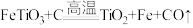 。
。第二步:氯化精制,二氧化钛在高温下与氯气、焦炭反应生成四氯化钛和一种可燃性气体,请写出该反应的化学方程式:
第三步:还原精炼,镁还原四氯化钛的反应类型为
Ⅱ.
 (高铁酸钾)是一种新型、高效、多功能绿色水处理剂,比
(高铁酸钾)是一种新型、高效、多功能绿色水处理剂,比 氧化性更强,无二次污染。
氧化性更强,无二次污染。(3)湿法制备高铁酸钾:在碱性环境下,反应体系中有六种微粒:
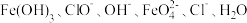 。
。①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
②若反应过程中转移了
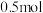 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为(4)高铁酸钾可用于水的杀菌消毒的原因是
(5)干法制备高铁酸钾:先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
 至饱和,使高铁酸钾析出。由此可知高铁酸钾的溶解度比高铁酸钠的
至饱和,使高铁酸钾析出。由此可知高铁酸钾的溶解度比高铁酸钠的(6)室温下,现有
 浓度均为
浓度均为 的试样,分别在
的试样,分别在 为4.74、7.00、11.50的条件下静置,结果见图,说明高铁酸钾溶液在
为4.74、7.00、11.50的条件下静置,结果见图,说明高铁酸钾溶液在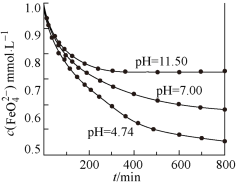
您最近一年使用:0次
解题方法
4 . 回答下列问题:
(1)某同学配制 溶液,回答问题:
溶液,回答问题:
①用托盘天平称取 固体
固体___________ g。
②配制过程所需的玻璃仪器有烧杯、量筒、___________ 。
③定容时仰视刻度线,则所配制的溶液的浓度会___________ (填“偏高”“偏低”或“不变”)。
(2)现有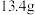 由
由 和
和 组成的混合气体,在标准状况下体积为
组成的混合气体,在标准状况下体积为 。回答问题:
。回答问题:
①混合气体中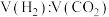 为
为___________ 。
②混合气体中各组分原子个数比 为
为___________ 。
(3)正常人的血液中葡萄糖(简称血糖,分子式为 ,相对分子质量为180)的浓度在
,相对分子质量为180)的浓度在 之间,今测得某病人
之间,今测得某病人 血液中含葡萄糖
血液中含葡萄糖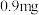 ,相当于
,相当于___________ 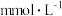 。
。
(4)科学家利用原子示踪法探究催化剂机理时发现,催化剂不是没有参加反应,只是反应前后催化剂的质量与性质不变。已知氯酸钾在二氧化锰催化下分解反应的第一步反应方程式为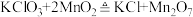 ,请写出第二步反应的化学方程式:
,请写出第二步反应的化学方程式:______________ 。
(1)某同学配制
 溶液,回答问题:
溶液,回答问题:①用托盘天平称取
 固体
固体②配制过程所需的玻璃仪器有烧杯、量筒、
③定容时仰视刻度线,则所配制的溶液的浓度会
(2)现有
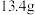 由
由 和
和 组成的混合气体,在标准状况下体积为
组成的混合气体,在标准状况下体积为 。回答问题:
。回答问题:①混合气体中
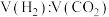 为
为②混合气体中各组分原子个数比
 为
为(3)正常人的血液中葡萄糖(简称血糖,分子式为
 ,相对分子质量为180)的浓度在
,相对分子质量为180)的浓度在 之间,今测得某病人
之间,今测得某病人 血液中含葡萄糖
血液中含葡萄糖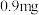 ,相当于
,相当于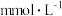 。
。(4)科学家利用原子示踪法探究催化剂机理时发现,催化剂不是没有参加反应,只是反应前后催化剂的质量与性质不变。已知氯酸钾在二氧化锰催化下分解反应的第一步反应方程式为
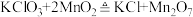 ,请写出第二步反应的化学方程式:
,请写出第二步反应的化学方程式:
您最近一年使用:0次
5 . 某溶液可能由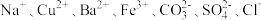 中的若干种离子组成。现取适量溶液进行如下实验:
中的若干种离子组成。现取适量溶液进行如下实验:错误 的是
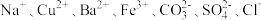 中的若干种离子组成。现取适量溶液进行如下实验:
中的若干种离子组成。现取适量溶液进行如下实验: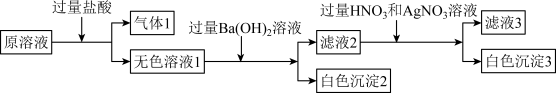
| A.气体1可使澄清石灰水变浑浊 | B.滤液2中加入 不产生白色沉淀 不产生白色沉淀 |
C.原溶液中一定存在 ,一定不存在 ,一定不存在 | D.无色溶液说明不存在 、 、 |
您最近一年使用:0次
解题方法
6 . 某废液中含有大量 、
、 和
和 。为了减少污染并促进废物利用,计划采用如图所示步骤从该废液中回收
。为了减少污染并促进废物利用,计划采用如图所示步骤从该废液中回收 和金属铜,以下说法
和金属铜,以下说法错误 的是
 、
、 和
和 。为了减少污染并促进废物利用,计划采用如图所示步骤从该废液中回收
。为了减少污染并促进废物利用,计划采用如图所示步骤从该废液中回收 和金属铜,以下说法
和金属铜,以下说法
A.滤渣③的成分是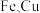 |
| B.步骤I中利用了覆铜板制作印刷电路板的原理 |
| C.过量④可以用稀盐酸,不可用稀硫酸 |
D.通入的⑥气体可换成 ,发生反应的离子方程式是 ,发生反应的离子方程式是 |
您最近一年使用:0次
解题方法
7 . 下列实验或图示与描述不相符的是
| A | B |
数字化实验光照氯水过程中纵坐标代表的物理量可能是 | 向 溶液中加入硫酸铜时溶液的导电能力随时间变化如图,a点说明恰好完全反应 溶液中加入硫酸铜时溶液的导电能力随时间变化如图,a点说明恰好完全反应 |
|
|
| C | D |
此装置可长时间观察到 白色沉淀 白色沉淀 | 纯金属与合金的结构比较,合金内原子层之间的相对滑动变得困难,其硬度变大 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 常温下,往烧杯中加入10mL 1mol/L  溶液和10mL 2mol/L KI溶液,
溶液和10mL 2mol/L KI溶液, 随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
 溶液和10mL 2mol/L KI溶液,
溶液和10mL 2mol/L KI溶液, 随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是 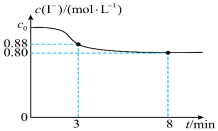
| A.反应一段时间后溶液颜色逐渐变浅 |
B. |
C.3~8min内, 的平均反应速率为0.016mol/(L·min) 的平均反应速率为0.016mol/(L·min) |
| D.8min时,往烧杯中滴加KSCN溶液,溶液不变红 |
您最近一年使用:0次
9 . 连二亚硫酸钠( )俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白剂。
)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白剂。 易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。锌粉法制备
易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。锌粉法制备 的工艺流程如图所示:
的工艺流程如图所示:
(1)工业上常将锌块进行预处理得到锌粉—水悬浊液,其目的是___________ 。
(2)步骤Ⅰ中发生反应的化学方程式为___________ 。
(3)在步骤Ⅲ中得到的 固体要用乙醇洗涤,其优点是
固体要用乙醇洗涤,其优点是___________ 。“后续处理”过程中要加入少量的 固体,其原因是
固体,其原因是___________ 。
(4)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将 和烧碱加入乙醇水溶液中,然后通入
和烧碱加入乙醇水溶液中,然后通入 发生反应,有
发生反应,有 气体放出,总反应的离子方程式为
气体放出,总反应的离子方程式为___________ 。
(5)保险粉可以用于除去废水中的重铬酸根离子( 被转化为
被转化为 ,
, 被转化为
被转化为 ),这是目前除去酸性废水中重铬酸根离子的有效方法之一,写出该反应的离子方程式:
),这是目前除去酸性废水中重铬酸根离子的有效方法之一,写出该反应的离子方程式:___________ 。
(6)保险粉在空气中易吸收 而被氧化。发生反应的化学方程式为:①
而被氧化。发生反应的化学方程式为:①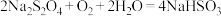 或②
或② 。请设计实验证明氧化时发生的反应是②:
。请设计实验证明氧化时发生的反应是②:___________ 。
 )俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白剂。
)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白剂。 易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。锌粉法制备
易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。锌粉法制备 的工艺流程如图所示:
的工艺流程如图所示: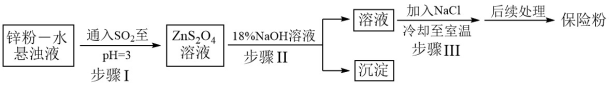
(1)工业上常将锌块进行预处理得到锌粉—水悬浊液,其目的是
(2)步骤Ⅰ中发生反应的化学方程式为
(3)在步骤Ⅲ中得到的
 固体要用乙醇洗涤,其优点是
固体要用乙醇洗涤,其优点是 固体,其原因是
固体,其原因是(4)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将
 和烧碱加入乙醇水溶液中,然后通入
和烧碱加入乙醇水溶液中,然后通入 发生反应,有
发生反应,有 气体放出,总反应的离子方程式为
气体放出,总反应的离子方程式为(5)保险粉可以用于除去废水中的重铬酸根离子(
 被转化为
被转化为 ,
, 被转化为
被转化为 ),这是目前除去酸性废水中重铬酸根离子的有效方法之一,写出该反应的离子方程式:
),这是目前除去酸性废水中重铬酸根离子的有效方法之一,写出该反应的离子方程式:(6)保险粉在空气中易吸收
 而被氧化。发生反应的化学方程式为:①
而被氧化。发生反应的化学方程式为:①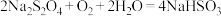 或②
或② 。请设计实验证明氧化时发生的反应是②:
。请设计实验证明氧化时发生的反应是②:
您最近一年使用:0次
10 . 碳、硫的含量对钢铁性能影响很大,其含量的一种测定方法是将钢样中的碳、硫转化为气体,再用测碳、测硫装置进行测定。实验流程如图:___________ 。气体a的主要成分有___________ 、 和未反应的
和未反应的 。
。
(2)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。___________ 。
②计算钢样中碳的质量分数,应测量的数据是___________ 。
(3)为充分吸收气体a测定硫的含量,下列吸收装置合适的是___________ (填字母)。 溶液吸收转化为溶液b,发生反应的化学方程式为
溶液吸收转化为溶液b,发生反应的化学方程式为___________ ,用已知浓度的 溶液滴定生成的溶液b,根据消耗
溶液滴定生成的溶液b,根据消耗 溶液的体积可确定钢样中硫的质量分数。
溶液的体积可确定钢样中硫的质量分数。
(5)某课外小组同学为测定空气中 的含量,将空气样品经过管道通入盛有
的含量,将空气样品经过管道通入盛有 的酸性
的酸性 溶液的密闭容器中。
溶液的密闭容器中。 与该溶液反应的离子方程式为
与该溶液反应的离子方程式为___________ ,若管道中空气流量为 ,经过
,经过 溶液恰好褪色,假定样品中的
溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量为
的含量为___________ g/L。

 和未反应的
和未反应的 。
。(2)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。
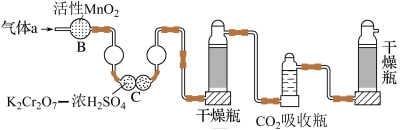
②计算钢样中碳的质量分数,应测量的数据是
(3)为充分吸收气体a测定硫的含量,下列吸收装置合适的是
A. B.
B.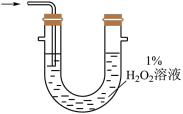 C.
C. D.
D.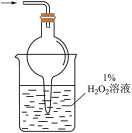
 溶液吸收转化为溶液b,发生反应的化学方程式为
溶液吸收转化为溶液b,发生反应的化学方程式为 溶液滴定生成的溶液b,根据消耗
溶液滴定生成的溶液b,根据消耗 溶液的体积可确定钢样中硫的质量分数。
溶液的体积可确定钢样中硫的质量分数。(5)某课外小组同学为测定空气中
 的含量,将空气样品经过管道通入盛有
的含量,将空气样品经过管道通入盛有 的酸性
的酸性 溶液的密闭容器中。
溶液的密闭容器中。 与该溶液反应的离子方程式为
与该溶液反应的离子方程式为 ,经过
,经过 溶液恰好褪色,假定样品中的
溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量为
的含量为
您最近一年使用:0次