解题方法
1 . 某研究小组用工业钛白副产品为原料制备纳米级电池材料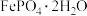 ,按如下流程开展实验。
,按如下流程开展实验。 ,含少量的
,含少量的 、
、 、
、 等杂质。
等杂质。
②已知 和
和 的氧化性随酸性的增强而增强。
的氧化性随酸性的增强而增强。
请回答:
(1)常温下步骤Ⅰ所得料液其pH___________ 7(填“>”、“<”)。
(2)下列说法不正确 的是___________。
(3)步骤Ⅴ中Mn元素的去除率及滤液中Mn元素含量随着溶液pH值的关系如图1所示,___________ 。
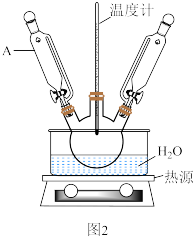
(4)步骤Ⅵ操作之一采用如图2所示装置进行(忽略夹持装置),仪器A的名称是___________ ;该操作不宜用酒精灯直接加热的原因是___________ 。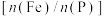 是衡量磷酸铁品质最关键的指标。
是衡量磷酸铁品质最关键的指标。
Fe元素的定量测定:①配制一系列pH=3~5, 浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺(
浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺( )溶液,调pH=3~5,加入邻菲罗啉。③进行比色
)溶液,调pH=3~5,加入邻菲罗啉。③进行比色
①通过比色能获得Fe元素浓度的原理是___________ 。
②测得产品中铁磷比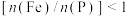 ,可能原因是
,可能原因是___________ 。
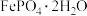 ,按如下流程开展实验。
,按如下流程开展实验。
 ,含少量的
,含少量的 、
、 、
、 等杂质。
等杂质。②已知
 和
和 的氧化性随酸性的增强而增强。
的氧化性随酸性的增强而增强。请回答:
(1)常温下步骤Ⅰ所得料液其pH
(2)下列说法
| A.步骤Ⅱ,加入Fe粉的目的是调节溶液pH值,以便Ti元素水解沉淀 |
B.步骤Ⅲ,加入 的目的是除去Mg元素 的目的是除去Mg元素 |
| C.为了提高实验效率,可以将Ⅱ、Ⅲ、Ⅴ的过滤操作合并 |
D.步骤Ⅳ中过量的 可在步骤Ⅴ中被氧化去除 可在步骤Ⅴ中被氧化去除 |
(3)步骤Ⅴ中Mn元素的去除率及滤液中Mn元素含量随着溶液pH值的关系如图1所示,
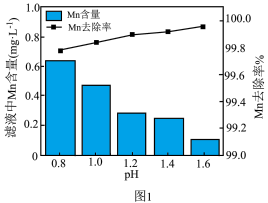
(4)步骤Ⅵ操作之一采用如图2所示装置进行(忽略夹持装置),仪器A的名称是
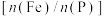 是衡量磷酸铁品质最关键的指标。
是衡量磷酸铁品质最关键的指标。Fe元素的定量测定:①配制一系列pH=3~5,
 浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺(
浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺( )溶液,调pH=3~5,加入邻菲罗啉。③进行比色
)溶液,调pH=3~5,加入邻菲罗啉。③进行比色①通过比色能获得Fe元素浓度的原理是
②测得产品中铁磷比
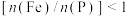 ,可能原因是
,可能原因是
您最近一年使用:0次
解题方法
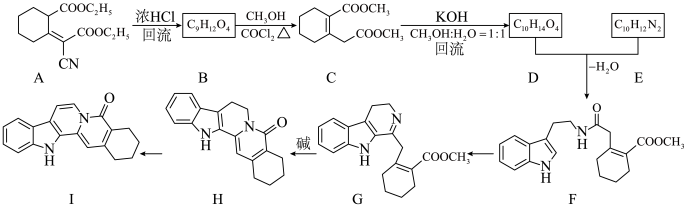
2 . 化合物Ⅰ具有良好的降血压、减肥以及治疗心脏疾病等功效,其合成路线如下(部分反应条件省略)
(1)化合物A的非全碳 官能团名称是___________ 。
(2)下列说法不正确 的是___________。
(3)化合物E的结构简式是___________ 。
(4)写出G→H的化学方程式___________ 。
(5)写出同时符合下列条件的化合物C的一种同分异构体的结构简式___________ 。
①分子中含有苯环且与 溶液发生显色反应
溶液发生显色反应
②核磁共振氢谱和红外光谱检测表明:分子中共有4种不同化学环境的氢原子,不含 键
键
(6)写出以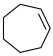 、
、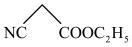 以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。___________
已知:①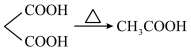
②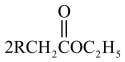
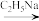
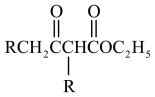
③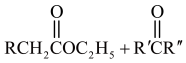

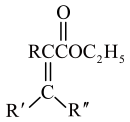
(1)化合物A的
(2)下列说法
| A.A→B的转变只是官能团种类和数量的变化 |
B.在B→C的反应中, 作催化剂 作催化剂 |
C.化合物G的分子式为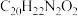 |
| D.化合物I可在酸性或碱性条件下发生水解反应 |
(3)化合物E的结构简式是
(4)写出G→H的化学方程式
(5)写出同时符合下列条件的化合物C的一种同分异构体的结构简式
①分子中含有苯环且与
 溶液发生显色反应
溶液发生显色反应②核磁共振氢谱和红外光谱检测表明:分子中共有4种不同化学环境的氢原子,不含
 键
键(6)写出以
 、
、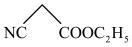 以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
3 . 以锗石矿A(化学式为 )为原料,可以实现如下转化。
)为原料,可以实现如下转化。
请回答:
(1)D的化学式为___________ ,液体E的沸点___________  (填“高于”或“低于”)。
(填“高于”或“低于”)。
(2)下列说法不正确 的是___________。
(3)已知液体E以物质的量之比1∶1与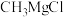 反应,该反应可用来构建
反应,该反应可用来构建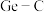 键,写出步骤Ⅲ的化学方程式
键,写出步骤Ⅲ的化学方程式___________ 。
(4)写出溶液G中所有的阴离子___________ ,设计实验证明溶液G中含有Cu元素___________ 。
 )为原料,可以实现如下转化。
)为原料,可以实现如下转化。
请回答:
(1)D的化学式为
 (填“高于”或“低于”)。
(填“高于”或“低于”)。(2)下列说法
| A.气体B是形成酸雨的成分之一 | B.固体C中可能含有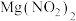 |
C. 也能与浓盐酸反应 也能与浓盐酸反应 | D.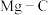 键强于 键强于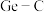 键 键 |
(3)已知液体E以物质的量之比1∶1与
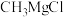 反应,该反应可用来构建
反应,该反应可用来构建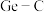 键,写出步骤Ⅲ的化学方程式
键,写出步骤Ⅲ的化学方程式(4)写出溶液G中所有的阴离子
您最近一年使用:0次
4 . 已知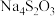 和
和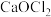 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法不正确 的是
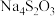 和
和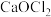 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法A.1mo 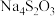 固体中共含有6mol离子 固体中共含有6mol离子 |
B.向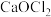 中加入足量稀硫酸会有 中加入足量稀硫酸会有 产生,被氧化与被还原的原子数相等 产生,被氧化与被还原的原子数相等 |
C.向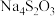 中加入足量稀硫酸时发生反应: 中加入足量稀硫酸时发生反应: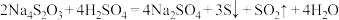 。 。 |
D. 是含有极性键的非极性分子 是含有极性键的非极性分子 |
您最近一年使用:0次
5 . 在给定条件下,下列物质间转化能一步实现的是
A.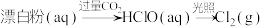 |
B.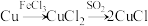 |
C.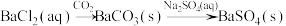 |
D.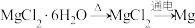 |
您最近一年使用:0次
6 . 电解高浓度的丙酸钠溶液可制得丁烷,下列说法不正确 的是
A.阳极反应为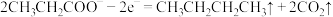 |
| B.电解过程中溶液的pH不断增大 |
| C.若电解槽存在阳离子交换膜,则每生成1mol丁烷,阳极区增重44g |
D.已知电解过程中会生成乙基自由基(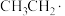 ),采用高浓度丙酸钠是为了提高自由基偶联的概率 ),采用高浓度丙酸钠是为了提高自由基偶联的概率 |
您最近一年使用:0次
名校
解题方法
7 . 硫酸与Cl2反应的生成物的结构如图所示。有关说法不正确的是
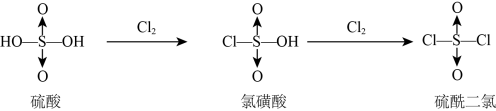
| A.氯磺酸钠NaSO3Cl与水反应:NaSO3Cl+H2O=Na++OH-+HSO3Cl- |
B.硫酰二氯与水反应的离子方程式:SO2Cl2+6H2O=4H3O++ +2Cl- +2Cl- |
| C.氯磺酸与BaCl2溶液反应的化学方程式:HSO3Cl+BaCl2+H2O=BaSO4↓+3HCl |
| D.硫酰二氯可脱去金属氯化物中的水:MgCl2·6H2O+3SO2Cl2=MgCl2+3H2SO4+6HCl |
您最近一年使用:0次
名校
解题方法
8 . 1994年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V形,键角116.5o,与SO2近似,三个原子以一个O原子为中心,与另外两个O原子分别构成一个极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个大π键——三个O原子均等地享有这4个电子。在1.01×105Pa,273K时,O3在催化剂作用下能迅速转化为O2,当生成该状态下22.4L O2时,转移电子数的物质的量为
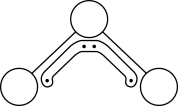
| A.1 mol | B.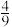 mol mol | C.0 mol | D.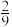 mol mol |
您最近一年使用:0次
9 . S8与NH3在无水条件下反应,得到一种二元化合物A,元素分析可知,A中含S元素69.60%。A进行如下反应:
(1)A、B、C、D的化学式分别为___________ 、___________ 、___________ 、___________ 。
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式___________ 。
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式___________ ,理由是___________ ,该Lewis结构式中,S原子的电子构型是___________ 。

(1)A、B、C、D的化学式分别为
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式
您最近一年使用:0次
10 . 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是
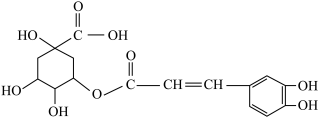
| A.绿原酸的分子式为C16H16O9 |
| B.1mol绿原酸最多与4molNaOH反应 |
| C.1个绿原酸分子中含有4个手性碳原子 |
| D.绿原酸分子能与1.3-丁二烯加热条件下进行D-A反应 |
您最近一年使用:0次



