23-24高一下·全国·期末
1 . 回答下列问题:
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有______________ (写一种)。
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_______________ 等。
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是________________ 。
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是
您最近一年使用:0次
23-24高一下·全国·课前预习
解题方法
2 . “乙醇燃料电池”的工作原理为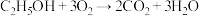 ,装置如图所示。
,装置如图所示。 的移动方向为由
的移动方向为由_______ (填“A到B”或“B到A”)。写出A电极的电极反应式:_____________ 。
②若标况下有11.2L 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为_______ 。
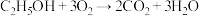 ,装置如图所示。
,装置如图所示。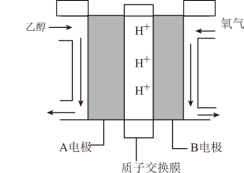
 的移动方向为由
的移动方向为由②若标况下有11.2L
 参与反应,理论上通过质子交换膜的
参与反应,理论上通过质子交换膜的 数目为
数目为
您最近一年使用:0次
21-22高一下·全国·单元测试
3 . 乙烯应用:乙烯是石油化工重要的基本原料,通过一系列反应,乙烯可以合成有机高分子材料、_______ 等。乙烯产量可以用来衡量一个国家_______ 的发展水平。乙烯还是一种植物_______ 。
您最近一年使用:0次
21-22高一下·全国·单元测试
4 . 乙烯物理性质:乙烯为_______ 色、稍有_______ 的气体,_______ 溶于水,密度比空气的_______ 。熔、沸点分别为-169℃、-104℃。
您最近一年使用:0次
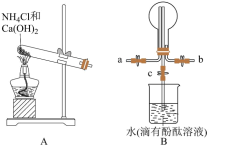
5 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ ;干燥氨气常用的干燥剂是___________ 。
(2)收集氨气时,请你选择氨气的进气口___________ (填“a”或“b”),理由是___________ 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是___________ 。
(2)收集氨气时,请你选择氨气的进气口
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
您最近一年使用:0次
2024-05-21更新
|
150次组卷
|
2卷引用:名校期末好题汇编-非金属元素(非选择题)
名校
解题方法
6 . 某小组同学设计实验实现几种价态硫元素的转化。
Ⅰ:从下列试剂中选择合适的试剂实现S(+6价)→S(+4价)的转化。
试剂清单:①浓H2SO4;②稀H2SO4;③酸性KMnO4溶液;④Na2SO3溶液;⑤Cu;⑥品红溶液。
(1)写出实现转化的化学方程式:___________ 。
(2)设计实验,证明实现了该转化(写出操作和现象):___________ 。
Ⅱ:实现硫元素在0价、+2价、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2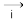 Na2SO3溶液
Na2SO3溶液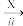 Na2S2O3溶液
Na2S2O3溶液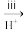 X
X
(3)ⅰ中加入的物质是___________ ,该转化说明SO2的类别是___________ 。
(4)写出ⅲ反应的离子方程式:___________ 。
Ⅰ:从下列试剂中选择合适的试剂实现S(+6价)→S(+4价)的转化。
试剂清单:①浓H2SO4;②稀H2SO4;③酸性KMnO4溶液;④Na2SO3溶液;⑤Cu;⑥品红溶液。
(1)写出实现转化的化学方程式:
(2)设计实验,证明实现了该转化(写出操作和现象):
Ⅱ:实现硫元素在0价、+2价、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2
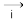 Na2SO3溶液
Na2SO3溶液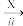 Na2S2O3溶液
Na2S2O3溶液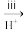 X
X(3)ⅰ中加入的物质是
(4)写出ⅲ反应的离子方程式:
您最近一年使用:0次
2024-05-11更新
|
88次组卷
|
2卷引用:湖北省武汉西藏中学2023-2024学年高一下学期5月期中考试化学试题
7 . 塑料
(1)主要成分:_______ 。如:_______ 、_______ 、聚氯乙烯、_______ 树脂等。
(2)性能:强度高、密度_______ 、耐腐蚀、易加工。
(3)常见塑料
①聚乙烯(PE),结构简式为_______ 。
②聚氯乙烯(PVC):结构简式_______ 。
③聚苯乙烯(PS):结构简式为_______ 。
④聚四氟乙烯(PTFE):结构简式为_______ 。
⑤聚丙烯(PP):结构简式为_______ 。
⑥有机玻璃(PMMA)和电玉(UF)等。
(1)主要成分:
(2)性能:强度高、密度
(3)常见塑料
①聚乙烯(PE),结构简式为
②聚氯乙烯(PVC):结构简式
③聚苯乙烯(PS):结构简式为
④聚四氟乙烯(PTFE):结构简式为
⑤聚丙烯(PP):结构简式为
⑥有机玻璃(PMMA)和电玉(UF)等。
您最近一年使用:0次
8 . 价类二维图是学习和研究物质转化及其性质的有效方法,如图是氮元素的价类二维图。回答下列问题:_______ ,B_______ 。
(2)从N元素的化合价分析,N2具有氧化性和还原性,请写出N2还原性化学方程式:_______ 。
(3)写出铜与硝酸反应生成物质A的离子方程式_______ 。
(4)HNO3与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。
(5)物质D是一种重要的氮肥,写出检验D的阳离子的方法_______ 。

(2)从N元素的化合价分析,N2具有氧化性和还原性,请写出N2还原性化学方程式:
(3)写出铜与硝酸反应生成物质A的离子方程式
(4)HNO3与图中的物质C常用于检验
 的存在,则C的化学式为
的存在,则C的化学式为(5)物质D是一种重要的氮肥,写出检验D的阳离子的方法
您最近一年使用:0次
2024-05-08更新
|
134次组卷
|
2卷引用:名校期末好题汇编-非金属元素(非选择题)
9 . 烷烃——只含有碳和氢两种元素
(1)示例:乙烷的结构式为_______ ,分子式为_______ ,丙烷的结构式为_______ ,分子式为_______ 。
(2)结构特点
①分子中碳原子之间都以_______ 结合;
②碳原子的剩余价键均与_______ 结合,使碳原子的化合价都达到“饱和”,称为饱和烃,又称烷烃。
(3)分子组成通式:链状烷烃中的碳原子数为n,氢原子数就是_______ ,分子通式可表示为_______ 。
(4)烷烃的一般命名
①方法
②示例:C4H10称_______ ,C8H18称_______ ,C12H26称_______ 。
(1)示例:乙烷的结构式为
(2)结构特点
①分子中碳原子之间都以
②碳原子的剩余价键均与
(3)分子组成通式:链状烷烃中的碳原子数为n,氢原子数就是
(4)烷烃的一般命名
①方法
| 碳原子数(n)及表示 | ||||||||||
| n≤10 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| n>10 | 相应汉字数字 | |||||||||
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
10 . 氨气( )
)
(1)分子结构:由极性键形成的_______ 形的极性分子,N原子有一孤对电子;N为_______ 价,为N元素的最低价态;
(2)物理性质:_______ 气味的气体,密度比空气_______ ,_______ 溶于水,常温常压下1体积水能溶解_______ 体积的氨气,易_______ ;
(3)化学性质:
①与 反应:
反应:_______ ,溶液呈弱碱性,氨水的成分为:_______ ;氨水易_______ ;
②与酸反应:硫酸_______ ,盐酸_______ (有白烟生成);
③还原性(催化氧化):_______ (N为 价,最低价态,具有还原性);
价,最低价态,具有还原性);
(4)实验室制法_______ ;工业上采取 与
与 在高温高压催化剂条件下合成氨气;
在高温高压催化剂条件下合成氨气;
(5)用途:化工原料,制硝酸、氮肥等,做_______ 剂。
 )
)(1)分子结构:由极性键形成的
(2)物理性质:
(3)化学性质:
①与
 反应:
反应:②与酸反应:硫酸
③还原性(催化氧化):
 价,最低价态,具有还原性);
价,最低价态,具有还原性);(4)实验室制法
 与
与 在高温高压催化剂条件下合成氨气;
在高温高压催化剂条件下合成氨气;(5)用途:化工原料,制硝酸、氮肥等,做
您最近一年使用:0次



