解题方法
1 . 某同学在研究钠及其化合物的性质时,将一块纯净的金属钠置于氧气流中充分加热进行反应,最终得到淡黄色固体。冷却后称量固体的质量为7.8g,将该固体放入适量水中得到溶液500mL,且放出气体。请计算(写出计算过程):
(1)反应中生成气体的体积是多少(标准状况下)________ ?
(2)所得溶液中溶质的物质的量浓度是多少________ ?
(1)反应中生成气体的体积是多少(标准状况下)
(2)所得溶液中溶质的物质的量浓度是多少
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)用20 g NaOH 配制成500 mL溶液,其物质的量浓度为_______ mol/L,从中取出1 mL,其物质的量浓度为_______ mol/L,含溶质_______ g。若将这1 mL溶液用水稀释到100 mL,所得溶液中溶质的物质的量浓度为_______ moI/L。
(2)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为_______ 。
(3)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为_______ 。
(4)标准状况下,1.7g NH3与_______ LH2S气体含有的氢原子数相同。
(1)用20 g NaOH 配制成500 mL溶液,其物质的量浓度为
(2)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为
(3)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
(4)标准状况下,1.7g NH3与
您最近一年使用:0次
2023-11-26更新
|
251次组卷
|
2卷引用:山西省实验中学2023-2024学年高一上学期期中考试化学试题
解题方法
3 . 工业制取盐酸时,将标准状况下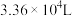 氢气与适量氯气恰好完全反应,再将反应生成的全部气体用水吸收,得到
氢气与适量氯气恰好完全反应,再将反应生成的全部气体用水吸收,得到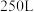 盐酸。请计算该工业制得盐酸的物质的量浓度
盐酸。请计算该工业制得盐酸的物质的量浓度______ 。
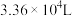 氢气与适量氯气恰好完全反应,再将反应生成的全部气体用水吸收,得到
氢气与适量氯气恰好完全反应,再将反应生成的全部气体用水吸收,得到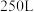 盐酸。请计算该工业制得盐酸的物质的量浓度
盐酸。请计算该工业制得盐酸的物质的量浓度
您最近一年使用:0次
解题方法
4 . 将 氢气在足量氯气中完全燃烧,消耗氯气的物质的量为
氢气在足量氯气中完全燃烧,消耗氯气的物质的量为_____ 。
 氢气在足量氯气中完全燃烧,消耗氯气的物质的量为
氢气在足量氯气中完全燃烧,消耗氯气的物质的量为
您最近一年使用:0次
5 . 辛烷值是衡量汽油抵抗震爆能力的指标。请计算114g辛烷(C8H18)完全燃烧至少需要氧气的体积(标准状况下)_______ 。
您最近一年使用:0次
解题方法
6 . 火法炼铜的一种方法是用 与氧气在高温条件下反应生成铜与
与氧气在高温条件下反应生成铜与 。欲用该方法生产
。欲用该方法生产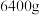 铜单质,请计算同时产生的
铜单质,请计算同时产生的 的体积(标准状况下)
的体积(标准状况下)___________ 。
 与氧气在高温条件下反应生成铜与
与氧气在高温条件下反应生成铜与 。欲用该方法生产
。欲用该方法生产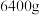 铜单质,请计算同时产生的
铜单质,请计算同时产生的 的体积(标准状况下)
的体积(标准状况下)
您最近一年使用:0次
解题方法
7 . 湿法炼铜(铁与硫酸铜溶液反应)是一种重要的炼铜工艺。欲用该原理制备 铜单质,请计算至少需要铁的物质的量
铜单质,请计算至少需要铁的物质的量____________ 。
 铜单质,请计算至少需要铁的物质的量
铜单质,请计算至少需要铁的物质的量
您最近一年使用:0次
名校
8 . 碳酸氢钠用于焙制糕点,在270℃时分解2NaHCO3 Na2CO3+H2O+CO2↑。现取NaHCO316.8g,在敞口容器中加热到质量不再改变。计算容器中剩余固体物质的质量
Na2CO3+H2O+CO2↑。现取NaHCO316.8g,在敞口容器中加热到质量不再改变。计算容器中剩余固体物质的质量__ (计算结果保留一位小数)。
 Na2CO3+H2O+CO2↑。现取NaHCO316.8g,在敞口容器中加热到质量不再改变。计算容器中剩余固体物质的质量
Na2CO3+H2O+CO2↑。现取NaHCO316.8g,在敞口容器中加热到质量不再改变。计算容器中剩余固体物质的质量
您最近一年使用:0次
2021-10-29更新
|
242次组卷
|
2卷引用:山西省阳泉市第一中学2022-2023学年高一上学期期中考试化学试题
解题方法
9 . 在一定条件下,在2L密闭容器中发生反应3A(g)+B(g)=2C(g),开始时加入4molA、6molB,在2min末时测得C的物质的量是2mol。
(1)用A的浓度变化表示反应的平均速率v(A)=_____ ;
(2)2min末时,B的浓度c(B)=____ ;
(1)用A的浓度变化表示反应的平均速率v(A)=
(2)2min末时,B的浓度c(B)=
您最近一年使用:0次
10 . 合成氨工业是重要的化工基础。欲用N2和H2合成6800gNH3,请利用化学方程式计算参加反应的N2的体积___ (标准状况下)。
您最近一年使用:0次



