解题方法
1 . 将硝酸钠(NaNO3)和硝酸钡[Ba(NO3)2]的混合物29.1g放入烧杯,加入100.0g水使其完全溶解,再加入94.2g硫酸钠溶液恰好完全反应,过滤(忽略溶液的损失),称得滤液的质量为200.0g。请计算:
(1)恰好完全反应后产生的沉淀质量为______ g。
(2)所得滤液的溶质质量分数(写出完整的解题过程)________ 。
(1)恰好完全反应后产生的沉淀质量为
(2)所得滤液的溶质质量分数(写出完整的解题过程)
您最近一年使用:0次
2 . 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。
(1)为研究A的组成与结构,进行如下实验:
(2)综上所述,A的结构简式为___________ 。
(3)两分子A可反应生成一个六元环状化合物,写出该反应的化学方程式___________ 。
(1)为研究A的组成与结构,进行如下实验:
| 实验步骤: | 实验结论 |
| ①称取9.0 g A,升温使其汽化,测其密度是相同条件下H2的45倍 | A的相对分子质量为 |
| ②将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | A的分子式为 |
| ③另取9.0 g A,与足量的NaHCO3粉末反应,生成2.24 LCO2(标准状况);若与足量金属钠反应则生成2.24 LH2 (标准状况) | 用结构简式表示A中含有的官能团 |
④A的核磁共振氢谱如图: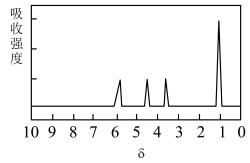 | A中含有 |
(3)两分子A可反应生成一个六元环状化合物,写出该反应的化学方程式
您最近一年使用:0次
2023-07-31更新
|
132次组卷
|
2卷引用:陕西省延安市宜川中学2020-2021学年高二上学期期末考试化学试题
解题方法
3 . 如图是某硫酸试剂瓶标签上的部分文字说明。请计算:
(1)H2SO4的摩尔质量为_____ g/mol。
(2)该试剂瓶中H2SO4的物质的量浓度为______ mol/L。
(3)取10mL该硫酸稀释至100mL,与足量锌粒充分反应求生成氢气的质量______ (写出计算过程)。
| 硫酸 500mL 化学式: H2SO4 密度: 1.84 g/cm3 质量分数: 98% |
(2)该试剂瓶中H2SO4的物质的量浓度为
(3)取10mL该硫酸稀释至100mL,与足量锌粒充分反应求生成氢气的质量
您最近一年使用:0次
2023-01-07更新
|
311次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
名校
解题方法
4 . 回答下列问题
(1)在25℃,101kpa下,1g甲醇( )燃烧生成
)燃烧生成 和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________ 。
(2)已知几种化学键的键能数据如表所示:
请写出氨气与溴蒸气反应的热化学方程式:___________ 。
(3)已知:
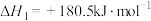

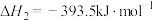
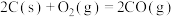
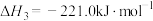
若某反应的平衡常数表达式为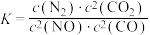 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式___________ 。
(4)根据图示信息写出热化学方程式:___________ 。
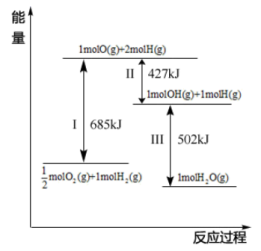
(5)已知:C(s)、CO(g)和 完全燃烧的热化学方程式分别为
完全燃烧的热化学方程式分别为




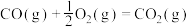
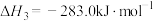
请你根据以上数据,写出C(s)与水蒸气反应生成CO和 的热化学方程式:
的热化学方程式:___________ 。
(1)在25℃,101kpa下,1g甲醇(
 )燃烧生成
)燃烧生成 和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为(2)已知几种化学键的键能数据如表所示:
| 化学键 | N—H |  | Br—Br | H—Br |
键能/ | 391 | 946 | 194 | 366 |
(3)已知:

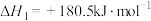

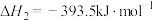
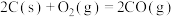
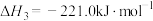
若某反应的平衡常数表达式为
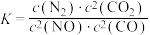 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(4)根据图示信息写出热化学方程式:

(5)已知:C(s)、CO(g)和
 完全燃烧的热化学方程式分别为
完全燃烧的热化学方程式分别为



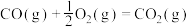
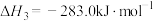
请你根据以上数据,写出C(s)与水蒸气反应生成CO和
 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
解题方法
5 . 常温下,1mLpH=13的Ba(OH)2溶液,其c(OH-)是_________ 。Ba(OH)2物质的量浓度是_________ 。0.01 mol·L-1的NaOH溶液的pH是_________ 。
您最近一年使用:0次
解题方法
6 . 填空。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式_______ 。
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=_______ kJ∙mol-1。
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
则N2(g)+O2(g)=2NO(g) ΔH=_______ kJ·mol-1。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
| 物质 | N2 | O2 | NO |
| 能量(kJ·mol-1) | 946 | 498 | 632 |
您最近一年使用:0次
解题方法
7 . 在一定温度时的水溶液中,若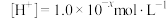 ,
, ,若x和y符合如图所示的线性关系, 过点A和点B。
,若x和y符合如图所示的线性关系, 过点A和点B。

(1)该温度下的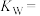
_______ 该中性溶液的pH =_______
(2)在该温度下10 mL 0.01 mol·L-1的盐酸与10 mL 0.015 mol·L-1的Ba(OH)2溶液混合后所得溶液的pH =_______
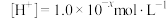 ,
, ,若x和y符合如图所示的线性关系, 过点A和点B。
,若x和y符合如图所示的线性关系, 过点A和点B。
(1)该温度下的
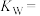
(2)在该温度下10 mL 0.01 mol·L-1的盐酸与10 mL 0.015 mol·L-1的Ba(OH)2溶液混合后所得溶液的pH =
您最近一年使用:0次
解题方法
8 . 25℃时欲使水电离产生的[H+]=10-13 mol·L-1,配制1L溶液,应向其中加入5.0mol·L-1的盐酸溶液_______ L,或加入氢氧化钠晶体_______ g。
您最近一年使用:0次
9 . 在一个容积为1L的密闭容器中,充入5mol H2和2 mol N2。在一定温度和一定压强下,发生如下反应在:3H2(g) +N2(g)  2NH3(g),经过5min后达到平衡状态。若此时测得NH3的浓度为2 mol/L,求:
2NH3(g),经过5min后达到平衡状态。若此时测得NH3的浓度为2 mol/L,求:
(1)达平衡时N2的转化率_______ ;
(2)该温度下的K_______ 。
 2NH3(g),经过5min后达到平衡状态。若此时测得NH3的浓度为2 mol/L,求:
2NH3(g),经过5min后达到平衡状态。若此时测得NH3的浓度为2 mol/L,求:(1)达平衡时N2的转化率
(2)该温度下的K
您最近一年使用:0次
10 . 已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17,Ksp[Mg(OH)2]=4.0×10-12,lg5=0.7。请回答下列问题:
(1)25℃时,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中的c(Ag+)为___________ mol·L-1,pH为___________ 。
(2)25℃时,Mg(OH)2饱和溶液___________ (填“能”或“不能”)使石蕊溶液变蓝色。
(1)25℃时,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中的c(Ag+)为
(2)25℃时,Mg(OH)2饱和溶液
您最近一年使用:0次



