1 . 常温下, 、HCOOH(甲酸)、二元弱酸
、HCOOH(甲酸)、二元弱酸 的电离常数见下表,下列说法正确的是
的电离常数见下表,下列说法正确的是
 、HCOOH(甲酸)、二元弱酸
、HCOOH(甲酸)、二元弱酸 的电离常数见下表,下列说法正确的是
的电离常数见下表,下列说法正确的是| 分子式 |  | HCOOH |  |
| 电离常数 |  |  |  、 、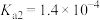 |
A.等物质的量浓度的几种溶液pH大小关系: |
B.HCOONa溶液中滴入少量 ,发生反应 ,发生反应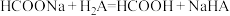 |
C.NaHA溶液中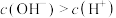 |
D. 的电离常数小于 的电离常数小于 |
您最近一年使用:0次
2 . 0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答:
(1)烃A的分子式为______ 。
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有____ g烃A参加了反应,燃烧时消耗标准状况下的氧气____ L。
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其氯代物只有一种,则烃A的结构简式为_______ 。
(4)若烃A能使溴水褪色,且在催化剂作用下,与 加成所得产物的分子中含4个甲基,烃A可能的结构简式为
加成所得产物的分子中含4个甲基,烃A可能的结构简式为_______ ,比烃A少2个碳原子的同系物,且能和 发生加成反应生成2-甲基丙烷的是
发生加成反应生成2-甲基丙烷的是_______ (填结构简式),它与溴的四氯化碳溶液反应的化学方程式为_______ 。
(1)烃A的分子式为
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其氯代物只有一种,则烃A的结构简式为
(4)若烃A能使溴水褪色,且在催化剂作用下,与
 加成所得产物的分子中含4个甲基,烃A可能的结构简式为
加成所得产物的分子中含4个甲基,烃A可能的结构简式为 发生加成反应生成2-甲基丙烷的是
发生加成反应生成2-甲基丙烷的是
您最近一年使用:0次
名校
解题方法
3 . 硼元素有两种同位素: (相对原子质量10.0129,丰度19.78%)和
(相对原子质量10.0129,丰度19.78%)和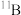 (相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
(相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)___________ 。
 (相对原子质量10.0129,丰度19.78%)和
(相对原子质量10.0129,丰度19.78%)和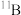 (相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
(相对原子质量11.00931,丰度80.22%)。请列式计算硼元素的相对原子质量(计算结果保留至小数点后两位)
您最近一年使用:0次
名校
解题方法
4 . 用氨水吸收 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液, 时该混合溶液的
时该混合溶液的
___________ 。(已知: 时,电离常数
时,电离常数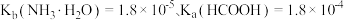 )
)
 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液, 时该混合溶液的
时该混合溶液的
 时,电离常数
时,电离常数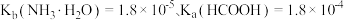 )
)
您最近一年使用:0次
23-24高二下·全国·课前预习
5 . 某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.16%,氢的质量分数为13.14%。则:
(1)氧的质量分数为___________ 。
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈___________ 。
(3)该未知物A的实验式为___________ 。
(1)氧的质量分数为
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈
(3)该未知物A的实验式为
您最近一年使用:0次
解题方法
6 . 常温下,将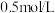 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以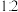 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与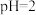 的某一元弱酸溶液
的某一元弱酸溶液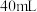 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液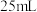 ,试求:
,试求:
(1) 溶液的物质的量浓度为
溶液的物质的量浓度为______  。
。
(2)该一元弱酸的物质的量浓度为______  。
。
(3)此条件下该一元弱酸的电离度为______ 。
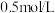 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以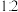 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与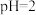 的某一元弱酸溶液
的某一元弱酸溶液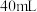 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液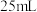 ,试求:
,试求:(1)
 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(2)该一元弱酸的物质的量浓度为
 。
。(3)此条件下该一元弱酸的电离度为
您最近一年使用:0次
名校
7 . 某有机物X(分子组成可表示为CxHyOz)是生物体的一种代谢产物,在不同的生命体中发挥不同的功能。现对X进行相关实验:
①取纯净的X固体9.0g(不含结晶水),控制在125℃~150℃缓慢加热,将其完全转化为蒸气,所得X气体所占体积为2.24L(已折算成标准状况);
②取纯净的X固体18.0g(不含结晶水),迅速加热到190℃以上,使其完全分解,得到三种气体产物;
③将分解产物依次通过足量浓硫酸和无水硫酸铜固体,浓硫酸增重3.6g,无水硫酸铜不显蓝色;
④将剩余的气体8.96L(已折算成标准状况)通过足量澄清石灰水,有白色沉淀生成,最后剩余的气体在装置末端可以被点燃;
⑤被点燃的尾气产生蓝色火焰,用干冷的烧杯罩在火焰上方没有水雾产生,用涂有澄清石灰水的烧杯罩在火焰上方有浑浊。
回答下列问题:
(1)有机物X的摩尔质量为___________ ;X分解产物的化学式为___________ 。
(2)通过计算推导出X的分子式(写出计算过程)___________ 。
(3)取0.5g含有杂质的X固体,溶于水配成25.00mL溶液,取所配溶液于锥形瓶中,加入少量硫酸酸化,用KMnO4溶液滴定至X恰好全部氧化成二氧化碳,共消耗0.002mol 的KMnO4.(MnO 转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为___________ 。
①取纯净的X固体9.0g(不含结晶水),控制在125℃~150℃缓慢加热,将其完全转化为蒸气,所得X气体所占体积为2.24L(已折算成标准状况);
②取纯净的X固体18.0g(不含结晶水),迅速加热到190℃以上,使其完全分解,得到三种气体产物;
③将分解产物依次通过足量浓硫酸和无水硫酸铜固体,浓硫酸增重3.6g,无水硫酸铜不显蓝色;
④将剩余的气体8.96L(已折算成标准状况)通过足量澄清石灰水,有白色沉淀生成,最后剩余的气体在装置末端可以被点燃;
⑤被点燃的尾气产生蓝色火焰,用干冷的烧杯罩在火焰上方没有水雾产生,用涂有澄清石灰水的烧杯罩在火焰上方有浑浊。
回答下列问题:
(1)有机物X的摩尔质量为
(2)通过计算推导出X的分子式(写出计算过程)
(3)取0.5g含有杂质的X固体,溶于水配成25.00mL溶液,取所配溶液于锥形瓶中,加入少量硫酸酸化,用KMnO4溶液滴定至X恰好全部氧化成二氧化碳,共消耗0.002mol 的KMnO4.(MnO
 转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
转化为Mn2+,不考虑X中杂质反应)。请计算X的纯度为
您最近一年使用:0次
2024-02-24更新
|
149次组卷
|
2卷引用:浙江省宁波市北仑中学2023-2024学年高二下学期期中考试化学试题
名校
8 . 在2 L密闭容器中进行反应:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
已知2 min内v(Q)=0.075 mol·L-1·min-1, =0.5
=0.5
(1)试确定以下物质的相关量:起始时n(Y)=___________ ,n(Q)=___________ ;
(2)方程式中m=___________ ,n=___________ ,p=___________ ,q=___________ ;
(3)用Z表示2 min内的反应速率___________ 。
 pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:| 物质 时间 | X | Y | Z | Q |
| 起始/mol | 0.7 | 1 | ||
| 2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3 min末/mol | 0.8 |
 =0.5
=0.5(1)试确定以下物质的相关量:起始时n(Y)=
(2)方程式中m=
(3)用Z表示2 min内的反应速率
您最近一年使用:0次
名校
解题方法
9 . 电化学广泛应用于工业生产和环境保护上。
(1)全钒液流电池是化学储能领域的一个研究热点,储能容量大、使用寿命长。利用该电池电解处理含 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
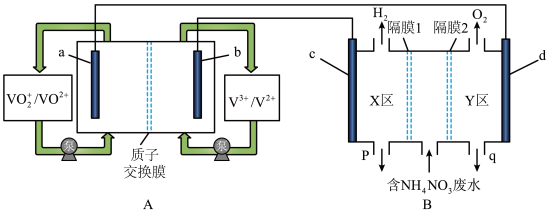
①全钒液流电池放电时,a电极反应式为___________ ,电子的流向由___________ (填“a→导线→d”或“d→导线→a”)。
②隔膜1为___________ 离子交换膜(填“阴”或“阳”),装置B中q口流出液中主要的溶质为___________ (填化学式),d电极的电极反应式为___________ 。
③当装置A中有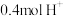 通过质子交换膜时,则装置B中产生气体的总体积为
通过质子交换膜时,则装置B中产生气体的总体积为___________ L(标准状况下),处理___________ 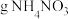 。
。
(2)用电解法可除去硝酸工业产生的尾气NO,并得到 ,工作原理如下图。
,工作原理如下图。
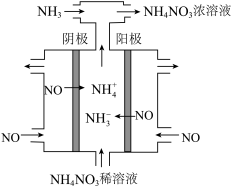
理论上通入 与NO的最佳物质的量之比为
与NO的最佳物质的量之比为___________ 。
(1)全钒液流电池是化学储能领域的一个研究热点,储能容量大、使用寿命长。利用该电池电解处理含
 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
①全钒液流电池放电时,a电极反应式为
②隔膜1为
③当装置A中有
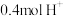 通过质子交换膜时,则装置B中产生气体的总体积为
通过质子交换膜时,则装置B中产生气体的总体积为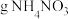 。
。(2)用电解法可除去硝酸工业产生的尾气NO,并得到
 ,工作原理如下图。
,工作原理如下图。
理论上通入
 与NO的最佳物质的量之比为
与NO的最佳物质的量之比为
您最近一年使用:0次
解题方法
10 . 已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)计算H2S的平衡转化率a=_____ (写出计算过程)。
(2)计算浓度平衡常数K=_____ 。(写出计算过程)。
 COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)计算H2S的平衡转化率a=
(2)计算浓度平衡常数K=
您最近一年使用:0次



