名校
解题方法
1 . 化合物M(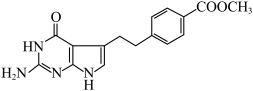 )是合成叶酸抗结剂培美曲塞二钠盐的中间体,可由化合物X(
)是合成叶酸抗结剂培美曲塞二钠盐的中间体,可由化合物X(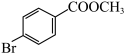 )经过多步反应获得。下列说法正确的是
)经过多步反应获得。下列说法正确的是
A.M的化学式为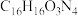 |
| B.M中只有酯基能水解,产物中有甲醇 |
| C.X能发生加成反应、取代反应 |
D.X与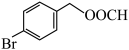 互为同分异构体,且都能与银氨溶液反应 互为同分异构体,且都能与银氨溶液反应 |
您最近一年使用:0次
2 . 某同学设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验探究。下列说法正确的是
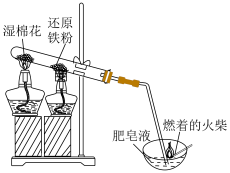

A.该反应的原理为 |
| B.实验中先加热铁粉,再加热湿棉花 |
| C.反应后点燃蒸发皿中产生的气泡,可听到爆鸣声 |
| D.实验结束后应先撤掉导管,再熄灭酒精灯 |
您最近一年使用:0次
3 . 下列各组离子在指定条件下能够大量共存的是
A.在强碱性的溶液中: 、 、 、 、 、 、 |
B.在能使紫色石蕊溶液变为蓝的溶液中: 、 、 、 、 、 、 |
C.在澄清透明的溶液中: 、 、 、 、 、 、 |
D.在 溶液中: 溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
4 . 下列描述的结论能正确解释实验操作所对应的现象的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向NaAlO2溶液中滴加饱和NaHCO3溶液 | 有白色沉淀生成 |  结合H+的能力大于 结合H+的能力大于 |
| B | 用光束分别照射氢氧化铁胶体和三氯化铁溶液 | 氢氧化铁胶体中有一条光亮的通路 | 胶体的分散质粒子使光散射 |
| C | 将Al2O3分别加入氨水和盐酸溶液中 | 仅盐酸中固体溶解 | Al2O3是碱性氧化物 |
| D | FeCl3、KI混合溶液中滴加KSCN溶液 | 溶液呈红色 | FeCl3不与KI反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。高铁酸钠(Na2FeO4)制备方法有:
湿法制备:
干法制备: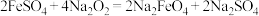 。
。
有关分析错误的是
湿法制备:

干法制备:
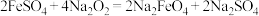 。
。有关分析错误的是
A.干法制备中每生成 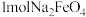 转移 转移  电子 电子 |
| B.湿法制备中,次氯酸钠的氧化性大于高铁酸钠 |
| C.在净水能力上,Na2FeO4氧化能力不如NaClO |
| D.高铁酸钠做水处理剂的优点之一是比较环保 |
您最近一年使用:0次
名校
6 . 运用元素周期律分析下面的推断,其中错误的是
| A.已知Ra是第7周期IIA族的元素,故Ra(OH)2的碱性比 Mg(OH)2的碱性弱 |
| B.已知As是第4周期ⅤA族的元素,故AsH3的稳定性比NH3的稳定性弱 |
| C.已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈 |
| D.已知 Cl的原子半径比 S的原子半径小,故HClO3的酸性比 H2SO3的强 |
您最近一年使用:0次
名校
解题方法
7 . 铁盐与亚铁盐在工业生产和生活中具有重要应用。硫酸亚铁溶液可用于脱除烟气中的二氧化硫等有害气体。  溶液催化脱除烟气中
溶液催化脱除烟气中  的反应原理如图所示。下列说法正确的是
的反应原理如图所示。下列说法正确的是

 溶液催化脱除烟气中
溶液催化脱除烟气中  的反应原理如图所示。下列说法正确的是
的反应原理如图所示。下列说法正确的是
A.“反应I”中氧化剂和还原剂的物质的量之比为  |
B.“反应II”的离子方程式为 |
C.反应一段时间后,溶液中 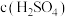 增大 增大 |
D.反应每脱除 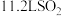 转移电子的物质的量为 转移电子的物质的量为  |
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液 | 溶液颜色变红 | 溶液X含有Fe3+ |
| B | 向饱和的Na2CO3溶液通入CO2 | 产生白色沉淀 | 溶解度:NaHCO3<Na2CO3 |
| C | 向Fe2O3、CuO、Fe的混合粉末中加入过量稀盐酸 | 析出红色固体 | 反应后溶液中阳离子只有H+和Fe2+ |
| D | 取少量溶液Y,先滴加稀硝酸酸化,再滴加适量AgNO3溶液 | 生成白色沉淀 | Y溶液中有Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-22更新
|
131次组卷
|
2卷引用:海南省白沙学校2023-2024学年高一上学期期末考试化学试题
9 . 已知KBrO3可发生反应:2KBrO3 + I2 = 2KIO3 + Br2,下列有关溴酸钾的说法不正确的是
| A.氧化剂与还原剂的物质的量之比为1:2 |
| B.该反应说明I2的还原性强于Br2 |
| C.当有1molKBrO3参与反应时转移5 mol电子 |
| D.该反应中物质氧化性强弱顺序为:KBrO3 < KIO3 |
您最近一年使用:0次
10 . 设NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.18g H2O中含有的电子数目为10 NA |
| B.1 mol·L-1 CaCl2溶液中,含有的Cl-数目为2 NA |
| C.25°C、101kPa下,22.4 L Cl2含的有分子数目为NA |
| D.常温下,1 mol Na与足量氧气反应成Na2O,转移的电子数目为NA |
您最近一年使用:0次



