名校
1 . 在密闭容器中发生反应2SO2+O2⇌2SO3(g),下表各组反应条件为
反应速率由大到小的顺序是
| ① | ② | ③ | ④ | |
| 温度/℃ | 400 | 400 | 300 | 300 |
| C(SO2)/mol/L | 10 | 20 | 5 | 10 |
| C(O2)/mol/L | 5 | 5 | 5 | 5 |
| A.①②③④ | B.②①③④ | C.②①④③ | D.③④①② |
您最近一年使用:0次
名校
解题方法
2 . 完成下列方程式
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:___________ 。
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:___________ 。
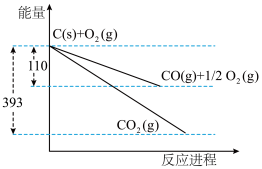
②固体C和CO2气体生成CO气体的热化学方程式:___________ 。
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:___________ 。
(4)某碱性电池的电池反应为3Zn+2K2FeO4 Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:___________ 。
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:

②固体C和CO2气体生成CO气体的热化学方程式:
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:
(4)某碱性电池的电池反应为3Zn+2K2FeO4
 Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
您最近一年使用:0次
名校
解题方法
3 . Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O Cu2O+H2↑装置如图所示,回答下列问题。
Cu2O+H2↑装置如图所示,回答下列问题。
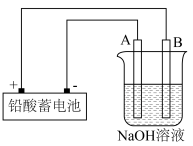
已知铅酸蓄电池的电池反应为PbO2+Pb+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
(1)制备过程中铅酸蓄电池正极电极反应式___________ 。
(2)A、B电极反应式为A:___________ 、B:___________ 。
(3)制备过程中,每生成1molCu2O,电路中转移___________ mol电子,消耗___________ molH2SO4。
 Cu2O+H2↑装置如图所示,回答下列问题。
Cu2O+H2↑装置如图所示,回答下列问题。
已知铅酸蓄电池的电池反应为PbO2+Pb+2H2SO4
 2PbSO4+2H2O
2PbSO4+2H2O(1)制备过程中铅酸蓄电池正极电极反应式
(2)A、B电极反应式为A:
(3)制备过程中,每生成1molCu2O,电路中转移
您最近一年使用:0次
名校
解题方法
4 . 如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL1.0mol/L。

(1)判断装置的名称:A为___________ 。
(2)A装置中,Ag电极的电极反应式为:___________ 。
(3)B装置中的电极b极为电极反应式为___________ ,B装置中总反应的离子方程式为___________ 。
(4)一段时间后,当Zn片质量减少6.5g时,b极生成的气体在标准状况下的体积___________ L,CuSO4溶液的质量___________ (填“增加”或“减少”)了___________ g。
(5)一段时间后,当Zn片质量减少29.25g时,a极生成的气体的物质的量为___________ 。

(1)判断装置的名称:A为
(2)A装置中,Ag电极的电极反应式为:
(3)B装置中的电极b极为电极反应式为
(4)一段时间后,当Zn片质量减少6.5g时,b极生成的气体在标准状况下的体积
(5)一段时间后,当Zn片质量减少29.25g时,a极生成的气体的物质的量为
您最近一年使用:0次
名校
解题方法
5 . 下列有关电解的说法正确的是
| A.惰性电极电解硝酸银溶液不可能在电极上生成银,因为银可以溶于硝酸 |
| B.25℃,惰性电极电解氢氧化钠溶液,溶液pH不变,因为实质是电解水 |
| C.惰性电极电解足量硫酸铜溶液一段时间加入氧化铜固体可使电解质恢复到电解前 |
| D.惰性电极电解淀粉碘化钾溶液,可看到阴极区域溶液变蓝 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法正确的是
| A.电镀时,待镀金属连接电源负极,发生氧化反应 |
| B.工业上电解NaCl水溶液制备钠,电解熔融态Al2O3制备Al |
| C.往往将铁闸门与直流电源的负极相连,这是牺牲阳极的阴极保护法 |
| D.电解精炼铜时,电解液选用硫酸酸化的硫酸铜,精炼过程中,Cu2+浓度降低 |
您最近一年使用:0次
7 . 化学作为一门自然科学倾注着无数科学家的心血和智慧。下列说法不正确 的是
| A.凯库勒——苯的发现和提出苯分子结构学说 |
| B.科里——提出有机合成逆合成分析原理 |
| C.门捷列夫——由无机物合成有机物,打破了有机物的生命力学说 |
| D.贝采利乌斯——首先提出有机化学概念 |
您最近一年使用:0次
名校
8 . 铜银合金在现代工业中有广泛应用。从铜银合金切割废料(不含其它金属)中回收银并制备铜化工产品的工艺如图。
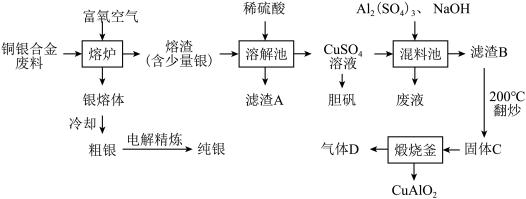
(1)向熔炉中通入适量富氧空气的目的是:___________ 。
(2)滤渣A溶于稀硝酸时产生无色气体,该反应的离子方程式为___________ 。
(3)在混料池中,将三种原料按一定的物质的量之比混合均匀,煮沸,过滤。将滤渣B在200℃下翻炒至质量不再变化,得到固体C.C只含CuO、Al2O3,物质的量之比为2:1。在惰性气体保护下,将C在煅烧釜中高温灼烧,得到CuAlO2.该反应的方程式为___________ 。
(4)若溶解所得溶液中含有1molCuSO4,则混料时应加入___________ molNaOH。
(5)冷却银熔体得到的粗银可使用电解法精炼,精炼池中阳极的电极反应为___________ 。
(6)该工艺中,可循环利用的物质为___________ 。

(1)向熔炉中通入适量富氧空气的目的是:
(2)滤渣A溶于稀硝酸时产生无色气体,该反应的离子方程式为
(3)在混料池中,将三种原料按一定的物质的量之比混合均匀,煮沸,过滤。将滤渣B在200℃下翻炒至质量不再变化,得到固体C.C只含CuO、Al2O3,物质的量之比为2:1。在惰性气体保护下,将C在煅烧釜中高温灼烧,得到CuAlO2.该反应的方程式为
(4)若溶解所得溶液中含有1molCuSO4,则混料时应加入
(5)冷却银熔体得到的粗银可使用电解法精炼,精炼池中阳极的电极反应为
(6)该工艺中,可循环利用的物质为
您最近一年使用:0次
2023-04-26更新
|
114次组卷
|
2卷引用:北京市中国人民大学附属中学2019-2020学年高三下学期月考化学试题
解题方法
9 . 央视《每周质量报告》曝光了一种叫“富氧水”的高价饮用水,它是以饮用水为基质,加压充入氧气制得。打开“富氧水”的瓶盖,气体从瓶中逸出的主要原因是
| A.富氧水变成蒸气挥发出来 |
| B.富氧水中的水蒸气挥发出来 |
| C.压强减小后,使富氧水中氧气溶解度减小而逸出 |
| D.温度升高使富氧水中的水分解 |
您最近一年使用:0次
名校
10 . 回答下列问题
(一)已知碳酸的电离平衡常数约为Ka1=4×10-7,Ka2=5×10-11,HCN电离平衡常数约为6×10-10。
(1)比较给出H+能力的相对强弱:H2CO3___ HCN。(填“>”、“<”或“=”)
(2)用一个离子方程式说明 和CN-结合H+能力的相对强弱
和CN-结合H+能力的相对强弱___ 。
(二)某工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如图所示:
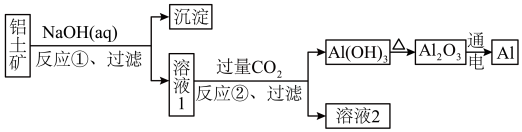
(3)写出反应 ① 的离子方程式____________________________________________________ 。
(4)写出反应 ② 的离子方程式____________________________________________________ 。
(5)以石墨为电极,通过电解熔融Al2O3可制得金属铝。电解池中接电源负极的一极的电极反应式是__________________________________ 。
(6)将溶液1与溶液2混合,观察到有白色沉淀生成,写出生成白色沉淀的离子方程式___________________ 。
(一)已知碳酸的电离平衡常数约为Ka1=4×10-7,Ka2=5×10-11,HCN电离平衡常数约为6×10-10。
(1)比较给出H+能力的相对强弱:H2CO3
(2)用一个离子方程式说明
 和CN-结合H+能力的相对强弱
和CN-结合H+能力的相对强弱(二)某工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如图所示:

(3)写出反应 ① 的离子方程式
(4)写出反应 ② 的离子方程式
(5)以石墨为电极,通过电解熔融Al2O3可制得金属铝。电解池中接电源负极的一极的电极反应式是
(6)将溶液1与溶液2混合,观察到有白色沉淀生成,写出生成白色沉淀的离子方程式
您最近一年使用:0次



