1 . Koselugo(司美替尼selumetinib)是FDA批准的首款NF1治疗药物,用于治疗2岁及以上的I型神经纤维瘤(NF1)儿童患者。化合物F是生产司美替尼的中间体,其合成路线如下:

回答下列问题:
(1)A的名称为___________ 。
(2)A→B反应中所需的条件和试剂是___________ 。
(3)B中含氧官能团的名称为___________ ;B→C反应的反应类型为___________ 。
(4)书写D→E的化学反应方程式___________ 。
(5)A有多种同分异构体,写出两种满足下列条件的同分异构体的结构简式___________ 、___________ 。
a.属于芳香族化合物
b.核磁共振氢谱有2组峰,峰面积之比为2∶1
c.能发生水解反应,也能发生银镜反应
(6)请参照上述流程图,以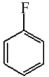 和甲醛为原料,设计
和甲醛为原料,设计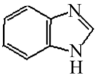 的合成路线图(其他无机试剂任选)
的合成路线图(其他无机试剂任选)___________

回答下列问题:
(1)A的名称为
(2)A→B反应中所需的条件和试剂是
(3)B中含氧官能团的名称为
(4)书写D→E的化学反应方程式
(5)A有多种同分异构体,写出两种满足下列条件的同分异构体的结构简式
a.属于芳香族化合物
b.核磁共振氢谱有2组峰,峰面积之比为2∶1
c.能发生水解反应,也能发生银镜反应
(6)请参照上述流程图,以
 和甲醛为原料,设计
和甲醛为原料,设计 的合成路线图(其他无机试剂任选)
的合成路线图(其他无机试剂任选)
您最近一年使用:0次
名校
解题方法
2 . 保幼酮是保幼激素的一种。保幼激素可以保持昆虫的幼虫特征而阻止其转变为成虫,从而达到阻止昆虫繁殖的作用。合成保幼酮的部分合成路线如图:
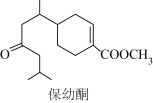

已知:RMgBr
(1)BrCH2COOCH2CH3的化学名称为___ 。保幼酮中所含官能团的名称为___ 。
(2)E的结构简式为___ 。
(3)反应⑧的反应类型为___ 。
(4)反应⑥的化学方程式为___ 。
(5)反应⑥设计的目的为___ 。
(6)化合物D的同分异构体中能同时满足以下三个条件的有___ (不考虑立体异构体,填字母)。
①含有两个甲基;②含有酯基;③苯环上只有一个取代基。
a.不超过6种 b.7~10种 c.11~14种 d.超过14种
同分异构体中,水解产物之一为2—丙醇的结构简式为___ 。


已知:RMgBr

(1)BrCH2COOCH2CH3的化学名称为
(2)E的结构简式为
(3)反应⑧的反应类型为
(4)反应⑥的化学方程式为
(5)反应⑥设计的目的为
(6)化合物D的同分异构体中能同时满足以下三个条件的有
①含有两个甲基;②含有酯基;③苯环上只有一个取代基。
a.不超过6种 b.7~10种 c.11~14种 d.超过14种
同分异构体中,水解产物之一为2—丙醇的结构简式为
您最近一年使用:0次
名校
3 . 乙酸环己酯是一种香料,可用于配制苹果、香蕉等果香型香精。一种制备乙酸环己酯的合成路线如下:
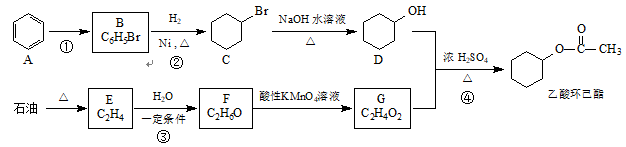
回答下列问题:
(1)反应①所用试剂是__________ ,由石油获得E的生产工艺称为___________ 。
(2)G中官能团名称是_______ ,在反应①~④中,原子利用率理论上可达100%的是_____ (填序号)。
(3)反应③的化学方程式为________________________ ,反应类型是_________ 。
(4)下列关于合成路线中所涉及物质的说法正确的是___________ (填标号)。
a.A、E分子中的原子均处于同一平面 b.用水可分离A和B的混合物
c.D和E均能与KMnO4酸性溶液反应 d.F与D互为同系物
(5)X是E的同系物,其相对分子质量比E大42,X可能的结构有_____ 种,其中含3个-CH3的X结构简式为____________ 。

回答下列问题:
(1)反应①所用试剂是
(2)G中官能团名称是
(3)反应③的化学方程式为
(4)下列关于合成路线中所涉及物质的说法正确的是
a.A、E分子中的原子均处于同一平面 b.用水可分离A和B的混合物
c.D和E均能与KMnO4酸性溶液反应 d.F与D互为同系物
(5)X是E的同系物,其相对分子质量比E大42,X可能的结构有
您最近一年使用:0次
2021-07-14更新
|
1609次组卷
|
5卷引用:吉林省梅河口市第五中学2021-2022学年高二上学期开学考试化学试题
4 . 苯是一种重要的化工原料,用苯合成药物中间体高分子化合物H的路线如下:
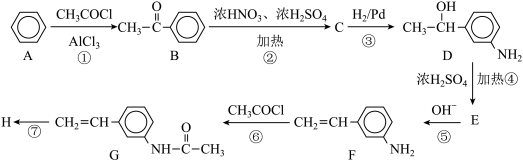
(1)C的结构简式为_________ ,D的分子式为_________ 。
(2)⑥的反应类型为_________ 。
(3)F中含有官能团的名称为_________ 。
(4)下列关于物质D的说法不正确的是_________。
(5)在催化剂、加热、加压条件下⑦的化学方程式_________ 。
(6)C有多种同分异构体,满足下列条件的有_________ 种。写出核磁共振氢谱有4组峰,面积比为1:2:2:2的同分异构体的结构简式_________ 。
①硝基与苯环直接相连
②能发生银镜反应

(1)C的结构简式为
(2)⑥的反应类型为
(3)F中含有官能团的名称为
(4)下列关于物质D的说法不正确的是_________。
| A.与金属Na反应 | B.能使酸性高锰酸钾溶液褪色 |
| C.与FeCl3溶液显紫色 | D.该物质具有两性 |
(6)C有多种同分异构体,满足下列条件的有
①硝基与苯环直接相连
②能发生银镜反应
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题:
(1)合成 所用原料气
所用原料气 ,可用天然气为原料制得,有关反应能量变化如下所示。
,可用天然气为原料制得,有关反应能量变化如下所示。




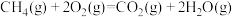

则用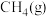 和
和 反应制得
反应制得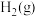 和
和 的热化学方程式为
的热化学方程式为___________ 。
(2)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有 )的原理示意图如下图所示。
)的原理示意图如下图所示。

① 极的电极反应式为
极的电极反应式为___________ , 极附近的
极附近的
___________ (填“变大”或“变小”或“不变”)。
②写出电解池中 转化为
转化为 的离子方程式
的离子方程式___________ 。
(3) 、
、 和熔融
和熔融 可制作燃料电池,其原理见图1,石墨Ⅰ为电池的
可制作燃料电池,其原理见图1,石墨Ⅰ为电池的___________ 极;该电池在使用过程中石墨Ⅰ电极上生成氧化物 ,其电极反应式为
,其电极反应式为___________ 。

(4)如图是用惰性电极电解 硫酸铜溶液,若
硫酸铜溶液,若 电极产生
电极产生 (标准状况)气体,此时溶液中
(标准状况)气体,此时溶液中 浓度为
浓度为___________ (不考虑溶液体积变化)。

(1)合成
 所用原料气
所用原料气 ,可用天然气为原料制得,有关反应能量变化如下所示。
,可用天然气为原料制得,有关反应能量变化如下所示。



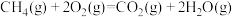

则用
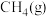 和
和 反应制得
反应制得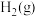 和
和 的热化学方程式为
的热化学方程式为(2)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有
 )的原理示意图如下图所示。
)的原理示意图如下图所示。
①
 极的电极反应式为
极的电极反应式为 极附近的
极附近的
②写出电解池中
 转化为
转化为 的离子方程式
的离子方程式(3)
 、
、 和熔融
和熔融 可制作燃料电池,其原理见图1,石墨Ⅰ为电池的
可制作燃料电池,其原理见图1,石墨Ⅰ为电池的 ,其电极反应式为
,其电极反应式为
(4)如图是用惰性电极电解
 硫酸铜溶液,若
硫酸铜溶液,若 电极产生
电极产生 (标准状况)气体,此时溶液中
(标准状况)气体,此时溶液中 浓度为
浓度为
您最近一年使用:0次
名校
解题方法
6 . 温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将 CO2 应用于生产中实现其综合利用是目前的研究热点。
Ⅰ.在催化作用下由 CO2和 CH4 转化为 CH3COOH 的反应历程示意图如图。

在合成 CH3COOH 的反应历程中,下列有关说法正确的是___________ (填字母)。
a.该催化剂使反应的平衡常数增大
b.CH4 →CH3COOH 过程中,有C—H 键断裂和C—C 键形成
c.生成乙酸的反应原子利用率 100%
d.ΔH=E2-E1
Ⅱ.以 CO2、C2H6为原料合成 C2H4涉及的主要反应如下:
CO2(g)+C2H6 (g) C2H4(g)+H2O(g)+CO(g) ΔH=+177 kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177 kJ·mol-1 (主反应)
C2H6 (g) CH4 (g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4 (g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
(1)主反应的反应历程可分为如下两步,反应过程中能量变化如图1所示:

i.C2H6 (g) C2H4 (g)+H2 (g) ΔH1 =+136 kJ·mol-1
C2H4 (g)+H2 (g) ΔH1 =+136 kJ·mol-1
ii.H2 (g)+CO2 (g) H2O(g)+CO(g) Δ H2
H2O(g)+CO(g) Δ H2
ΔH2=___________ ,主反应的决速步骤为___________ (填“反应 i”或“反应 ii”)
(2)向恒压密闭容器中充入CO2和C2H6,温度对催化剂 K-Fe-Mn/Si-2 性能的影响如图2所示:工业生产中主反应应选择的温度是___________ 。

(3)在一定温度下的密闭容器中充入一定量的CO2和C2H6,固定时间测定不同压强下C2H4的产率如图3所示,P1压强下a点反应速率 v(正)___________ v(逆)。

(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的CO2和C2H6,只发生主反应,达到平衡时 C2H4的物质的量分数为20%,该温度下反应的平衡常数 Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。
(5)我国科学家使用电化学的方法(装置如下图),用 C2H6 和CO2 合成了C2H4.阴极电极反应式是___________ 。

Ⅰ.在催化作用下由 CO2和 CH4 转化为 CH3COOH 的反应历程示意图如图。

在合成 CH3COOH 的反应历程中,下列有关说法正确的是
a.该催化剂使反应的平衡常数增大
b.CH4 →CH3COOH 过程中,有C—H 键断裂和C—C 键形成
c.生成乙酸的反应原子利用率 100%
d.ΔH=E2-E1
Ⅱ.以 CO2、C2H6为原料合成 C2H4涉及的主要反应如下:
CO2(g)+C2H6 (g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177 kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177 kJ·mol-1 (主反应)C2H6 (g)
 CH4 (g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4 (g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)(1)主反应的反应历程可分为如下两步,反应过程中能量变化如图1所示:

i.C2H6 (g)
 C2H4 (g)+H2 (g) ΔH1 =+136 kJ·mol-1
C2H4 (g)+H2 (g) ΔH1 =+136 kJ·mol-1ii.H2 (g)+CO2 (g)
 H2O(g)+CO(g) Δ H2
H2O(g)+CO(g) Δ H2ΔH2=
(2)向恒压密闭容器中充入CO2和C2H6,温度对催化剂 K-Fe-Mn/Si-2 性能的影响如图2所示:工业生产中主反应应选择的温度是

(3)在一定温度下的密闭容器中充入一定量的CO2和C2H6,固定时间测定不同压强下C2H4的产率如图3所示,P1压强下a点反应速率 v(正)

(4)某温度下,在0.1MPa恒压密闭容器中充入等物质的量的CO2和C2H6,只发生主反应,达到平衡时 C2H4的物质的量分数为20%,该温度下反应的平衡常数 Kp=
(5)我国科学家使用电化学的方法(装置如下图),用 C2H6 和CO2 合成了C2H4.阴极电极反应式是

您最近一年使用:0次
2021-06-15更新
|
547次组卷
|
2卷引用:吉林省东北师范大学附属中学2021届高三第五次模拟考试理科综合化学试题



