解题方法
1 . 下列四种肥料可以与草木灰(主要成分是K2CO3)混合施用的是
| A.硫酸铵 | B.氯化铵 | C.硝酸钾 | D.硝酸铵 |
您最近半年使用:0次
2 . 苯是一种重要的化工原料,用苯合成药物中间体高分子化合物H的路线如下:
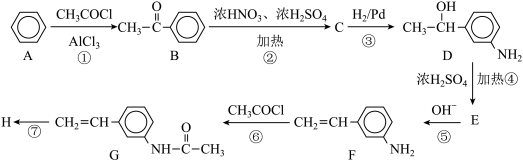
(1)C的结构简式为_________ ,D的分子式为_________ 。
(2)⑥的反应类型为_________ 。
(3)F中含有官能团的名称为_________ 。
(4)下列关于物质D的说法不正确的是_________。
(5)在催化剂、加热、加压条件下⑦的化学方程式_________ 。
(6)C有多种同分异构体,满足下列条件的有_________ 种。写出核磁共振氢谱有4组峰,面积比为1:2:2:2的同分异构体的结构简式_________ 。
①硝基与苯环直接相连
②能发生银镜反应

(1)C的结构简式为
(2)⑥的反应类型为
(3)F中含有官能团的名称为
(4)下列关于物质D的说法不正确的是_________。
| A.与金属Na反应 | B.能使酸性高锰酸钾溶液褪色 |
| C.与FeCl3溶液显紫色 | D.该物质具有两性 |
(6)C有多种同分异构体,满足下列条件的有
①硝基与苯环直接相连
②能发生银镜反应
您最近半年使用:0次
解题方法
3 . 高锰酸钾(KMnO4)被广泛用作氧化剂、消毒剂、水处理剂等。回答下列问题:
(1)基态锰原子的价电子排布式是_________ ,含有_________ 个未成对电子。
(2)高锰酸钾中各元素电负性的大小顺序为_________ 。
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是_________ 。
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是_________ ,其原因是_________ 。过氧化氢中氧原子的杂化方式为_________ 。
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有_________ 个;
②与I距离最近的O形成的空间构型为_________ 。
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为_________ ;
④与I距离最近的钾为_________ nm(已知 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
(1)基态锰原子的价电子排布式是
(2)高锰酸钾中各元素电负性的大小顺序为
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有
②与I距离最近的O形成的空间构型为
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为
④与I距离最近的钾为
 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
您最近半年使用:0次
解题方法
4 . 钛是一种性能非常优越的金属,有着广泛的应用,有人说“21世纪将是钛的世纪”。以金红石矿(主要成分为TiO2,含有少量Al2O3、SiO2、FeO、Fe2O3等杂质)为主要原料,首先反应生成TiCl4,然后再用镁还原得到金属钛,其工艺流程如下:

已知:常温下Fe(OH)3和Fe(OH)2溶度积(Ksp)分别为4.0×10-38和8.0×10-16
请回答下列问题:
(1)加入浓NaOH溶液的目的是_________ 。
(2)镁和氯气主要来源于流程中的某种物质通过电解方法获得,该物质是_________ 。工业生产中需要适当补充该物质,该物质可来源于海水,制备过程如下:向海水中加入石灰乳后,向分离得到的固体中加入过量的盐酸,目的是_________ ,将得到的溶液通过_________ 、冷却结晶操作后得到晶体,在HCl气流中加热晶体即可得到该物质。
(3)高温下,滤渣Y、焦炭和氯气发生反应生成可燃性气体的化学方程式为:_________ 。
(4)工艺流程中稀有气体Ar的作用是_________ 。
(5)为提高原料的利用率,常温下某研究小组向⑤过滤后的滤液中,先加适量的H2O2,再加适量的碱调节溶液的pH至4,过滤后将滤渣加热灼烧,得到了常用的涂料。调节溶液的pH至4时,溶液中金属离子的浓度为_________ mol/L。
(6)TiN具有重要的用途,可在高温下由TiO2与NH3反应制得,同时生成一种可用作保护气的单质气体和一种无色无味的液体。该反应的化学方程式为_________ 。

已知:常温下Fe(OH)3和Fe(OH)2溶度积(Ksp)分别为4.0×10-38和8.0×10-16
请回答下列问题:
(1)加入浓NaOH溶液的目的是
(2)镁和氯气主要来源于流程中的某种物质通过电解方法获得,该物质是
(3)高温下,滤渣Y、焦炭和氯气发生反应生成可燃性气体的化学方程式为:
(4)工艺流程中稀有气体Ar的作用是
(5)为提高原料的利用率,常温下某研究小组向⑤过滤后的滤液中,先加适量的H2O2,再加适量的碱调节溶液的pH至4,过滤后将滤渣加热灼烧,得到了常用的涂料。调节溶液的pH至4时,溶液中金属离子的浓度为
(6)TiN具有重要的用途,可在高温下由TiO2与NH3反应制得,同时生成一种可用作保护气的单质气体和一种无色无味的液体。该反应的化学方程式为
您最近半年使用:0次
5 . 2021年4月21日,国家航天局揭晓我国首辆火星车名称——“祝融号”,同时多项拥有自主知识产权的黑科技悉数亮相,以下说法不正确的是
| A.抵抗极热极寒材料——气溶胶:固体分子簇处于纳米量级,密度小,能产生丁达尔现象 |
| B.登陆车轮毂——铝基碳化硅材料:具有高强度、高耐磨性等优良属性,属于新型复合材料 |
| C.深蓝色闪蝶状高光电转化效率太阳翼:晶体硅呈深蓝色,可用于光电池,实现电能获取 |
| D.正十一烷相变集热器:白天正十一烷吸热液化储能,夜间凝固放热,以便给设备控温 |
您最近半年使用:0次
6 . 已知A、B、C、D、E是中学化学中的常见气体,它们都是由1-18号元素组成的单质或化合物,并有如下的信息:
①A气体能使湿润的红色石蕊试纸变蓝;
②B气体通入品红溶液,红色褪去,继续加热,溶液又变红色;
③C气体通入紫色石蕊试液,溶液先变红色,迅速变为无色;
④D为红棕色、有刺激性气味的气体,能和水反应生成无色气体。
⑤E为黄绿色的、有刺激性气味的气体。
试确定它们的化学式:A_____ ,B____ ,C____ ,D____ ,E____ 。
①A气体能使湿润的红色石蕊试纸变蓝;
②B气体通入品红溶液,红色褪去,继续加热,溶液又变红色;
③C气体通入紫色石蕊试液,溶液先变红色,迅速变为无色;
④D为红棕色、有刺激性气味的气体,能和水反应生成无色气体。
⑤E为黄绿色的、有刺激性气味的气体。
试确定它们的化学式:A
您最近半年使用:0次
2022-12-03更新
|
226次组卷
|
2卷引用:吉林江城中学2021-2022学年高三上学期9月月考化学试题
解题方法
7 . 2014年3月8日马航MH370航班失联,引发世人对航空安全的强烈关注。已知该航班客机机型为波音777,使用了钛铝合金材料。钛铝合金属于
| A.混合物 | B.化合物 | C.氧化物 | D.单质 |
您最近半年使用:0次
8 . 铝土矿中的主要成分是Al2O3,还含有少量Fe2O3等杂质。工业上从铝土矿中提取铝的工艺流程如下图所示。
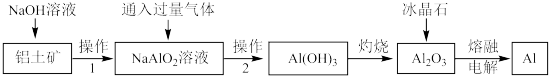
请回答下列问题
(1)“操作1”“操作2”相同,操作的名称为_______ ,实验室进行此项操除使用烧杯外还要使用的玻璃仪器有_______ 。
(2)向 溶液中通入了一种过量气体,这种气体是下列中的
溶液中通入了一种过量气体,这种气体是下列中的_______ (填字母)。
a.HCl b.NH3 c.CO2 d.O2
(3)冶炼铝需要纯度较高的氧化铝,检验得到的氧化铝中不含Fe2O3的化学方法是_______ 。
(4)写出电解熔融氧化铝的方程式_______ 。
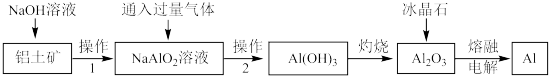
请回答下列问题
(1)“操作1”“操作2”相同,操作的名称为
(2)向
 溶液中通入了一种过量气体,这种气体是下列中的
溶液中通入了一种过量气体,这种气体是下列中的a.HCl b.NH3 c.CO2 d.O2
(3)冶炼铝需要纯度较高的氧化铝,检验得到的氧化铝中不含Fe2O3的化学方法是
(4)写出电解熔融氧化铝的方程式
您最近半年使用:0次
9 . 已知:
(1)在相同浓度的H2CO3和HF的溶液中,用“>”“<”或“=”填空。c(H+):H2CO3_______ HF;c(F-)_______ c(CO )。
)。
(2)HCO 、CO
、CO 、F-、CN-结合质子能力:
、F-、CN-结合质子能力:_______ 。
(3)H2CO3、HCO 、HF、HCN酸性由强到弱的顺序为:
、HF、HCN酸性由强到弱的顺序为:_______ 。
(4)将足量的二氧化碳通入到NaCN溶液中的离子方程式为_______ 。
| H2CO3 | HF | HCN | |
| K或Ka1 | 4.3×10-7 | 7.2×10-4 | 4.9×10-10 |
| Ka2 | 5.6×10-11 |
(1)在相同浓度的H2CO3和HF的溶液中,用“>”“<”或“=”填空。c(H+):H2CO3
 )。
)。(2)HCO
 、CO
、CO 、F-、CN-结合质子能力:
、F-、CN-结合质子能力:(3)H2CO3、HCO
 、HF、HCN酸性由强到弱的顺序为:
、HF、HCN酸性由强到弱的顺序为:(4)将足量的二氧化碳通入到NaCN溶液中的离子方程式为
您最近半年使用:0次
10 . 完成下列问题。
(1)一定条件下,在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示。25℃时,Kw=_______ ,100℃时,Kw=_______ ,100℃若盐酸中c(H+)=1.0×10-4mol/L,则由水电离产生的c(H+)=_______ 。B点时pH=2的盐酸与pH=10的氢氧化钠溶液等体积混合后,溶液显_______ 性。

(2)如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答。
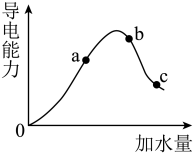
①“O”点为什么不导电_______ 。
②a、b、c三点醋酸的电离程度由大到小的顺序为_______ 。
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是_______ 。
A.H+个数 B.c(H+) C.c(H+)/c(CH3COOH) D.CH3COOH分子数
(1)一定条件下,在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示。25℃时,Kw=

(2)如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答。

①“O”点为什么不导电
②a、b、c三点醋酸的电离程度由大到小的顺序为
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是
A.H+个数 B.c(H+) C.c(H+)/c(CH3COOH) D.CH3COOH分子数
您最近半年使用:0次
2022-09-19更新
|
576次组卷
|
3卷引用:吉林江城中学2021-2022学年高二上学期期中考试化学试题



