高锰酸钾(KMnO4)被广泛用作氧化剂、消毒剂、水处理剂等。回答下列问题:
(1)基态锰原子的价电子排布式是_________ ,含有_________ 个未成对电子。
(2)高锰酸钾中各元素电负性的大小顺序为_________ 。
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是_________ 。
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是_________ ,其原因是_________ 。过氧化氢中氧原子的杂化方式为_________ 。
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有_________ 个;
②与I距离最近的O形成的空间构型为_________ 。
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为_________ ;
④与I距离最近的钾为_________ nm(已知 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
(1)基态锰原子的价电子排布式是
(2)高锰酸钾中各元素电负性的大小顺序为
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有
②与I距离最近的O形成的空间构型为
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为
④与I距离最近的钾为
 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
更新时间:2022-12-09 09:50:26
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】H、C、N、O、Cl是重要的非金属元素。其单质或化合物有重要的应用。
(1)氮原子中电子空间运动状态有____ 种。
(2)C、N、O原子的第一电离能由大到小的顺序是____ 。
(3)已知:
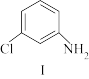 +
+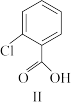

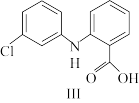
1mol化合物I分子中含有σ键数目为____ 。
(4)已知[Cu(NH3)4]SO4中[Cu(NH3)4]2+具有对称的空间构型,且当两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为____ (填序号);
a.平面正方形b.正四面体c.三角锥型d.V型
(5)联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示:

①Cu2O与NH3·H2O反应能形成较稳定的Cu(NH3) 的原因是
的原因是____ 。
②N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃),沸点(114℃)分别远远高于O2的熔点(-218℃),沸点(-183℃),原因是____ 。
③NaClO发生水解可生成HClO,HClO的空间构型是____ ,中心原子的杂化类型是____ 。
(1)氮原子中电子空间运动状态有
(2)C、N、O原子的第一电离能由大到小的顺序是
(3)已知:
 +
+


1mol化合物I分子中含有σ键数目为
(4)已知[Cu(NH3)4]SO4中[Cu(NH3)4]2+具有对称的空间构型,且当两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
a.平面正方形b.正四面体c.三角锥型d.V型
(5)联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示:

①Cu2O与NH3·H2O反应能形成较稳定的Cu(NH3)
 的原因是
的原因是②N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃),沸点(114℃)分别远远高于O2的熔点(-218℃),沸点(-183℃),原因是
③NaClO发生水解可生成HClO,HClO的空间构型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】丙烯腈CH2=CH-C≡N可通过乙炔(CH≡CH)和氢氰酸(HCN)在CuCl-KCl -NaCl -HCl催化下反应制得。回答下列问题:
(1)Cu+的核外电子排布式为_______ 。
(2)HCN中所含元素的第一电离能由大到小的顺序为_______ 。
(3)CH≡CH分子的空间构型为_______ ;丙烯腈中碳原子的杂化方式为_______ ,其中含有的σ键与π键的数目之比为_______ 。
(4)NaCl的熔点比KCl的熔点高,其原因是_______ 。
(5)已知铜元素的一种氧化物的晶胞结构如图所示,该氧化物的化学式为_______ ,若该晶胞参数为a pm,则该晶体的密度为 _______ g·cm-3(NA表示阿伏加德罗常数的值,列出表达式)。

(1)Cu+的核外电子排布式为
(2)HCN中所含元素的第一电离能由大到小的顺序为
(3)CH≡CH分子的空间构型为
(4)NaCl的熔点比KCl的熔点高,其原因是
(5)已知铜元素的一种氧化物的晶胞结构如图所示,该氧化物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
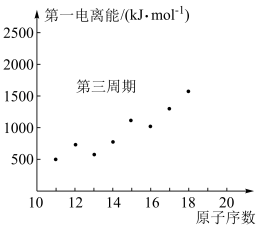
(1)第三周期元素I1变化规律如图所示,第三周期元素中I1处于Al与P之间的元素是___________ 。___________ 。
(3)已知固态HF、H2O、NH3的氢键键能和结构如下:
___________ 个水分子包围形成___________ 构型。
②解释H2O、HF、NH3沸点依次降低的原因___________ 。
(4)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________ 个。
(1)第三周期元素I1变化规律如图所示,第三周期元素中I1处于Al与P之间的元素是
(3)已知固态HF、H2O、NH3的氢键键能和结构如下:
| 物质 | 氢键X-H···Y | 氢键键能kJ·mol-1 |
| (HF)n | F-H···F | 28.1 |
| 冰 | O-H···O | 18.8 |
| (NH3)n | N-H···N | 5.4 |

②解释H2O、HF、NH3沸点依次降低的原因
(4)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铜是人类最早发现并广泛使用的一种金属。黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)Cu的价电子排布式为_______ ,CuFeS2中三种元素的电负性从大到小的顺序为_______ (用元素符号表示)。
(2)在较低温度下,CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①则X是_______ (填化学名称),X分子的立体构型是_______ ,中心原子杂化类型为_______ 。X属于_______ (填“极性”或“非极性”)分子。
②X的沸点比水的沸点_______ (填“高”或“低”),主要原因是_______ 。
(3)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图1所示,该化合物中的化学键有_______ (填标号)。
A.金属键 B.σ键 C.π键 D.氢键 E.配位键
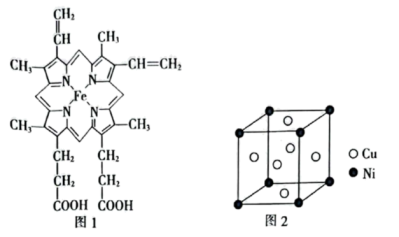
(4)某镍白铜合金的立方晶胞结构如图2所示:
①晶胞中铜原子与镍原子的数目之比为_______ 。
②若该合金的晶胞边长为a nm,则该合金的密度为_______  。(设NA为阿伏加德罗常数的值)
。(设NA为阿伏加德罗常数的值)
(1)Cu的价电子排布式为
(2)在较低温度下,CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①则X是
②X的沸点比水的沸点
(3)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图1所示,该化合物中的化学键有
A.金属键 B.σ键 C.π键 D.氢键 E.配位键

(4)某镍白铜合金的立方晶胞结构如图2所示:
①晶胞中铜原子与镍原子的数目之比为
②若该合金的晶胞边长为a nm,则该合金的密度为
 。(设NA为阿伏加德罗常数的值)
。(设NA为阿伏加德罗常数的值)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】Li、Fe、Al、As、Zn、Cu、Ni等均为重要的合金材料,回答下列问题。
(1)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因是___________ 。
(2)在元素周期表中,与Al化学性质相似的邻族元素是___________ ,其单质与氢氧化钠溶液的反应离子方程式为___________ 。
(3)元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___________ 。
(4)KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为___________ ,写出SCN-的一种等的电子体_________ (填分子),K4[Fe(CN)6]中所含元素电负性由大到小的顺序为__________ 。
(5)H3AsO3的酸性弱于H3AsO4的原因为___________ 。含砷有机物“对氨基苯胂酸”的结构简式如图,As原子轨道杂化类型为___________ ,lmol对氨基苯胂酸含σ键数目为___________ 。

(6)基态Fe原子的价电子排布图为___________ ,用原子结构知识解释Fe2+易被氧化为Fe3+的原因___________ 。
(7)甘氨酸亚铁[(H2NCH2COO)2Fe]的主要生理功能是预防和改善缺铁性贫血。甘氨酸H2NCH2COOH易溶于水,原因为___________ 。
(8)五羰基合铁[Fe(CO)5]的配体是___________ ,配位原子是___________ 。
(1)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因是
(2)在元素周期表中,与Al化学性质相似的邻族元素是
(3)元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
(4)KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为
(5)H3AsO3的酸性弱于H3AsO4的原因为

(6)基态Fe原子的价电子排布图为
(7)甘氨酸亚铁[(H2NCH2COO)2Fe]的主要生理功能是预防和改善缺铁性贫血。甘氨酸H2NCH2COOH易溶于水,原因为
(8)五羰基合铁[Fe(CO)5]的配体是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】含硼化合物由于其特殊的结构和性质在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的核外电子的空间运动状态有_______ 种;B、N、H的电负性由大到小的顺序为_______ 。
(2)含硼阴离子[B6O7(OH)6]2-的结构如图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
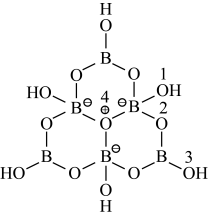
(3)BF3与H2O结合形成固态化合物BF3·OH2…OH2,该物质在6.2℃时熔化电离出H3O+和一种含硼阴离子_______ (填离子符号),该熔化电离过程破坏的作用力为_______ ,H3O+的空间构型为_______ 。
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子:四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90°,棱长为apm,密度为ρg·cm-3,阿伏加德罗常数的值为NA。
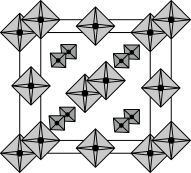
①该晶体的化学式为_______ 。
②金属M原子与硼原子间最短距离为_______ pm。
③金属M的相对原子质量为_______ (列出表达式)
(1)基态硼原子的核外电子的空间运动状态有
(2)含硼阴离子[B6O7(OH)6]2-的结构如图所示。其中硼原子的杂化方式为

(3)BF3与H2O结合形成固态化合物BF3·OH2…OH2,该物质在6.2℃时熔化电离出H3O+和一种含硼阴离子
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子:四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90°,棱长为apm,密度为ρg·cm-3,阿伏加德罗常数的值为NA。

①该晶体的化学式为
②金属M原子与硼原子间最短距离为
③金属M的相对原子质量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】铬铁合金作为钢的添加料生产多种具有高强度、耐高温、耐腐蚀等优良性能的特种钢,这类特种钢中含有碳、硅、氧、氮、磷、硫等元素。
(1)基态Cr原子的价电子排布式为___________ 。
(2) C、N、O、Si三种元素的第一电离能由大到小的顺序为___________ 。
(3)PO 的空间构型为
的空间构型为___________ ,中心原子的杂化方式为___________ 。
(4)SiO2晶体常伴生于各种矿石中,其晶体结构中,最小的环上有___________ 个原子;Si与C元素位于同一主族,比较SiO2与CO2的键角大小:SiO2___________ CO2(填写“大于”、“小于”或“等于”),原因是___________ 。
(5)无水CrCl3和氨分子作用能形成某种配合物,该配合物的组成相当于CrCl3·6NH3.已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构简式___________ ,配位数___________ ,1 mol该配合物中含有σ键的数目为___________ 。
(6)铁和氮形成一种晶体,晶胞结构如图所示,则该晶体的化学式为___________ ,若该晶体的晶胞密度ρg·cm-3,用NA表示阿伏加德罗常数的值,则该晶胞的体积是___________ cm3。
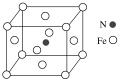
(1)基态Cr原子的价电子排布式为
(2) C、N、O、Si三种元素的第一电离能由大到小的顺序为
(3)PO
 的空间构型为
的空间构型为(4)SiO2晶体常伴生于各种矿石中,其晶体结构中,最小的环上有
(5)无水CrCl3和氨分子作用能形成某种配合物,该配合物的组成相当于CrCl3·6NH3.已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构简式
(6)铁和氮形成一种晶体,晶胞结构如图所示,则该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素。X元素是元素周期表中核电荷数最小的元素。Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质。ZX3气体溶于水呈碱性。W的外围电子排布是3s1。G2+离子的M层d轨道只有5个电子。请回答下列问题:
(1)W在元素周期表中的位置是______ ;W和Z形成的化合物水溶液呈碱性,用离子方程式表示其原因_____ 。
(2)Z原子的第一电离能比氧原子的____ (填“大”或“小”);G的基态原子电子排布式是__________
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是_________ ;该化合物中Y的杂化轨道类型是________ 。
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是____________
(5)可用YX4还原ZOx以消除其污染。已知:
YX4(g) +4ZO2(g)=4ZO(g)+YO2(g)+2X2O(g) △H=-574 kJ·mol-1
YX4(g)+4ZO(g)=2Z2(g)十YO2(g) +2X2O(g) △H = -1160kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式________ 。
(1)W在元素周期表中的位置是
(2)Z原子的第一电离能比氧原子的
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是
(5)可用YX4还原ZOx以消除其污染。已知:
YX4(g) +4ZO2(g)=4ZO(g)+YO2(g)+2X2O(g) △H=-574 kJ·mol-1
YX4(g)+4ZO(g)=2Z2(g)十YO2(g) +2X2O(g) △H = -1160kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】化合物AgMnAs2在磁记录材料领域有着广泛的应用前景,回答下列问题:
(1)Ag的焰色反应与铁相似,接近无色,下列有关焰色反应原理的分析正确的是___ (填字母)。
a.电子从基态跃迁到较高的激发态
b.电子从较高的激发态跃迁回基态
c.焰色反应的光谱属于吸收光谱
d.焰色反应的光谱属于发射光谱
(2)基态Mn原子中核外电子占据的最高能层符号___ 。其核外未成对电子数为___ 个。
(3)Mn(NO3)2中阴离子的空间构型是___ ,Mn、N、O中第一电离能最大的元素是___ (填元素符号)。
(4)NH3、PH3、AsH3的沸点由高到低的顺序为___ (填化学式,下同),键角由大到小的顺序为___ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系AgMnAs2的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。

找出距离Ag(0,0,0)最近的Mn(用分数坐标表示)___ 。
(1)Ag的焰色反应与铁相似,接近无色,下列有关焰色反应原理的分析正确的是
a.电子从基态跃迁到较高的激发态
b.电子从较高的激发态跃迁回基态
c.焰色反应的光谱属于吸收光谱
d.焰色反应的光谱属于发射光谱
(2)基态Mn原子中核外电子占据的最高能层符号
(3)Mn(NO3)2中阴离子的空间构型是
(4)NH3、PH3、AsH3的沸点由高到低的顺序为
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系AgMnAs2的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。

| 坐标 原子 | x | y | z |
| Ag | 0 | 0 | 0 |
| Mn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |
找出距离Ag(0,0,0)最近的Mn(用分数坐标表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】乙炔是有机合成工业的一种重要原料。工业上曾用焦炭制备电石 (CaC2),再与水反应制备乙炔。
(1)焦炭、金刚石和 都是碳的单质。已知金刚石中碳碳键的键长为
都是碳的单质。已知金刚石中碳碳键的键长为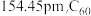 中碳碳键的键长为
中碳碳键的键长为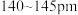 ,二者比较熔点高的是
,二者比较熔点高的是___________ ,理由是___________ 。
(2)乙炔与氢氰酸反应可得丙烯腈 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是___________ ,该分子中 键与
键与 键个数比为
键个数比为___________ 。
(3)将乙炔通入 溶液生成
溶液生成 红棕色沉淀。
红棕色沉淀。 基态核外电子排布式为
基态核外电子排布式为___________ 。 的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:___________ 。
(4)CaC2中 与
与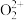 互为等电子体,
互为等电子体,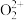 的电子式为
的电子式为___________ 。
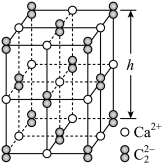
(5)CaC2晶体的晶胞结构与NaCl晶体相似,但CaC2晶体中哑铃形 的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的
的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的 有
有___________ 个。已知CaC2晶体密度为 ,晶胞中两个
,晶胞中两个 的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=
的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=___________ cm。
(1)焦炭、金刚石和
 都是碳的单质。已知金刚石中碳碳键的键长为
都是碳的单质。已知金刚石中碳碳键的键长为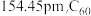 中碳碳键的键长为
中碳碳键的键长为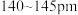 ,二者比较熔点高的是
,二者比较熔点高的是(2)乙炔与氢氰酸反应可得丙烯腈
 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是 键与
键与 键个数比为
键个数比为(3)将乙炔通入
 溶液生成
溶液生成 红棕色沉淀。
红棕色沉淀。 基态核外电子排布式为
基态核外电子排布式为 的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:(4)CaC2中
 与
与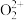 互为等电子体,
互为等电子体,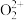 的电子式为
的电子式为(5)CaC2晶体的晶胞结构与NaCl晶体相似,但CaC2晶体中哑铃形
 的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的
的存在,使晶胞沿一个方向拉长,晶胞呈长方体(如图)。每个Ca2+周围距离相等且最近的 有
有 ,晶胞中两个
,晶胞中两个 的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=
的最近距离为acm,阿伏加德罗常数值为NA,则CaC2晶胞中棱长h=
您最近一年使用:0次
【推荐2】I.CP是一种起爆药,化学式为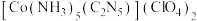 ,CP可由5-氰基四唑(结构简式如图所示)和
,CP可由5-氰基四唑(结构简式如图所示)和 反应制备。
反应制备。

(1)Co原子基态电子排布式为_______ 。
(2)5-氰基四唑分子中C原子的杂化类型为_______ ;1 mol 5-氰基四唑分子中含有σ键的数目为_______ 。
(3)在 配合物中
配合物中
①Co3+的配体为_______ (填分子式)。
②与H2O互为等电子体的一种阳离子为_______ (填化学式)。
③ 空间构型
空间构型_______ 。
Ⅱ.偏钛酸钡在小型变压器,话筒和扩音器中均有应用,其晶胞结构如图所示,则

(1)偏钛酸钡的化学式为_______ 。
(2)与Ba2+最近且等距离的O2-为_______ 个。
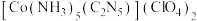 ,CP可由5-氰基四唑(结构简式如图所示)和
,CP可由5-氰基四唑(结构简式如图所示)和 反应制备。
反应制备。
(1)Co原子基态电子排布式为
(2)5-氰基四唑分子中C原子的杂化类型为
(3)在
 配合物中
配合物中①Co3+的配体为
②与H2O互为等电子体的一种阳离子为
③
 空间构型
空间构型Ⅱ.偏钛酸钡在小型变压器,话筒和扩音器中均有应用,其晶胞结构如图所示,则

(1)偏钛酸钡的化学式为
(2)与Ba2+最近且等距离的O2-为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Co、Al、 Si形成的合金是一种高性能的热电材料,备受研究人员关注。回答下列问题:
(1)基态Co原子的核外电子排布式为___________ ,它处于元素周期表的___________ 区。
(2)下列各状态的铝中,再电离出一个电子所需能量最小的是___________ (填序号)。
A. B.
B.
C. D.
D.
(3)AlCl3是某些有机反应的催化剂,如苯酚( )与乙酰氯(
)与乙酰氯( )反应的部分历程为
)反应的部分历程为 。
。
①乙酰氯分子中碳原子的杂化类型为___________ 。
②乙酰氯分子中C-C键与C-Cl键的夹角___________ 120°(填“大于“等于”或“小于”), 判断理由是___________ 。
③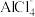 的空间构型为
的空间构型为___________ 。
(4)金刚石、金刚砂(SiC)、单晶硅的熔点由低到高的顺序为___________ 。
(5)Co、Al、Si形成的一种合金的晶胞结构如图所示(若不看 , 该晶胞具有萤石结构),1号原子、2号原、Al原子的分数坐标分别为(0, 1, 0)、(
, 该晶胞具有萤石结构),1号原子、2号原、Al原子的分数坐标分别为(0, 1, 0)、( ,
, ,
, )、(
)、( ,
, ,
, ),则3号原子的分数坐标为
),则3号原子的分数坐标为___________ ; 若晶胞参数为anm,,则该合金的密度为___________ g·cm-3(NA表示阿伏加德罗常数的值,只需列出式子)。

(1)基态Co原子的核外电子排布式为
(2)下列各状态的铝中,再电离出一个电子所需能量最小的是
A.
 B.
B.
C.
 D.
D.
(3)AlCl3是某些有机反应的催化剂,如苯酚(
 )与乙酰氯(
)与乙酰氯( )反应的部分历程为
)反应的部分历程为 。
。①乙酰氯分子中碳原子的杂化类型为
②乙酰氯分子中C-C键与C-Cl键的夹角
③
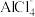 的空间构型为
的空间构型为(4)金刚石、金刚砂(SiC)、单晶硅的熔点由低到高的顺序为
(5)Co、Al、Si形成的一种合金的晶胞结构如图所示(若不看
 , 该晶胞具有萤石结构),1号原子、2号原、Al原子的分数坐标分别为(0, 1, 0)、(
, 该晶胞具有萤石结构),1号原子、2号原、Al原子的分数坐标分别为(0, 1, 0)、( ,
, ,
, )、(
)、( ,
, ,
, ),则3号原子的分数坐标为
),则3号原子的分数坐标为
您最近一年使用:0次



