名校
1 . 由于“新冠”病毒的输入,“84”消毒液已成为必需品。“84”消毒液一般是用氯气和氢氧化钠制备。某同学设计了如图所示的实验装置,按要求回答下列问题:
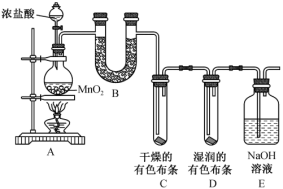
(1)E中反应的离子方程式为___________ 。
(2)装置C中的实验现象为___________ ,装置D中的实验现象为___________ 。
(3)A中挥发出的HCl对C、D中的实验结论是否有影响,请判断并说明理由___________ 。
(4)“84”消毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,证明消毒液已失效的实验操作步骤为___________ 。

(1)E中反应的离子方程式为
(2)装置C中的实验现象为
(3)A中挥发出的HCl对C、D中的实验结论是否有影响,请判断并说明理由
(4)“84”消毒液在空气中久置后,NaClO会转化为HClO,HClO分解失效,证明消毒液已失效的实验操作步骤为
您最近一年使用:0次
名校
解题方法
2 . K2[Cu(C2O4)2]·2H2O(二草酸合铜酸钾,式量为354)为蓝色晶体,是一种具有还原性配体的有机金属化合物。它可溶于热水,微溶于冷水、酒精,干燥时较为稳定,加热时易分解。某小组制备并探究二草酸合铜酸钾热分解的产物、测定草酸根配体的含量。制备流程如图所示:
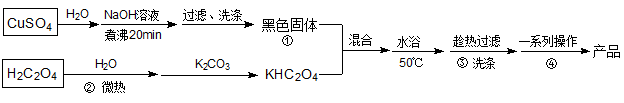
已知:①H2C2O4 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
②Cu2++4NH3·H2O [Cu(NH3)4]2++4H2O
[Cu(NH3)4]2++4H2O
③杂质受热不分解
回答下列问题:
(1)①处“黑色固体”的化学式为___ 。
(2)②处采用“微热”溶解草酸,其原因是加快溶解速率、___ 。③处最适宜的洗涤试剂为___ 。
(3)按如图所示探究二草酸合铜酸钾晶体的热分解产物,装置B、C、F中均盛有足量的澄清石灰水,装置E中填有精细氧化铜粉末(石棉绒作载体)。
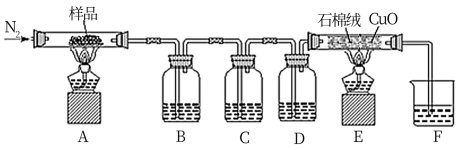
①通入氮气的目的是___ 。
②装置D中盛放的试剂是___ 。
③实验中观察到装置C中澄清石灰水未变浑浊,B、F中澄清石灰水均变浑浊,离心分离后测得沉淀质量相等,装置E中固体变为砖红色。由此推断二草酸合铜酸钾晶体热分解的化学方程式为___ 。
(4)室温下准确称取制取的晶体试样1.000g溶于氨水(1:1)中,并加水定容至250mL。取试样溶液25.00mL于锥形瓶中,再加入10mL3mol/L的H2SO4溶液,水浴加热至75~85℃,趁热用0.0100mol/L的KMnO4溶液滴定。平行滴定三次,KMnO4标准液平均消耗20.00mL。
①样品能溶解于氨水的原因是___ 。
②滴定终点的现象为___ 。
③该产品的纯度为___ 。

已知:①H2C2O4
 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O②Cu2++4NH3·H2O
 [Cu(NH3)4]2++4H2O
[Cu(NH3)4]2++4H2O③杂质受热不分解
回答下列问题:
(1)①处“黑色固体”的化学式为
(2)②处采用“微热”溶解草酸,其原因是加快溶解速率、
(3)按如图所示探究二草酸合铜酸钾晶体的热分解产物,装置B、C、F中均盛有足量的澄清石灰水,装置E中填有精细氧化铜粉末(石棉绒作载体)。

①通入氮气的目的是
②装置D中盛放的试剂是
③实验中观察到装置C中澄清石灰水未变浑浊,B、F中澄清石灰水均变浑浊,离心分离后测得沉淀质量相等,装置E中固体变为砖红色。由此推断二草酸合铜酸钾晶体热分解的化学方程式为
(4)室温下准确称取制取的晶体试样1.000g溶于氨水(1:1)中,并加水定容至250mL。取试样溶液25.00mL于锥形瓶中,再加入10mL3mol/L的H2SO4溶液,水浴加热至75~85℃,趁热用0.0100mol/L的KMnO4溶液滴定。平行滴定三次,KMnO4标准液平均消耗20.00mL。
①样品能溶解于氨水的原因是
②滴定终点的现象为
③该产品的纯度为
您最近一年使用:0次
2021-05-11更新
|
432次组卷
|
3卷引用:吉林省东北师范大学附属中学2021届高三下学期第四次模拟考试理科综合化学试题
名校
3 . 下列装置或操作能达到实验目的的是
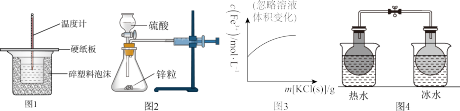

| A.用图1所示装置测定中和热 |
B.用图2所示装置测定 与硫酸反应的速率 与硫酸反应的速率 |
C.用图3表示向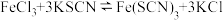 平衡体系中加入 平衡体系中加入 固体, 固体, 浓度的变化曲线 浓度的变化曲线 |
D.用图4所示装置利用装有 和 和 的混合气体的烧瓶探究温度对化学平衡移动的影响 的混合气体的烧瓶探究温度对化学平衡移动的影响 |
您最近一年使用:0次
名校
解题方法
4 . 实验室可利用如图所示装置还原 并检验该反应的产物。已知CO发生装置中的反应为
并检验该反应的产物。已知CO发生装置中的反应为 。
。

(1)试剂Y是___________ ,E中预期的实验现象是___________ 。
(2)向D中通入气体与点燃D处酒精灯的顺序是___________ ;实验中当D中固体变为黑色后就熄灭D处酒精灯,继续通CO冷却至室温的目的是___________ ;从环保角度上考虑,需对以上装置进行改进,改进的方法是___________ 。
(3)当固体冷却至室温时,某同学用磁铁进行试验,发现黑色固体能全部被磁铁吸引,该同学思考分析后猜想黑色固体的组成可能有i、ⅱ、iii三种情况,为确定其成分,他设计了如下方案:先将适量固体置于盛有足量盐酸的小烧杯中,观察产生的现象(记为①),待烧杯中反应停止后再加入试剂 ,观察现象(记为②),请填写下表。
,观察现象(记为②),请填写下表。
(4)若猜想ii成立,写出D中反应的化学方程式:___________ 。
 并检验该反应的产物。已知CO发生装置中的反应为
并检验该反应的产物。已知CO发生装置中的反应为 。
。
(1)试剂Y是
(2)向D中通入气体与点燃D处酒精灯的顺序是
(3)当固体冷却至室温时,某同学用磁铁进行试验,发现黑色固体能全部被磁铁吸引,该同学思考分析后猜想黑色固体的组成可能有i、ⅱ、iii三种情况,为确定其成分,他设计了如下方案:先将适量固体置于盛有足量盐酸的小烧杯中,观察产生的现象(记为①),待烧杯中反应停止后再加入试剂
 ,观察现象(记为②),请填写下表。
,观察现象(记为②),请填写下表。| 可能成分 | i:只有Fe | ii:只有 | iii:含有 、 、 | |
| 预期实验现象 | ① | —— | ||
| ② | 溶液无变化 | 溶液变为血红色 | —— | |
您最近一年使用:0次
5 . 某课外活动小组的同学通过进行乙醇的催化氧化实验来制取乙醛,其装置如图所示(部分夹持装置已略去)。下列有关说法错误的是
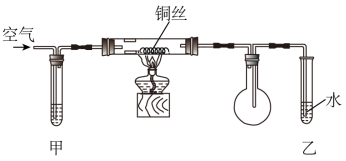
已知:乙醛的沸点为20.8℃,能与水互溶。

已知:乙醛的沸点为20.8℃,能与水互溶。
| A.实验开始时,需要检查装置气密性 |
| B.实验时,试管甲处需要用温水浴加热 |
| C.实验中,可观察到铜丝出现红色和黑色交替的现象 |
| D.实验结束后,装有铜丝的玻璃管的总质量减小 |
您最近一年使用:0次
2021-07-03更新
|
377次组卷
|
4卷引用:吉林省白山市2020-2021学年高一下学期期末考试化学试题
解题方法
6 . (1)1分子烷烃A中含有20个氢原子,写出该烷烃的分子式___ 。
(2)相对分子质量为212的烷烃,写出该烷烃的分子式___ 。
(3)正戊烷的结构简式为__ 。其同分异构体为___ (填结构简式)。
(4)写出甲烷与氯气发生取代反应的化学方程式___ (写第一步即可)。实验室中用如图所示的装置进行甲烷与氯气反应的实验。

光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是___ 。(填序号)
A.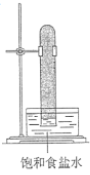 B.
B.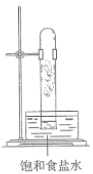 C.
C. D.
D.
(2)相对分子质量为212的烷烃,写出该烷烃的分子式
(3)正戊烷的结构简式为
(4)写出甲烷与氯气发生取代反应的化学方程式

光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是___________ (填序号),可作为证据的实验现象是___________ (填字母序号)。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”);当有0.1molO2生成时,转移电子的物质的量为___________ mol。
II.全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下,配平此化学方程式。___________
(3)_____NaIO3+______NaHSO3——_____NaHSO4+_______Na2SO4+_____I2+_____H2O
III.锑(Sb)被广泛用于生产各种阻燃剂、合金、陶瓷、半导体元件、医药用品等。以辉锑矿为原料制备金属锑的一种工艺流程如下。已知:辉锑矿的主要成分为Sb2S3,还含As2S5、PbS、CuO和SiO2等;浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AlCl3和PbCl2等。
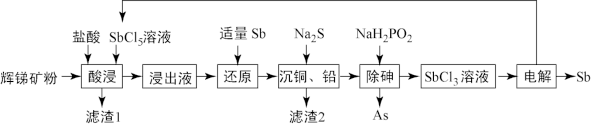
(4)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是___________ (填化学式)。
(5)写出“还原”反应的化学方程式___________ 。
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是
| 序号 | 实验 | 实验现象 |
| 1 | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去; b.有大量气泡产生 |
| 2 | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
II.全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下,配平此化学方程式。
(3)_____NaIO3+______NaHSO3——_____NaHSO4+_______Na2SO4+_____I2+_____H2O
III.锑(Sb)被广泛用于生产各种阻燃剂、合金、陶瓷、半导体元件、医药用品等。以辉锑矿为原料制备金属锑的一种工艺流程如下。已知:辉锑矿的主要成分为Sb2S3,还含As2S5、PbS、CuO和SiO2等;浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AlCl3和PbCl2等。

(4)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是
(5)写出“还原”反应的化学方程式
您最近一年使用:0次
2021-07-28更新
|
1110次组卷
|
3卷引用:吉林省长春希望高中2020-2021学年高二下学期期末考试化学试题
8 . 某同学为验证酸性:醋酸>碳酸>苯酚,经仔细考虑,设计如下实验装置,请回答下列问题:
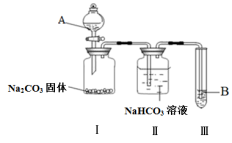
(1)A处的试剂是_______ (填序号,下同),B处的试剂是_______ 。
①醋酸溶液 ②CH3COONa溶液 ③苯酚溶液 ④苯酚钠溶液
(2)装置II中饱和NaHCO3溶液的作用_______ 。
(3)能证明三种酸的酸性强弱的现象_______ 。
(4)写出装置III中发生反应的化学方程式_______ 。

(1)A处的试剂是
①醋酸溶液 ②CH3COONa溶液 ③苯酚溶液 ④苯酚钠溶液
(2)装置II中饱和NaHCO3溶液的作用
(3)能证明三种酸的酸性强弱的现象
(4)写出装置III中发生反应的化学方程式
您最近一年使用:0次
2021-04-29更新
|
680次组卷
|
4卷引用:吉林省长春市第二十中学2020-2021学年高二下学期第二次质量测试化学试题
吉林省长春市第二十中学2020-2021学年高二下学期第二次质量测试化学试题北京市丰台区2020-2021学年高二下学期期中联考化学(B卷)试题(已下线)作业07 醇 酚-2021年高二化学暑假作业(人教版2019)(已下线)第08讲 酚(讲义)-【寒假自学课】2023年高二化学寒假精品课(人教版2019选择性必修3)
名校
解题方法
9 . 某化学小组进行NaHCO3热稳定性实验,并检验部分分解产物,请回答下列问题:

(1)图中仪器A的名称是___ ,图中仪器B的名称是___ 。
(2)按图连接装置后,首先应检查装置的___ 。
(3)仪器A管口向下倾斜的原因是___ 。
(4)开始加热后,C管中出现___ 现象,证明有CO2气体生成。
(5)经检验A中残留固体是Na2CO3,则NaHCO3受热分解的化学方程式为___ 。

(1)图中仪器A的名称是
(2)按图连接装置后,首先应检查装置的
(3)仪器A管口向下倾斜的原因是
(4)开始加热后,C管中出现
(5)经检验A中残留固体是Na2CO3,则NaHCO3受热分解的化学方程式为
您最近一年使用:0次
名校
10 . 科学实验中,要尽可能避免干扰因素对实验的影响。下列分析错误的


| A.用甲操作检验K+,应透过蓝色钴玻璃观察火焰颜色,来排除Na+干扰 |
| B.用乙装置制备氢氧化亚铁,胶头滴管插到覆盖一层苯的液面以下,以防止空气干扰 |
| C.用丙装置制备并检验乙烯,氢氧化钠溶液用来排除CO2对乙烯检验的干扰 |
| D.丁装置中,读出H2的体积时,待装置冷却至室温,将漏斗缓缓下移至两端的液面处于相平,是为了防止温度和压强对气体体积的影响 |
您最近一年使用:0次
2021-06-30更新
|
1442次组卷
|
5卷引用:吉林省长春外国语学校2022届高三上学期期初考试化学试题



