1 . 苯是一种重要的化工原料,用苯合成药物中间体高分子化合物H的路线如下:
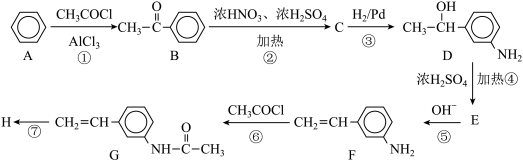
(1)C的结构简式为_________ ,D的分子式为_________ 。
(2)⑥的反应类型为_________ 。
(3)F中含有官能团的名称为_________ 。
(4)下列关于物质D的说法不正确的是_________。
(5)在催化剂、加热、加压条件下⑦的化学方程式_________ 。
(6)C有多种同分异构体,满足下列条件的有_________ 种。写出核磁共振氢谱有4组峰,面积比为1:2:2:2的同分异构体的结构简式_________ 。
①硝基与苯环直接相连
②能发生银镜反应

(1)C的结构简式为
(2)⑥的反应类型为
(3)F中含有官能团的名称为
(4)下列关于物质D的说法不正确的是_________。
| A.与金属Na反应 | B.能使酸性高锰酸钾溶液褪色 |
| C.与FeCl3溶液显紫色 | D.该物质具有两性 |
(6)C有多种同分异构体,满足下列条件的有
①硝基与苯环直接相连
②能发生银镜反应
您最近一年使用:0次
解题方法
2 . 高锰酸钾(KMnO4)被广泛用作氧化剂、消毒剂、水处理剂等。回答下列问题:
(1)基态锰原子的价电子排布式是_________ ,含有_________ 个未成对电子。
(2)高锰酸钾中各元素电负性的大小顺序为_________ 。
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是_________ 。
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是_________ ,其原因是_________ 。过氧化氢中氧原子的杂化方式为_________ 。
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有_________ 个;
②与I距离最近的O形成的空间构型为_________ 。
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为_________ ;
④与I距离最近的钾为_________ nm(已知 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
(1)基态锰原子的价电子排布式是
(2)高锰酸钾中各元素电负性的大小顺序为
(3)已知元素Mn与Fe的第三电离能分别为:I3(Mn)=3248kJ/mol、I3(Fe)=2957kJ/mol,I3(Mn)>I3(Fe)的原因是
(4)氧与硫位于相同主族,它们的最简单氢化物的沸点较高的是
(5)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,如图所示。晶胞中K、I、O分别处于顶角、体心、面心位置,晶胞参数为a=0.446nm。

①距离K最近且距离相等的O有
②与I距离最近的O形成的空间构型为
③已知A坐标(0,0,0),B坐标(1,1,1),则I的坐标为
④与I距离最近的钾为
 =1.732,计算结果保留小数点后三位有效数字)。
=1.732,计算结果保留小数点后三位有效数字)。
您最近一年使用:0次
解题方法
3 . 钛是一种性能非常优越的金属,有着广泛的应用,有人说“21世纪将是钛的世纪”。以金红石矿(主要成分为TiO2,含有少量Al2O3、SiO2、FeO、Fe2O3等杂质)为主要原料,首先反应生成TiCl4,然后再用镁还原得到金属钛,其工艺流程如下:

已知:常温下Fe(OH)3和Fe(OH)2溶度积(Ksp)分别为4.0×10-38和8.0×10-16
请回答下列问题:
(1)加入浓NaOH溶液的目的是_________ 。
(2)镁和氯气主要来源于流程中的某种物质通过电解方法获得,该物质是_________ 。工业生产中需要适当补充该物质,该物质可来源于海水,制备过程如下:向海水中加入石灰乳后,向分离得到的固体中加入过量的盐酸,目的是_________ ,将得到的溶液通过_________ 、冷却结晶操作后得到晶体,在HCl气流中加热晶体即可得到该物质。
(3)高温下,滤渣Y、焦炭和氯气发生反应生成可燃性气体的化学方程式为:_________ 。
(4)工艺流程中稀有气体Ar的作用是_________ 。
(5)为提高原料的利用率,常温下某研究小组向⑤过滤后的滤液中,先加适量的H2O2,再加适量的碱调节溶液的pH至4,过滤后将滤渣加热灼烧,得到了常用的涂料。调节溶液的pH至4时,溶液中金属离子的浓度为_________ mol/L。
(6)TiN具有重要的用途,可在高温下由TiO2与NH3反应制得,同时生成一种可用作保护气的单质气体和一种无色无味的液体。该反应的化学方程式为_________ 。

已知:常温下Fe(OH)3和Fe(OH)2溶度积(Ksp)分别为4.0×10-38和8.0×10-16
请回答下列问题:
(1)加入浓NaOH溶液的目的是
(2)镁和氯气主要来源于流程中的某种物质通过电解方法获得,该物质是
(3)高温下,滤渣Y、焦炭和氯气发生反应生成可燃性气体的化学方程式为:
(4)工艺流程中稀有气体Ar的作用是
(5)为提高原料的利用率,常温下某研究小组向⑤过滤后的滤液中,先加适量的H2O2,再加适量的碱调节溶液的pH至4,过滤后将滤渣加热灼烧,得到了常用的涂料。调节溶液的pH至4时,溶液中金属离子的浓度为
(6)TiN具有重要的用途,可在高温下由TiO2与NH3反应制得,同时生成一种可用作保护气的单质气体和一种无色无味的液体。该反应的化学方程式为
您最近一年使用:0次
4 . 2021年4月21日,国家航天局揭晓我国首辆火星车名称——“祝融号”,同时多项拥有自主知识产权的黑科技悉数亮相,以下说法不正确的是
| A.抵抗极热极寒材料——气溶胶:固体分子簇处于纳米量级,密度小,能产生丁达尔现象 |
| B.登陆车轮毂——铝基碳化硅材料:具有高强度、高耐磨性等优良属性,属于新型复合材料 |
| C.深蓝色闪蝶状高光电转化效率太阳翼:晶体硅呈深蓝色,可用于光电池,实现电能获取 |
| D.正十一烷相变集热器:白天正十一烷吸热液化储能,夜间凝固放热,以便给设备控温 |
您最近一年使用:0次
5 . 下列关于电化学腐蚀及防护的说法不正确 的是
| A.“牺牲阳极的阴极保护法”就是将被保护的钢铁设备连接到外接直流电源的负极 |
| B.白铁皮是在薄钢板表面镀锌,即便镀层破损,仍然可以保护钢板不被腐蚀 |
| C.在钢铁制品表面喷漆、涂油、镀铬或覆盖搪瓷、塑料都可以避免钢铁腐蚀 |
| D.钢铁表面吸附的溶有氧气的水膜酸性很弱时,仍然以吸氧腐蚀为主 |
您最近一年使用:0次
2021-11-20更新
|
514次组卷
|
4卷引用:吉林省大安市第一中学校2021-2022学年高二上学期第三次月考化学试题
吉林省大安市第一中学校2021-2022学年高二上学期第三次月考化学试题浙江省温州市十校联合体2021-2022学年高二上学期期中联考化学试题(已下线)4.4 金属的腐蚀与防护-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第28讲 金属的腐蚀与防护(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
6 . 下列说法中正确的是
| A.电解熔融状态下的AlCl3或Al2O3均可得到单质铝 |
| B.钢铁、铜在适当条件均可发生吸氧腐蚀、析氢腐蚀 |
C.向 的稀混合液中滴加AgNO3溶液,可确定Ksp(AgCl)、Ksp(AgI)的相对大小 的稀混合液中滴加AgNO3溶液,可确定Ksp(AgCl)、Ksp(AgI)的相对大小 |
| D.BaSO4、BaCO3均难溶于水,故BaCO3不能与Na2SO4溶液反应 |
您最近一年使用:0次
2021-11-17更新
|
241次组卷
|
2卷引用:吉林省洮南市第一中学2021-2022学年高二上学期第三次月考化学试题
名校
解题方法
7 . 近年来国家大力扶持新能源项目建设。图1是太阳能电池工作示意图,可与图2石墨烯锂电池联合使用。已知石墨烯锂电池的反应式为: (M=Mn、Co、Ni),下列说法错误的是
(M=Mn、Co、Ni),下列说法错误的是

 (M=Mn、Co、Ni),下列说法错误的是
(M=Mn、Co、Ni),下列说法错误的是
| A.给石墨烯锂电池充电时,Y接太阳能电池的P电极 |
| B.石墨烯锂电池具有能量密度高的优点 |
C.石墨烯锂电池放电时,负极反应为: |
| D.石墨烯锂电池充电时,每转移2mol电子,图2阳极质量减少7g |
您最近一年使用:0次
2021-11-11更新
|
1076次组卷
|
3卷引用:吉林省洮南市第一中学2021-2022学年高二上学期第三次月考化学试题
8 . 已知①N2(g)+3H2(g)  2NH3(g) ΔH<0,反应速率为v1;
2NH3(g) ΔH<0,反应速率为v1;
②2HI(g) H2(g)+I2(g) ΔH>0,反应速率为v2。
H2(g)+I2(g) ΔH>0,反应速率为v2。
对于上述两个可逆反应,当改变条件时,试判断v1、v2的变化(填“增大”、“减小”或“不变”)
(1)保持体积不变,反应①通入N2,反应②分离出I2(g),v1___________ ,v2___________ 。
(2)保持压强不变,反应①②通入“He”气,v1___________ ,v2___________ 。
(3)反应①、反应②均压缩体积,v1___________ ,v2___________ 。
(4)保持体积不变,反应①②通入“He”气,v1___________ ,v2___________ 。
(5)其他条件不变,反应①②均升温,v1___________ ,v2___________ 。
(6)其他条件不变,反应①②均加入正催化剂,v1___________ ,v2___________ 。
 2NH3(g) ΔH<0,反应速率为v1;
2NH3(g) ΔH<0,反应速率为v1;②2HI(g)
 H2(g)+I2(g) ΔH>0,反应速率为v2。
H2(g)+I2(g) ΔH>0,反应速率为v2。对于上述两个可逆反应,当改变条件时,试判断v1、v2的变化(填“增大”、“减小”或“不变”)
(1)保持体积不变,反应①通入N2,反应②分离出I2(g),v1
(2)保持压强不变,反应①②通入“He”气,v1
(3)反应①、反应②均压缩体积,v1
(4)保持体积不变,反应①②通入“He”气,v1
(5)其他条件不变,反应①②均升温,v1
(6)其他条件不变,反应①②均加入正催化剂,v1
您最近一年使用:0次
名校
9 . 某气体化合物A密度是同温同压下H2密度的14倍,则A为
| A.N2 | B.CO | C.O2 | D.NH3 |
您最近一年使用:0次
2021-11-07更新
|
120次组卷
|
2卷引用:吉林省洮南市第一中学2021-2022学年高一上学期期中考试化学试题
10 . 生产、生活离不开各种化学物质,下列说法不正确的是
| A.Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,NaHCO3可用于治疗胃酸过多及制造发酵粉等 |
| B.ClO2和O3可用于自来水消毒 |
| C.在食品袋中放入盛有生石灰的透气小袋,可防止食物受潮变质 |
| D.漂白粉处理水和明矾处理水原理相同 |
您最近一年使用:0次



