1 . 控制变量法是科学研究的重要方法。相同质量的锌与足量的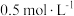 硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是
硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是
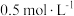 硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是
硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是| 选项 | 锌的状态 | 实验温度 |
| A | 粉末 | 20 |
| B | 粉末 | 30 |
| C | 块状 | 20 |
| D | 块状 | 30 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . “绿水青山就是金山银山。”下列相关做法错误的是
| A.垃圾分类回收 | B.化石燃料脱硫 | C.推广使用氢能源 | D.先污染后治理 |
您最近一年使用:0次
3 . 摄入人体内的淀粉在酶的催化作用下可发生如下转化过程。
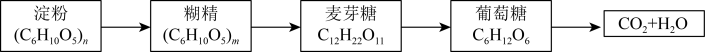
| A.n>m |
| B.上述转化过程均为水解反应 |
C.葡萄糖转化为CO2和H2O的过程中能量转化:热能 化学能 化学能 |
| D.纤维素在人体内也可按上述转化过程最终水解成葡萄糖 |
您最近一年使用:0次
7日内更新
|
474次组卷
|
3卷引用:2023年7月浙江省普通高中学业水平考试(学考)化学试题
2023年7月浙江省普通高中学业水平考试(学考)化学试题浙江省杭州市联谊学校2023-2024学年高一下学期5月教学质量检测化学选考试题(已下线)期末押题卷02-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
解题方法
4 . 工业上以黄铁矿为原料制备硫酸的原理示意图如下。
(1)黄铁矿主要成分的化学式是_______ 。
(2)SO2使品红溶液褪色,体现SO2具有_______ 性。
(3)步骤Ⅲ的化学方程式是_______ 。
(4)下列说法不正确 的是_______。

(1)黄铁矿主要成分的化学式是
(2)SO2使品红溶液褪色,体现SO2具有
(3)步骤Ⅲ的化学方程式是
(4)下列说法
| A.步骤Ⅰ前需将黄铁矿粉碎,目的是增大接触面积,加快反应速率 |
| B.步骤Ⅱ中使用催化剂,能使SO2的转化率达到100% |
| C.步骤Ⅲ中选用98.3%的浓硫酸作吸收剂 |
| D.图中每一步含硫物质均发生氧化反应 |
您最近一年使用:0次
5 . 一定温度下,在1L恒容密闭容器中发生反应: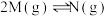 ,测得N的物质的量随时间变化的曲线如图所示。下列说法
,测得N的物质的量随时间变化的曲线如图所示。下列说法不正确 的是
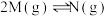 ,测得N的物质的量随时间变化的曲线如图所示。下列说法
,测得N的物质的量随时间变化的曲线如图所示。下列说法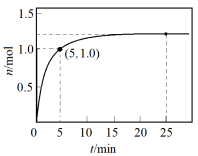
A.0 5 min内,用N表示的平均反应速率为0.2 mol/(L·min) 5 min内,用N表示的平均反应速率为0.2 mol/(L·min) |
| B.5 min时,M的正反应速率小于M的逆反应反应速率 |
| C.5 min时容器内压强大于10min容器内压强 |
| D.25 min时,该反应处于平衡状态 |
您最近一年使用:0次
6 . Mg-AgCl电池是一种贮备电池,充入海水即可激活,电池总反应: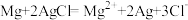 电池工作时,下列说法
电池工作时,下列说法不正确 的是
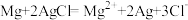 电池工作时,下列说法
电池工作时,下列说法| A.Mg为负极 |
| B.充入电池的海水作电解质溶液 |
| C.电子由负极经电解质溶液流向正极 |
D.正极反应式: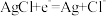 |
您最近一年使用:0次
解题方法
7 .  是重要的供氧剂。图所示装置(省略夹持部件)用于验证
是重要的供氧剂。图所示装置(省略夹持部件)用于验证 和
和 的反应,所需
的反应,所需 由
由 固体与稀盐酸反应制备。回答下列问题:
固体与稀盐酸反应制备。回答下列问题:______ 。
(2)验证装置的气密性时,需用F替换装置中的E。若装置气密性良好,应观察到F中的导管口会有______ 的现象。
(3)装置中的B与C用于除去 气体中的杂质。饱和
气体中的杂质。饱和 溶液的作用是吸收
溶液的作用是吸收______ (填化学式)气体;为了干燥 气体,C中盛放的试剂是足量的
气体,C中盛放的试剂是足量的______ 。
(4)实验过程中,D中部分 固体由淡黄色变为
固体由淡黄色变为______ 色。在E的瓶口放置一条带火星的木条,若木条复燃,则说明生成的气体是______ (填化学式),并且E中的气体______ (填“已集满”或“未集满”)。收集气体时,E的瓶口朝上的主要原因是______ 。
(5)完成上述实验后,除去玻璃纤维,回收D中的所有固体药品共22.76g。使该固体与过量的水充分反应,假定该反应生成的气体共224mL(标准状况)。据此计算,实验中与 反应的
反应的 的物质的量为
的物质的量为______ mol。
 是重要的供氧剂。图所示装置(省略夹持部件)用于验证
是重要的供氧剂。图所示装置(省略夹持部件)用于验证 和
和 的反应,所需
的反应,所需 由
由 固体与稀盐酸反应制备。回答下列问题:
固体与稀盐酸反应制备。回答下列问题:
(2)验证装置的气密性时,需用F替换装置中的E。若装置气密性良好,应观察到F中的导管口会有
(3)装置中的B与C用于除去
 气体中的杂质。饱和
气体中的杂质。饱和 溶液的作用是吸收
溶液的作用是吸收 气体,C中盛放的试剂是足量的
气体,C中盛放的试剂是足量的(4)实验过程中,D中部分
 固体由淡黄色变为
固体由淡黄色变为(5)完成上述实验后,除去玻璃纤维,回收D中的所有固体药品共22.76g。使该固体与过量的水充分反应,假定该反应生成的气体共224mL(标准状况)。据此计算,实验中与
 反应的
反应的 的物质的量为
的物质的量为
您最近一年使用:0次
解题方法
8 . 配制100mL0.50mol/L 溶液时,下列各图所表示的操作中,正确的是
溶液时,下列各图所表示的操作中,正确的是
 溶液时,下列各图所表示的操作中,正确的是
溶液时,下列各图所表示的操作中,正确的是A. | B. | C.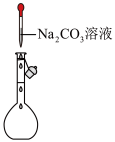 | D.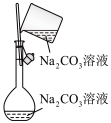 |
您最近一年使用:0次
9 . 硫及其化合物广泛存在于自然界中,硫的部分化合物相互转化关系如图所示。回答下列问题: 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化______ (填图中的序号),由该反应推断。 属于
属于______ (填“酸性”或“碱性”)氧化物。
(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明 具有
具有______ (填“氧化性”或“还原性”)。
(3) 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成______ (填化学式)和 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中 被Cu
被Cu______ (填“氧化”或“还原”)成 。
。 能使
能使______ (填试剂名称)溶液褪色,说明 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。
(5)为检验Cu与浓硫酸反应后溶液中的 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴______ (填化学式)溶液,振荡,生成______ 色沉淀,则证明溶液中含有 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为______ 。
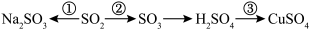
 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化 属于
属于(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明
 具有
具有(3)
 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中
 被Cu
被Cu 。
。 能使
能使 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。(5)为检验Cu与浓硫酸反应后溶液中的
 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为
您最近一年使用:0次
解题方法
10 . 半导体元器件中含晶体硅。据图硅原子结构示意图判断,下列说法不正确 的是
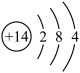
| A.核电荷数为14 | B.电子层数为2 | C.最外层电子数为4 | D. 表示硅原子核 表示硅原子核 |
您最近一年使用:0次



