真题
名校
1 . 如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期元素,基态X原子的核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q是ds区元素,焰色试验呈绿色。下列说法错误的是


A.单质沸点: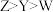 | B.简单氢化物键角: |
| C.反应过程中有蓝色沉淀产生 | D. 是配合物,配位原子是Y 是配合物,配位原子是Y |
您最近一年使用:0次
昨日更新
|
2037次组卷
|
5卷引用:2024年吉林省高考化学试题
2024年吉林省高考化学试题2024年黑龙江省高考化学试卷2024年辽宁省高考化学试卷(已下线)2024年高考化学真题完全解读(黑龙江、吉林、辽宁卷)(课件+讲义)山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高二下学期第三次月考化学试题
名校
2 . 按照要求填空
(1)现有下列各组物质:① 和
和 、②
、②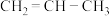 和
和 、③
、③ 和
和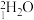 、④
、④ 和
和 、⑤
、⑤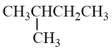 和
和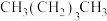 、⑥
、⑥ 和
和 、⑦
、⑦ 和
和
属于同系物的是___________ (填序号)。
(2)把下列物质的沸点按由高到低的顺序排列___________ 。(填入编号)
①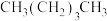 ②
②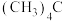 ③十一烷④
③十一烷④
(3)戊烷的同分异构体有___________ 种
(4)已知乳酸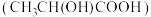 是身体代谢产物之一,该物质所含官能团的名称
是身体代谢产物之一,该物质所含官能团的名称___________ 。 乳酸分别与足量
乳酸分别与足量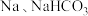 反应产生气体体积之比为:
反应产生气体体积之比为:___________ 。
(5)某有机物的键线式为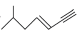 该分子最多有
该分子最多有___________ 个碳原子共面,最多有___________ 个碳原子共线。
(1)现有下列各组物质:①
 和
和 、②
、②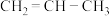 和
和 、③
、③ 和
和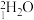 、④
、④ 和
和 、⑤
、⑤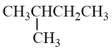 和
和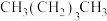 、⑥
、⑥ 和
和 、⑦
、⑦ 和
和
属于同系物的是
(2)把下列物质的沸点按由高到低的顺序排列
①
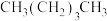 ②
②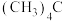 ③十一烷④
③十一烷④
(3)戊烷的同分异构体有
(4)已知乳酸
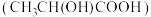 是身体代谢产物之一,该物质所含官能团的名称
是身体代谢产物之一,该物质所含官能团的名称 乳酸分别与足量
乳酸分别与足量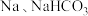 反应产生气体体积之比为:
反应产生气体体积之比为:(5)某有机物的键线式为
 该分子最多有
该分子最多有
您最近一年使用:0次
名校
解题方法
3 . 化合物G(丙酸异丙酯)可用作食品香料。现可通过下列转化制取(部分反应条件略去):___________ 。
(2)写出B→C的化学方程式___________ 。
(3)A→E是加成反应,写出该反应的化学方程式___________ 。
(4)写出D+F→G的化学方程式___________ 。
(5)G的同分异构体中能与碳酸氢钠溶液反应产生CO2的共有___________ 种。
(6)F的同分异构体中能被催化氧化成醛的是___________ (写出结构简式)。
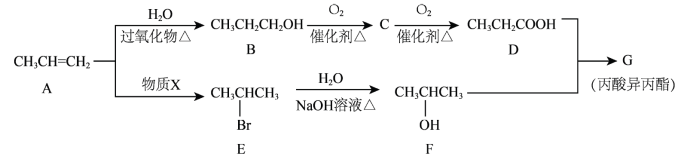
(2)写出B→C的化学方程式
(3)A→E是加成反应,写出该反应的化学方程式
(4)写出D+F→G的化学方程式
(5)G的同分异构体中能与碳酸氢钠溶液反应产生CO2的共有
(6)F的同分异构体中能被催化氧化成醛的是
您最近一年使用:0次
名校
解题方法
4 . 科学家利用氧化锆锌作催化剂,在一定温度下将CO2和H2转化为重要有机原料甲醇(CH3OH),其原理为: (即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题:
(即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题:
___________ 。
(2)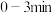 内,H2的反应速率为
内,H2的反应速率为___________ 。
(3)下列叙述正确的是___________ 。
a. 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率
b.由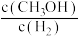 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态
c.当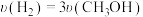 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态
d.当CO2的体积分数不再变化,可判断该反应达到平衡状态
(4)该温度下达到平衡,此时体系压强与开始时的压强之比为___________ 。
(5)其他条件不变时,下列措施不能使生成CH3OH的反应速率增大的是___________ (填序号)。
a.增大CO2的浓度 b.将容器的容积变为4L
c.恒容条件下充入一定量Ne d.将恒温恒容容器改为绝热恒容容器
(6)CH4燃料电池的工作原理如图所示,a、b均为铂电极,A、B为燃料或氧气入口。_______ 。
 (即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题:
(即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题: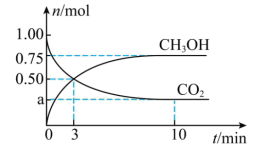

(2)
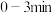 内,H2的反应速率为
内,H2的反应速率为(3)下列叙述正确的是
a.
 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率b.由
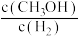 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态c.当
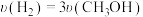 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态d.当CO2的体积分数不再变化,可判断该反应达到平衡状态
(4)该温度下达到平衡,此时体系压强与开始时的压强之比为
(5)其他条件不变时,下列措施不能使生成CH3OH的反应速率增大的是
a.增大CO2的浓度 b.将容器的容积变为4L
c.恒容条件下充入一定量Ne d.将恒温恒容容器改为绝热恒容容器
(6)CH4燃料电池的工作原理如图所示,a、b均为铂电极,A、B为燃料或氧气入口。

您最近一年使用:0次
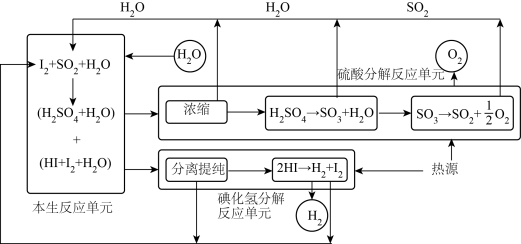
5 . 热化学硫碘循环制氢是目前最有前景的制氢方法之一,以太阳能为热源的一种制氢方法流程如图所示。
反应I: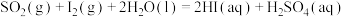
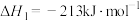
反应II: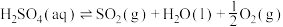
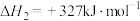
反应III: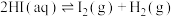
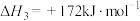
下列说法错误的是
反应I:
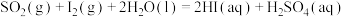
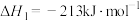
反应II:
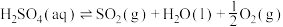
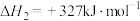
反应III:
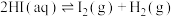
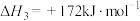
下列说法错误的是
A.整个设备不宜采用铁质材料,原因是 及HI对铁质设备有很强的腐蚀性 及HI对铁质设备有很强的腐蚀性 |
| B.反应I有非极性键的断裂与形成 |
| C.采用高压条件可以提高反应I的反应速率 |
D.总反应的热化学方程式为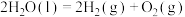 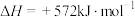 |
您最近一年使用:0次
2024·黑龙江吉林·模拟预测
6 . 我国科学家提出的聚集诱导发光机制已成为研究热点之一。一种具有聚集诱导发光性能的物质,其分子结构如图。下列说法错误的是
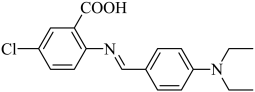
| A.分子中碳原子有sp2、sp3两种杂化轨道类型 | B.该物质既有酸性又有碱性 |
| C.该物质可发生取代反应、加成反应、氧化反应 | D.该分子不存在立体异构 |
您最近一年使用:0次
名校
7 . 工业上以有机物a、一氧化碳和乙醇为原料催化合成有机物d的反应机理如图所示,下列有关叙述正确的是
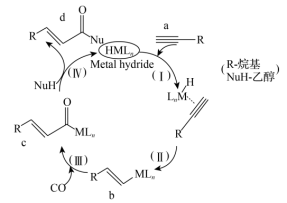
| A.a、b、c、d均存在顺反异构 |
| B.该反应的催化剂为NuH |
| C.反应(Ⅳ)是生成酮的取代反应 |
D.总反应式为  |
您最近一年使用:0次
解题方法
8 . 由下列实验操作及现象,能得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在试管中加入少量淀粉和适量稀硫酸,加热一段时间,冷却后加入 溶液 溶液 | 溶液变蓝 | 淀粉未发生水解 |
| B | 往溴的 溶液中加入牛油 溶液中加入牛油 | 溴的 溶液不褪色 溶液不褪色 | 油脂都不含有碳碳双键 |
| C | 向鸡蛋清溶液中加入醋酸铅溶液,后又加入足量的水 | 先出现白色沉淀,加水后沉淀不溶解 | 蛋白质与醋酸铅发生了化学反应 |
| D | 往硅酸钠溶液中滴加醋酸 | 溶液变浑浊 | 非金属性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 下列反应的离子方程式书写正确的是
A.硫酸氢铵溶液与足量氢氧化钠溶液混合: |
B.氢氧化亚铁与稀硝酸反应: |
C. 溶液与过量小苏打溶液反应: 溶液与过量小苏打溶液反应: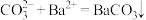 |
D.少量的过氧化钠与稀硫酸反应: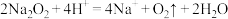 |
您最近一年使用:0次
10 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.22.4L  含有的原子总数为3 含有的原子总数为3 |
B.11.2g  含有的原子总数为0.8 含有的原子总数为0.8 |
C.常温下,将2.7g铝片投入浓硝酸中,转移电子总数为0.3 |
D.5.6g铁粉与足量硫粉反应,转移电子总数为0.3 |
您最近一年使用:0次



