名校
解题方法
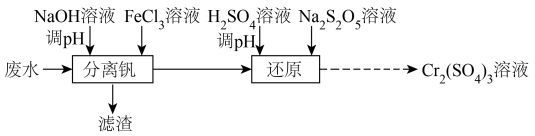
1 . 铬和钒具有广泛用途。从含高价钒(V)、铬(VI)废水中提取铬和钒的一种流程如下图所示: 调节溶液
调节溶液 ,钒(V)主要以
,钒(V)主要以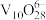 存在,再用
存在,再用 溶液沉钒得到钒铁共沉淀物。
溶液沉钒得到钒铁共沉淀物。
①如果用 调节溶液
调节溶液 ,调节
,调节 时就开始发生“沉钒”的原因是
时就开始发生“沉钒”的原因是________ 。
②图1表示 时不同铁钒摩尔比条件下对钒去除率的影响。当铁钒摩尔比大于2时,钒去除率会再次增大、但增加幅度趋缓,其原因是
时不同铁钒摩尔比条件下对钒去除率的影响。当铁钒摩尔比大于2时,钒去除率会再次增大、但增加幅度趋缓,其原因是________ 。 调节溶液
调节溶液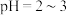 ,
,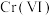 以
以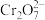 ,存在,再加入
,存在,再加入 溶液还原。写出
溶液还原。写出 还原
还原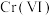 的离子方程式
的离子方程式________ 。
(3)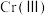 的存在形态的物质的量分数随溶液
的存在形态的物质的量分数随溶液 的分布如图2所示。请补充完整由
的分布如图2所示。请补充完整由 溶液制得
溶液制得 的实验方案:取分离、提纯得到的
的实验方案:取分离、提纯得到的 溶液,
溶液,________ ,低温烘干,得到高纯 晶体。(实验中须使用的试剂:蒸馏水、
晶体。(实验中须使用的试剂:蒸馏水、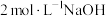 溶液、
溶液、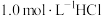 溶液、
溶液、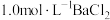 溶液)
溶液) 中有效氯含量的原理为:
中有效氯含量的原理为: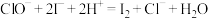 ;
; 。该实验方案:取
。该实验方案:取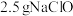 样品配制成
样品配制成 溶液,取
溶液,取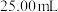 待测液于碘量瓶中,加入
待测液于碘量瓶中,加入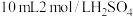 溶液和过量
溶液和过量 溶液,密封在暗处静置
溶液,密封在暗处静置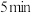 ;用
;用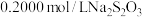 溶液滴定至溶液呈微黄色,加入2~3滴淀粉溶液,继续滴定至终点,平行滴定三次,平均消耗
溶液滴定至溶液呈微黄色,加入2~3滴淀粉溶液,继续滴定至终点,平行滴定三次,平均消耗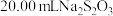 溶液。该
溶液。该 样品中有效氯含量为
样品中有效氯含量为________ 。(写出计算过程,该样品的有效氯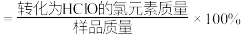 )
)
 调节溶液
调节溶液 ,钒(V)主要以
,钒(V)主要以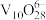 存在,再用
存在,再用 溶液沉钒得到钒铁共沉淀物。
溶液沉钒得到钒铁共沉淀物。①如果用
 调节溶液
调节溶液 ,调节
,调节 时就开始发生“沉钒”的原因是
时就开始发生“沉钒”的原因是②图1表示
 时不同铁钒摩尔比条件下对钒去除率的影响。当铁钒摩尔比大于2时,钒去除率会再次增大、但增加幅度趋缓,其原因是
时不同铁钒摩尔比条件下对钒去除率的影响。当铁钒摩尔比大于2时,钒去除率会再次增大、但增加幅度趋缓,其原因是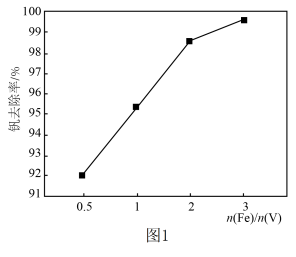
 调节溶液
调节溶液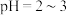 ,
,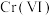 以
以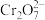 ,存在,再加入
,存在,再加入 溶液还原。写出
溶液还原。写出 还原
还原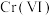 的离子方程式
的离子方程式(3)
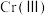 的存在形态的物质的量分数随溶液
的存在形态的物质的量分数随溶液 的分布如图2所示。请补充完整由
的分布如图2所示。请补充完整由 溶液制得
溶液制得 的实验方案:取分离、提纯得到的
的实验方案:取分离、提纯得到的 溶液,
溶液, 晶体。(实验中须使用的试剂:蒸馏水、
晶体。(实验中须使用的试剂:蒸馏水、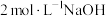 溶液、
溶液、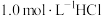 溶液、
溶液、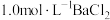 溶液)
溶液)
 中有效氯含量的原理为:
中有效氯含量的原理为: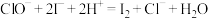 ;
; 。该实验方案:取
。该实验方案:取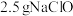 样品配制成
样品配制成 溶液,取
溶液,取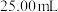 待测液于碘量瓶中,加入
待测液于碘量瓶中,加入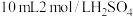 溶液和过量
溶液和过量 溶液,密封在暗处静置
溶液,密封在暗处静置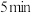 ;用
;用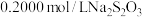 溶液滴定至溶液呈微黄色,加入2~3滴淀粉溶液,继续滴定至终点,平行滴定三次,平均消耗
溶液滴定至溶液呈微黄色,加入2~3滴淀粉溶液,继续滴定至终点,平行滴定三次,平均消耗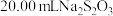 溶液。该
溶液。该 样品中有效氯含量为
样品中有效氯含量为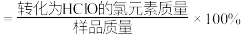 )
)
您最近一年使用:0次
解题方法
2 . 根据要求,回答下列问题:
(1)为了测定某有机物A的结构,进行如下实验:
a.将2.3 g该有机物完全燃烧,生成0.1mol 和27g水;
和27g水;
b.用质谱仪测定其相对分子质量,得到如图所示的质谱图。___________ 。
②有机物A的实验式是___________ 。
(2)有机物的结构可用“键线式”简化表示,例如: 可简写为
可简写为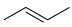 。有机物X的键线式为
。有机物X的键线式为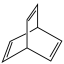 。
。
①有机物Y是X的同分异构体,则Y属于芳香烃的键线式为___________ 。
②X与足量的 在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有
在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有___________ 种,写出其中任意一种的键线式:___________ 。
(1)为了测定某有机物A的结构,进行如下实验:
a.将2.3 g该有机物完全燃烧,生成0.1mol
 和27g水;
和27g水;b.用质谱仪测定其相对分子质量,得到如图所示的质谱图。

②有机物A的实验式是
(2)有机物的结构可用“键线式”简化表示,例如:
 可简写为
可简写为 。有机物X的键线式为
。有机物X的键线式为 。
。①有机物Y是X的同分异构体,则Y属于芳香烃的键线式为
②X与足量的
 在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有
在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有③由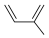 以及必要的无机试剂可合成
以及必要的无机试剂可合成 ,写出第一步合成反应的化学方程式:
,写出第一步合成反应的化学方程式:
④双烯合成反应(即Diels-Alder反应)是由二烯烃与单烯烃或炔烃合成六元环状化合物的重要反应,例如,1,3-丁二烯与乙烯的作用可表示为: ,则由1-丁烯和2-乙基-1,3-丁二烯发生双烯合成反应的产物为
,则由1-丁烯和2-乙基-1,3-丁二烯发生双烯合成反应的产物为
您最近一年使用:0次
3 . 除去下列物质中所含有的少量杂质(括号内为杂质),所选用的试剂和分离方法均正确的是
| 选项 | 混合物 | 试剂 | 分离方法 |
| A | 粗苯甲酸(氯化钠) | 水 | 重结晶 |
| B | 乙烷(乙烯) | 氢气(Ni作催化剂) | 加热 |
| C | 乙酸(水) | 生石灰 | 蒸馏 |
| D | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 有机物的世界很丰富,种类和数目非常庞大,认识简单的有机物是我们学习有机化学的开始。回答下列问题:
(1)有下列几组物质:① 与
与 ;②乙醇和二甲醚(CH3OCH3);③乙二醇(
;②乙醇和二甲醚(CH3OCH3);③乙二醇( )与丙三醇(
)与丙三醇( );④
);④ 和
和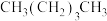 ;⑤CH2=CHCH3和CH2=CH2。
;⑤CH2=CHCH3和CH2=CH2。
①第②组物质中含有的官能团名称为___________ ;上述物质中不属于同分异构体的有___________ (填序号);
②CH3(CH2)3CH3的一氯取代物有___________ 种。
(2)乙酸与乙醇在浓硫酸、加热条件下发生酯化反应的化学方程式为___________ ,根据乙酸与乙醇发生酯化反应的原理,说明乙醇分子结构中极性较大的共价键是___________ 键。
(3)邻二氯苯和间二氯苯属于有机化合物构造异构中的___________ 异构(填“碳架”“位置”或“官能团”)。
(4)类比甲烷,乙烷与Cl2在光照条件下也能发生取代反应,写出第一步反应的化学方程式:___________ ,乙烷与足量的Cl2反应生成___________ 种产物。
(1)有下列几组物质:①
 与
与 ;②乙醇和二甲醚(CH3OCH3);③乙二醇(
;②乙醇和二甲醚(CH3OCH3);③乙二醇( )与丙三醇(
)与丙三醇( );④
);④ 和
和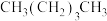 ;⑤CH2=CHCH3和CH2=CH2。
;⑤CH2=CHCH3和CH2=CH2。①第②组物质中含有的官能团名称为
②CH3(CH2)3CH3的一氯取代物有
(2)乙酸与乙醇在浓硫酸、加热条件下发生酯化反应的化学方程式为
(3)邻二氯苯和间二氯苯属于有机化合物构造异构中的
(4)类比甲烷,乙烷与Cl2在光照条件下也能发生取代反应,写出第一步反应的化学方程式:
您最近一年使用:0次
5 . 下列物质的性质与用途具有对应关系的是
A. 溶液呈酸性,可用于腐蚀电路板上的Cu 溶液呈酸性,可用于腐蚀电路板上的Cu |
B. 易溶于水,可用作工业电解制备单质镁 易溶于水,可用作工业电解制备单质镁 |
C.浓 具有脱水性,可用作实验室干燥 具有脱水性,可用作实验室干燥 气体的干燥剂 气体的干燥剂 |
| D.等离子体含有能自由移动的带电粒子,可应用于化学合成和材料表面改性 |
您最近一年使用:0次
7日内更新
|
75次组卷
|
3卷引用:2024届甘肃省民乐县第一中学高三下学期5月模拟考试化学试卷
6 . 有关下列实验装置的说法正确的是
|
|
| ① | ② |
|
|
| ③ | ④ |
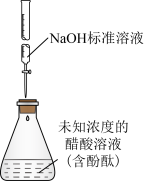
| A.装置①用于测定醋酸的浓度 |
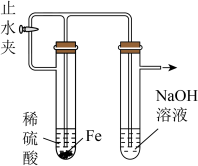
B.装置②用于 的制备,反应一开始就要关闭止水夹,让生成的氢气把左边试管中液体压入右边,以实现自动化控制 的制备,反应一开始就要关闭止水夹,让生成的氢气把左边试管中液体压入右边,以实现自动化控制 |
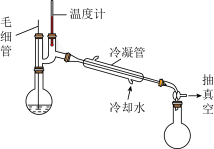
| C.装置③是减压蒸馏,减压条件下可以降低混合组分的熔沸点 |
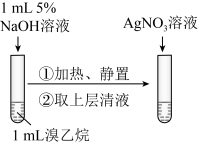
D.装置④可用于检验溴乙烷的水解产物 |
您最近一年使用:0次
解题方法
7 . 宏观辨识与微观探析是化学学科核心素养之一。常温下,下列各组粒子在指定溶液中能大量共存的是
A.0.1 mol⋅L 碳酸钠溶液( 碳酸钠溶液( )中: )中: 、 、 、 、 |
B.加入苯酚显紫色的溶液中能大量共存的离子: 、 、 、 、 、 、 |
C.0.1 mol⋅L 酸性 酸性 溶液中: 溶液中: 、 、 、 、 、 、 |
D.常温下 mol⋅L mol⋅L 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
8 . 我国科学家将聚酰亚胺(组成元素为H、C、N、O等)介电聚合物与高绝缘纳米氧化镁(MgO)填料混合,成功制得聚酰亚胺/纳米氧化镁复合材料。该复合材料特点为具有高击穿强度、宽温度范围和低介电损耗。结合所学知识,回答下列问题。
(1)基态Mg原子的电子排布式为_________ 。
(2)C、N、O第一电离能由大到小的顺序为_________ ;C、N、O电负性由大到小的顺序为_________ ,理由是________________ 。
(3) 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为_________ ; 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是__________ ; 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是________ 。
(1)基态Mg原子的电子排布式为
(2)C、N、O第一电离能由大到小的顺序为
(3)
 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。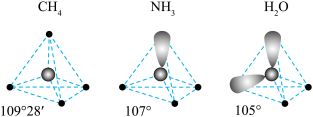
 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是
您最近一年使用:0次
名校
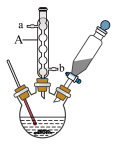
9 . 苯甲酸是一种重要原料。实验室可以用甲苯与高锰酸钾反应制得苯甲酸,反应装置图和有关数据如下:
合成步骤如下:
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时再迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
(1)仪器A的名称是____________ ,它的作用是____________ 。
(2)加入碎瓷片的作用是____________ 。
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为________________________ 。
(4)若得到的苯甲酸晶体产品不纯,则采用____________ 方法可得到纯度更高的产品。
(5)下列有关苯甲酸重结晶实验的说法正确的是_________ (填字母)。
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是____________ (保留一位小数)。
物质 | 熔点/℃ | 沸点/℃ | 水中溶解度/g(25℃) | 相对分子质量 | 密度/( |
甲苯 |
| 110.6 | 难溶 | 92 | 0.85 |
苯甲酸 | 122.13 | 249 | 0.344 | 122 | 1.27 |
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时再迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
已知: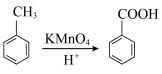 。
。
(1)仪器A的名称是
(2)加入碎瓷片的作用是
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为
(4)若得到的苯甲酸晶体产品不纯,则采用
(5)下列有关苯甲酸重结晶实验的说法正确的是
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是
您最近一年使用:0次
名校
10 . 非金属单质A经下图所示的过程可转化为含氧酸D,已知D为强酸。请回答下列问题.

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体;
①D的化学式为______________ ;
②在工业生产中,B气体大量排放,被雨水吸收后形成的______________ 会污染环境;
③98.3%的D溶液是常见的气体干燥剂,但它不能干燥 和
和 ,原因是
,原因是______________ ;
(2)若A在常温下为气体,C是红棕色的气体;
①A、C的化学式分别为_________ 、___________ ;
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为________ ,该反应_______ (填“属于”或“不属于”)氧化还原反应;
③工业上利用氨制备D,写出氨被催化氧化生成B气体的化学方程式:____________ 。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体;
①D的化学式为
②在工业生产中,B气体大量排放,被雨水吸收后形成的
③98.3%的D溶液是常见的气体干燥剂,但它不能干燥
 和
和 ,原因是
,原因是(2)若A在常温下为气体,C是红棕色的气体;
①A、C的化学式分别为
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为
③工业上利用氨制备D,写出氨被催化氧化生成B气体的化学方程式:
您最近一年使用:0次

 )
)