1 . Ⅰ、向某容积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答下列问题:_______ L。
(2)若t1=15s,则0~t1阶段以C物质浓度变化表示的反应速率为v(C)=_______ 。
(3)写出反应的化学方程式:_______ 。
(4)B的起始物质的量是_______ 。
(5)判断该反应达到平衡状态的依据是_______。
Ⅱ、如图为原电池装置示意图。_______ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式_______ 。
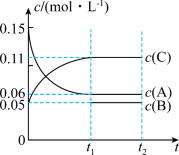
(2)若t1=15s,则0~t1阶段以C物质浓度变化表示的反应速率为v(C)=
(3)写出反应的化学方程式:
(4)B的起始物质的量是
(5)判断该反应达到平衡状态的依据是_______。
| A.t2时,正、逆反应速率均为零 | B.混合气体的密度不再变化 |
| C.vA∶vB∶vC=3∶1∶2 | D.t2时,cA=0.06mol·L-1,并保持不变 |
Ⅱ、如图为原电池装置示意图。
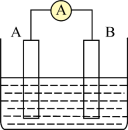
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式
您最近一年使用:0次
2 . 对于300mL 1mol·L-I盐酸与少量铁粉的反应,采取下列措施:①升高温度;②加几滴浓硫酸;③再加300mL 1mol·L-1盐酸;④滴入几滴硫酸铜溶液;⑤加入少量醋酸钠固体。其中能使反应速率加快且不改变生成H2总量的是
| A.①② | B.①③④ | C.①②③④ | D.①②③⑤ |
您最近一年使用:0次
3 . 下列说法正确的是
A.热化学方程式未注明温度和压强时, 表示标准状况下的数据 表示标准状况下的数据 |
| B.H2(g) + Cl2(g) = 2HCl(g) 在光照或点燃条件下反应的ΔH不同 |
| C.一个化学反应都有且只有一个相对应的焓变 |
| D.可逆反应的正反应和逆反应的焓变:ΔH正=-ΔH逆 |
您最近一年使用:0次
4 . 2023年10月26日,“神舟十七号”载人飞船发射成功,火箭推进过程中发生反应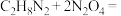
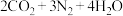 。已知
。已知 中
中 为-3价,则下列说法正确的是
为-3价,则下列说法正确的是
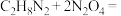
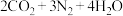 。已知
。已知 中
中 为-3价,则下列说法正确的是
为-3价,则下列说法正确的是A.氧化性: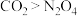 | B.该反应中 为还原产物 为还原产物 |
C.生成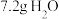 时,转移电子 时,转移电子 | D.氧化产物与还原产物的物质的量之比为2:3 |
您最近一年使用:0次
解题方法
5 . Ⅰ.已知 具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质:
具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质: 、
、 (难溶盐)、
(难溶盐)、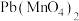 (强电解质)、
(强电解质)、 、X(水溶液呈无色)、
、X(水溶液呈无色)、 ,已知X是一种盐,且
,已知X是一种盐,且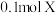 在该反应中失去
在该反应中失去 个电子。
个电子。
(1)写出X的化学式:_______ 。
(2)若有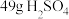 参加反应,则转移电子的物质的量为
参加反应,则转移电子的物质的量为_______ mol。
Ⅱ.二氧化氯 具有强氧化性,是国际公认的高效消毒灭菌剂。
具有强氧化性,是国际公认的高效消毒灭菌剂。 可用于水体中
可用于水体中 的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得
的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得 浓度随反应时间的变化如图所示。
浓度随反应时间的变化如图所示。 时水体中
时水体中 转化为
转化为 ,
, 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(4)反应相同时间,水体中 浓度随pH增大而降低的原因是
浓度随pH增大而降低的原因是_______ 。
(5) 在杀菌消毒过程中会产生亚氯酸盐
在杀菌消毒过程中会产生亚氯酸盐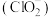 ,需将其转化为
,需将其转化为 除去,下列试剂可将
除去,下列试剂可将 转化为
转化为 的是_______(填标号)。
的是_______(填标号)。
(6) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_______ g。(计算结果保留两位小数)
Ⅲ.向 溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入
溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入 的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中
的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中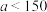 )
) 溶液的物质的量浓度为
溶液的物质的量浓度为_______ ,通入 后所得溶液的溶质物质的量之比为
后所得溶液的溶质物质的量之比为_______ (用含a的表达式表示)。
 具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质:
具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质: 、
、 (难溶盐)、
(难溶盐)、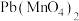 (强电解质)、
(强电解质)、 、X(水溶液呈无色)、
、X(水溶液呈无色)、 ,已知X是一种盐,且
,已知X是一种盐,且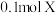 在该反应中失去
在该反应中失去 个电子。
个电子。(1)写出X的化学式:
(2)若有
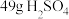 参加反应,则转移电子的物质的量为
参加反应,则转移电子的物质的量为Ⅱ.二氧化氯
 具有强氧化性,是国际公认的高效消毒灭菌剂。
具有强氧化性,是国际公认的高效消毒灭菌剂。 可用于水体中
可用于水体中 的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得
的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得 浓度随反应时间的变化如图所示。
浓度随反应时间的变化如图所示。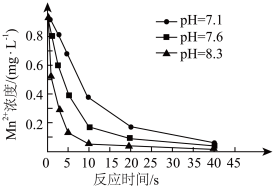
 时水体中
时水体中 转化为
转化为 ,
, 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为(4)反应相同时间,水体中
 浓度随pH增大而降低的原因是
浓度随pH增大而降低的原因是(5)
 在杀菌消毒过程中会产生亚氯酸盐
在杀菌消毒过程中会产生亚氯酸盐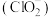 ,需将其转化为
,需将其转化为 除去,下列试剂可将
除去,下列试剂可将 转化为
转化为 的是_______(填标号)。
的是_______(填标号)。A. | B. | C. | D. |
(6) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为Ⅲ.向
 溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入
溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入 的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中
的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中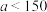 )
)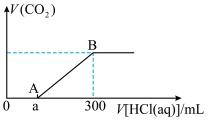
 溶液的物质的量浓度为
溶液的物质的量浓度为 后所得溶液的溶质物质的量之比为
后所得溶液的溶质物质的量之比为
您最近一年使用:0次
6 . 下列选项描述与对应图像不相符的是
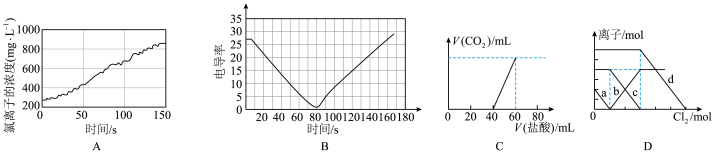
A.图A为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图B向某浓度的 溶液中滴入稀 溶液中滴入稀 ,溶液电导率随时间变化的曲线 ,溶液电导率随时间变化的曲线 |
C.图C为向等物质的量浓度的 、 、 混合液中滴加盐酸产生 混合液中滴加盐酸产生 的图像 的图像 |
D.图D为 、 、 混合液,各离子物质的量随氯气通入的变化图像,b代表的是 混合液,各离子物质的量随氯气通入的变化图像,b代表的是 |
您最近一年使用:0次
7 . 某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了如图装置进行实验。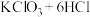 (浓)
(浓) ;
;
②石灰乳的主要成分为 ,其他杂质不参与反应。但反应放热会发生副反应:
,其他杂质不参与反应。但反应放热会发生副反应: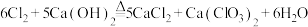
请回答下列问题:
(1)A反应中体现了浓盐酸的还原性和_______ 性,其中还原产物和氧化产物的物质的量之比为_______ 。
(2)装置B的作用:_______ 。
(3)装置C的实验目的是验证干燥和湿润的氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质正确的是_______(填标号)。
(4)制取漂白粉的化学方程式为_______ 。
(5)为提高产品中有效成分 的含量,在不改变石灰乳浓度和体积的条件下可采取的措施是
的含量,在不改变石灰乳浓度和体积的条件下可采取的措施是_______ (答案合理即可)。一定温度下将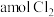 通入过量的石灰乳中充分反应,生成
通入过量的石灰乳中充分反应,生成 、
、 、
、 的混合物,且产物的成分含量与温度的高低有关。反应中转移电子的物质的量
的混合物,且产物的成分含量与温度的高低有关。反应中转移电子的物质的量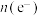 的范围为
的范围为_______ 。
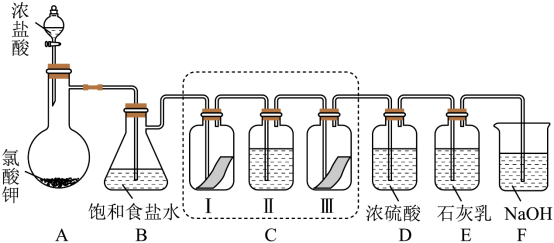
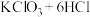 (浓)
(浓)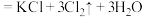 ;
;②石灰乳的主要成分为
 ,其他杂质不参与反应。但反应放热会发生副反应:
,其他杂质不参与反应。但反应放热会发生副反应: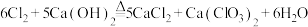
请回答下列问题:
(1)A反应中体现了浓盐酸的还原性和
(2)装置B的作用:
(3)装置C的实验目的是验证干燥和湿润的氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质正确的是_______(填标号)。
| Ⅰ | Ⅱ | Ⅲ | |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
| C | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
| D | 湿润的有色布条' | 浓硫酸 | 干燥的有色布条 |
| A.A | B.B | C.C | D.D |
(5)为提高产品中有效成分
 的含量,在不改变石灰乳浓度和体积的条件下可采取的措施是
的含量,在不改变石灰乳浓度和体积的条件下可采取的措施是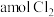 通入过量的石灰乳中充分反应,生成
通入过量的石灰乳中充分反应,生成 、
、 、
、 的混合物,且产物的成分含量与温度的高低有关。反应中转移电子的物质的量
的混合物,且产物的成分含量与温度的高低有关。反应中转移电子的物质的量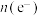 的范围为
的范围为
您最近一年使用:0次
解题方法
8 . 纳米铁是一种黑色粉末,可用于制作高密度磁性材料。以铁屑(含少量 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下: 是一种二元弱酸。
是一种二元弱酸。
(1)取少量产品分散于水中,用红色激光笔照射此液体,若出现_______ (填实验现象),可验证所得铁粉直径为纳米级。
(2)写出 与少量
与少量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(3)写出“酸溶”时氧化还原反应的离子方程式:_______ 、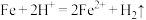 。
。
(4) 固体灼烧操作所需的硅酸盐质仪器包括:玻璃棒、酒精灯、泥三角、
固体灼烧操作所需的硅酸盐质仪器包括:玻璃棒、酒精灯、泥三角、_______ ;经灼烧后得到红棕色固体和CO、 混合气体,若产物中
混合气体,若产物中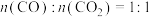 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为_______ 。
(5)纳米铁粉可用于处理含氧酸性废水中的 ,反应原理如图所示。
,反应原理如图所示。_______ 性(填“氧化”或“还原”)。
②该过程中生成 的离子方程式为
的离子方程式为_______ ,在铁粉总量一定的条件下,废水中的溶解氧过多不利于 的去除,原因是
的去除,原因是_______ 。
 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下: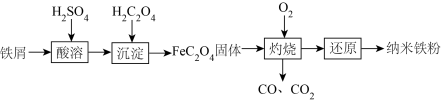
 是一种二元弱酸。
是一种二元弱酸。(1)取少量产品分散于水中,用红色激光笔照射此液体,若出现
(2)写出
 与少量
与少量 溶液反应的离子方程式
溶液反应的离子方程式(3)写出“酸溶”时氧化还原反应的离子方程式:
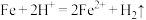 。
。(4)
 固体灼烧操作所需的硅酸盐质仪器包括:玻璃棒、酒精灯、泥三角、
固体灼烧操作所需的硅酸盐质仪器包括:玻璃棒、酒精灯、泥三角、 混合气体,若产物中
混合气体,若产物中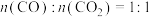 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为(5)纳米铁粉可用于处理含氧酸性废水中的
 ,反应原理如图所示。
,反应原理如图所示。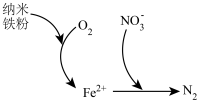
②该过程中生成
 的离子方程式为
的离子方程式为 的去除,原因是
的去除,原因是
您最近一年使用:0次
9 . A、B、C、D、E为常见的主族元素,根据下表信息回答问题。
(1)写出A单质溶于 溶液的化学方程式
溶液的化学方程式_______ 。
(2)比较A、B最高价氧化物对应水化物的碱性强弱_______ (用化学式表示)。
(3)用电子式表示B和D形成化合物的过程:_______ 。
(4)元素E在周期表中的位置_______ ,关于元素D、E非金属性强弱的判断不正确的是_______ (填标号)。
a.D、E与 反应D更容易
反应D更容易
b.D的单质可与E的钠盐水溶液发生置换反应
c.最高价氧化物对应水化物的酸性:E>D
d.气态氢化物稳定性:D>E
(5)R的原子序数比C大,且与C处于相邻周期同一主族,关于元素R及其化合物的有关说法正确的是_______(填标号)。
| 元素 | 元素性质或原子结构信息 |
| A | A元素是地壳中含量最多的金属元素 |
| B | B元素的原子失去2个电子,所得到的微粒具有与氖原子相同的电子层结构 |
| C | C元素原子核外M层比L层少2个电子 |
| D | 与A同周期,化合价有 , , 价等 价等 |
| E | 原子结构示意图: |
(1)写出A单质溶于
 溶液的化学方程式
溶液的化学方程式(2)比较A、B最高价氧化物对应水化物的碱性强弱
(3)用电子式表示B和D形成化合物的过程:
(4)元素E在周期表中的位置
a.D、E与
 反应D更容易
反应D更容易b.D的单质可与E的钠盐水溶液发生置换反应
c.最高价氧化物对应水化物的酸性:E>D
d.气态氢化物稳定性:D>E
(5)R的原子序数比C大,且与C处于相邻周期同一主族,关于元素R及其化合物的有关说法正确的是_______(填标号)。
| A.R原子的半径比C原子的大 |
B. 的稳定性比 的稳定性比 的强 的强 |
C. 能与 能与 溶液反应 溶液反应 |
D.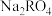 可以使酸性高锰酸钾溶液褪色 可以使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
解题方法
10 . 现有Fe和 的固体粉末
的固体粉末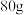 ,往其中加入
,往其中加入 稀硫酸,固体粉末全部溶解,产生
稀硫酸,固体粉末全部溶解,产生 的体积为
的体积为 (标准状况),反应后的溶液不能使
(标准状况),反应后的溶液不能使 溶液显色。为中和过量硫酸需要
溶液显色。为中和过量硫酸需要 溶液
溶液 (忽略溶液体积变化)。下列说法不正确的是
(忽略溶液体积变化)。下列说法不正确的是
 的固体粉末
的固体粉末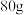 ,往其中加入
,往其中加入 稀硫酸,固体粉末全部溶解,产生
稀硫酸,固体粉末全部溶解,产生 的体积为
的体积为 (标准状况),反应后的溶液不能使
(标准状况),反应后的溶液不能使 溶液显色。为中和过量硫酸需要
溶液显色。为中和过量硫酸需要 溶液
溶液 (忽略溶液体积变化)。下列说法不正确的是
(忽略溶液体积变化)。下列说法不正确的是A.混合物中Fe的质量为 | B.与固体粉末反应的硫酸的物质的量为 |
C.原硫酸的浓度为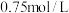 | D.混合物中 的物质的量为 的物质的量为 |
您最近一年使用:0次




