名校
1 . 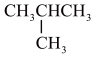 的一氯代物有
的一氯代物有 多一个碳原子的烷烃有
多一个碳原子的烷烃有
您最近一年使用:0次
名校
解题方法
2 . 化学与生活、科技发展息息相关。下列说法错误的是
| A.空间站使用石墨烯存储器,石墨烯属于新型无机非金属材料 |
| B.航天员穿的航天服中某层面料主要成分是涤纶,涤纶属于合成纤维 |
| C.我国某研究中心研发出国产“量子芯片温度计”,“芯片”的主要成分为二氧化硅 |
| D.陶瓷承载着我国悠久的历史和文化,陶瓷属于传统无机非金属材料 |
您最近一年使用:0次
名校
3 . 下列有机实验方案设计正确,且能达到预期目的的是
| 编号 | 目的 | 方案设计 |
| A | 除去乙烷中混有的少量乙烯 | 将混合气体通入盛有溴的四氯化碳溶液的洗气瓶中 |
| B | 比较水和乙醇中羟基氢活泼性强弱 | 向两支试管中分别加入2mL  和 和 水溶液,再同时向两支试管中加相同大小的金属Na,观察现象 水溶液,再同时向两支试管中加相同大小的金属Na,观察现象 |
| C | 探究淀粉是否完全水解 | 在0.5g淀粉中加入4mL 2mol/L的硫酸溶液,加热一段时间,冷却后加入NaOH溶液调至碱性,再加入少量新制 悬浊液加热,观察实验现象 悬浊液加热,观察实验现象 |
| D | 制备乙酸乙酯 | 在一支试管中加入2mL乙醇,边振荡边慢慢加入0.5mL浓硫酸和2mL乙酸,再加入几片碎瓷片。用小火加热,产生的蒸汽经导管通到饱和 溶液的上方约0.5cm处 溶液的上方约0.5cm处 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 如图为元素周期表的一部分,请参照a~h在表中的位置,回答下列问题:
(1)g在周期表中的位置是___________ 。
(2)元素d、g、h形成的简单离子中,离子半径最大的是___________ 。(填离子符号)
(3)元素c和元素f形成的化合物的化学式为___________ ,化学键为___________ 。
(4)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号。已知Te与S元素同主族。
①碲及其化合物可能具有的性质为___________ (填标号)。
A.单质Te在常温下是固体
B.H2Te比H2O稳定
C.H2TeO4的酸性比H2SO4的弱
D.Cl2通入H2Te溶液中不发生反应
E.Te元素位于周期表中第六周期
②TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。写出TeO2与过量NaOH溶液反应的离子方程式___________ 。
③工业上,把SO2通入TeCl4溶液中,可得到Te,该反应的化学方程式是___________ 。
| a | |||||||||
| b | c | d | |||||||
| e | f | g | h |
(2)元素d、g、h形成的简单离子中,离子半径最大的是
(3)元素c和元素f形成的化合物的化学式为
(4)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号。已知Te与S元素同主族。
①碲及其化合物可能具有的性质为
A.单质Te在常温下是固体
B.H2Te比H2O稳定
C.H2TeO4的酸性比H2SO4的弱
D.Cl2通入H2Te溶液中不发生反应
E.Te元素位于周期表中第六周期
②TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。写出TeO2与过量NaOH溶液反应的离子方程式
③工业上,把SO2通入TeCl4溶液中,可得到Te,该反应的化学方程式是
您最近一年使用:0次
5 . 某化学兴趣小组进行实验探究乙醇的某些性质。
I.利用如图装置(夹持装置已省略,乙、丙、丁中的装置为3V形玻璃管)探究乙醇与 的反应。实验过程中,丙处管内固体出现红黑交替的现象,实验结束后,取适量丁处管内液体于试管中,滴加适量紫色石蕊试液,溶液不变红。
的反应。实验过程中,丙处管内固体出现红黑交替的现象,实验结束后,取适量丁处管内液体于试管中,滴加适量紫色石蕊试液,溶液不变红。___________ ;丁处冷水的作用是___________ 。
(2)丙处管内发生的总反应为___________ ;丁处管内收集到的液体的成分为___________ (写结构简式或化学式)。
(3)该装置的不足之处有___________ 。
Ⅱ.利用如图装置(加热和夹持装置已省略)制备乙酸乙酯。仪器a中加入了4.0mL(约0.2mol)乙醇、4.0mL浓硫酸和5.7mL(0.1mol)醋酸。充分反应,并经过一系列分离提纯操作,最终制得6.6g乙酸乙酯。
(5)仪器a中发生反应的化学方程式为___________ ;该实验中,乙酸乙酯的产率为___________ 。
I.利用如图装置(夹持装置已省略,乙、丙、丁中的装置为3V形玻璃管)探究乙醇与
 的反应。实验过程中,丙处管内固体出现红黑交替的现象,实验结束后,取适量丁处管内液体于试管中,滴加适量紫色石蕊试液,溶液不变红。
的反应。实验过程中,丙处管内固体出现红黑交替的现象,实验结束后,取适量丁处管内液体于试管中,滴加适量紫色石蕊试液,溶液不变红。
(2)丙处管内发生的总反应为
(3)该装置的不足之处有
Ⅱ.利用如图装置(加热和夹持装置已省略)制备乙酸乙酯。仪器a中加入了4.0mL(约0.2mol)乙醇、4.0mL浓硫酸和5.7mL(0.1mol)醋酸。充分反应,并经过一系列分离提纯操作,最终制得6.6g乙酸乙酯。

| A.饱和NaCl溶液 | B.浓硫酸 |
C.饱和 溶液 溶液 | D.NaOH溶液 |
(5)仪器a中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
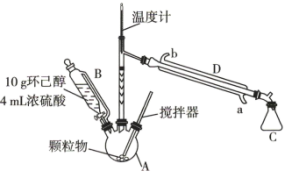
6 . 环己烯是合成赖氨酸、环己酮苯酚、聚环烯树脂等的原料,还可用作催化剂溶剂,和石油萃取剂、高辛烷值汽油稳定剂。环己烯可通过环己醇脱水得到,原理如下:
Ⅰ.环己烯粗品的制备。实验装置(加热和夹持装置已略)和步骤如下:
ⅰ.按图示连接好仪器,并进行气密性检验。
ⅱ.在干燥的仪器A中加入几粒颗粒物,再将B中液体加入到A中。
ⅲ.将仪器A在陶土网上用小火慢慢加热,并不断搅拌,控制加热速度,使分馏柱上端的温度不超过90℃,慢慢的蒸出生成的环己烯和水,直到蒸馏完全,停止蒸馏。
(1)仪器A的名称是_______ 。步骤ⅱ仪器A中放入颗粒物的作用是_______ 。
(2)装置D中冷凝水从_______ (填“a”或“b”)口进入。
(3)A中的反应液温度较高(130℃左右)时会产生副产物_______ (填结构简式)。
Ⅱ.环己烯的精制。
①将C中的蒸馏液加入精盐,然后加入3~4mL 5%的碳酸钠溶液。
②将此液体倒入分液漏斗中,振荡后静置分层……并加入1~2g无水氯化钙。
③将②中含环己烯的混合物滤入干燥的蒸馏烧瓶中进行蒸馏。
(4)步骤①中加入3~4mL5%的碳酸钠溶液的目的是_______ 。
(5)步骤②中分液的具体操作是打开分液漏斗上方的玻璃塞和下方的活塞,_______ 。
(6)若得到的产品为4.6g,则本实验中产品的产率是_______ (结果保留两位有效数字)。

物质 | 熔点/℃ | 沸点/℃ | 密度/( | 溶解性 | 相对分子质量 |
环己烯 | -103.7 | 83.0 | 0.81 | 不溶于水 | 82 |
环己醇 | 25.9 | 160.8 | 0.96 | 微溶于水 | 100 |
硫酸 | 10.4 | 337 | 1.83 | 与水互溶,能共沸产生白雾 |
ⅰ.按图示连接好仪器,并进行气密性检验。
ⅱ.在干燥的仪器A中加入几粒颗粒物,再将B中液体加入到A中。
ⅲ.将仪器A在陶土网上用小火慢慢加热,并不断搅拌,控制加热速度,使分馏柱上端的温度不超过90℃,慢慢的蒸出生成的环己烯和水,直到蒸馏完全,停止蒸馏。
(1)仪器A的名称是
(2)装置D中冷凝水从
(3)A中的反应液温度较高(130℃左右)时会产生副产物
Ⅱ.环己烯的精制。
①将C中的蒸馏液加入精盐,然后加入3~4mL 5%的碳酸钠溶液。
②将此液体倒入分液漏斗中,振荡后静置分层……并加入1~2g无水氯化钙。
③将②中含环己烯的混合物滤入干燥的蒸馏烧瓶中进行蒸馏。
(4)步骤①中加入3~4mL5%的碳酸钠溶液的目的是
(5)步骤②中分液的具体操作是打开分液漏斗上方的玻璃塞和下方的活塞,
(6)若得到的产品为4.6g,则本实验中产品的产率是
您最近一年使用:0次
名校
解题方法
7 . 下列生产生活的过程中,没有发生沉淀转化的是
| A.含氟牙膏的使用 |
B.原生铜的硫化物经氧化、淋滤变成 溶液,遇到ZnS、PbS转化为铜蓝(CuS) 溶液,遇到ZnS、PbS转化为铜蓝(CuS) |
| C.使用碳酸钠溶液处理锅炉水垢,再用盐酸洗涤 |
| D.使用热的碳酸钠溶液去除油污 |
您最近一年使用:0次
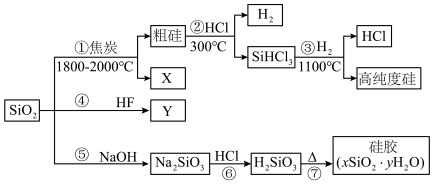
8 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。二氧化硅又称硅石,是制备硅及其化合物的重要原料,部分转化过程如图所示。回答下面问题:___________ 。可以循环使用的物质为___________ (填化学式,下同)和___________ 。
(2)光导纤维是一种良好的通讯材料,其成分是___________ (填化学式)。
(3)生产磨砂玻璃时可以用HF溶蚀玻璃,是因为HF溶液可与SiO2反应,其化学方程式为___________ 。
(4)关于硅及其相关化合物的叙述正确的是___________ (填字母)。
A.晶体硅熔点高、硬度大,故可用作半导体材料
B.玻璃、水泥、陶瓷都是传统的硅酸盐产品
C.二氧化硅是酸性氧化物,所以能溶于水且可与水反应生成硅酸
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.碳化硅是一种新型陶瓷材料,具有耐高温、耐磨的特点
(5)碳化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据氮和硅的原子结构示意图、元素周期律的知识,写出氮化硅的化学式___________ 。
(2)光导纤维是一种良好的通讯材料,其成分是
(3)生产磨砂玻璃时可以用HF溶蚀玻璃,是因为HF溶液可与SiO2反应,其化学方程式为
(4)关于硅及其相关化合物的叙述正确的是
A.晶体硅熔点高、硬度大,故可用作半导体材料
B.玻璃、水泥、陶瓷都是传统的硅酸盐产品
C.二氧化硅是酸性氧化物,所以能溶于水且可与水反应生成硅酸
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.碳化硅是一种新型陶瓷材料,具有耐高温、耐磨的特点
(5)碳化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据氮和硅的原子结构示意图、元素周期律的知识,写出氮化硅的化学式
您最近一年使用:0次
名校
解题方法
9 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。

| A.图中所示的物质中,只有W、D、E属于电解质 |
| B.Z、C、F均能与NaOH溶液反应,都是酸性氧化物 |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
| D.在催化剂的作用下,R可将Y、Z还原为X |
您最近一年使用:0次

 )
)

