解题方法
1 . 某实验小组以含铁污泥(主要成分为Fe2O3、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(FeSO4•7H2O)和柠檬酸铁铵。
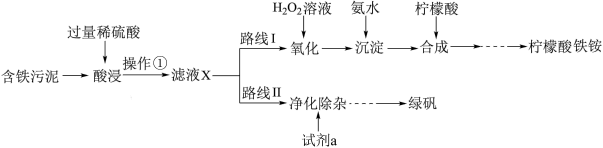
根据所学知识,回答下列问题:
(1)操作①的名称是_______ ,路线I中,加入H2O2溶液的目的是_______ 。
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:_______ ;检验含有Fe3+的试剂是_______ 。
(3)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是_______ 。
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(5)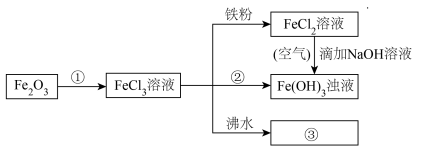
FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是_______ 。

根据所学知识,回答下列问题:
(1)操作①的名称是
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:
(3)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(5)

FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
您最近一年使用:0次
名校
解题方法
2 . 某实验小组以含铁污泥(主要成分为Fe2O3、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(FeSO4•7H2O)和柠檬酸铁铵。

根据所学知识,回答下列问题:
(1)“滤液X”中一定含有的阳离子为___________ 。
(2)路线Ⅰ中,加入H2O2溶液的目的是___________ (用离子方程式表示)。
(3)加入过量试剂a时发生反应的离子方程式___________ 。
(4)“操作②”为过滤、___________ 、___________ 过滤、洗涤、干燥。
(5)“酸浸”时加入400mL 1.5mol/L 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得绿矾得质量为___________ g。

根据所学知识,回答下列问题:
(1)“滤液X”中一定含有的阳离子为
(2)路线Ⅰ中,加入H2O2溶液的目的是
(3)加入过量试剂a时发生反应的离子方程式
(4)“操作②”为过滤、
(5)“酸浸”时加入400mL 1.5mol/L 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得绿矾得质量为
您最近一年使用:0次
解题方法
3 . 某实验小组以含铁污泥(主要成分为 、
、 及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
(1)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:___________ 。
(2)“滤液X”中含有的阳离子为___________ 。
(3)路线I中,加入 溶液的目的是
溶液的目的是___________ 。
(4)写出加入氨水“沉淀”时的离子方程式:___________ 。
(5)写出加入过量铁粉时发生反应的离子方程式:___________ 、___________ 。
(6)“酸浸”时加入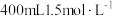 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为___________ g。
 、
、 及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及其他杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。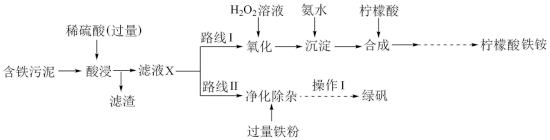
(1)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(2)“滤液X”中含有的阳离子为
(3)路线I中,加入
 溶液的目的是
溶液的目的是(4)写出加入氨水“沉淀”时的离子方程式:
(5)写出加入过量铁粉时发生反应的离子方程式:
(6)“酸浸”时加入
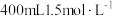 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近一年使用:0次
名校
4 . 有机工业制备的重要的中间体F的合成工艺流程如图:
(1)X的结构简式为______ 。E的结构简式为______ 。
(2)下列说法正确的是______ 。
(3)根据题中信息,写出Y在NaOH溶液中反应化学反应方程式______ 。
(4)写出所有符合下列条件的化合物C的同分异构体:______ 。
①结构中含有苯环,无其他环状结构;苯环上的一元取代物只有一种
②IR光谱显示结构中含“-CN”和“C=S”结构;
③1H-NMR谱显示结构中有3种化学环境的氢原子,个数比为1:6:6。
(5)请以化合物CH2=CH2、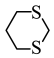 为原料,设计化合物
为原料,设计化合物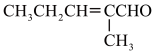 的合成路线:
的合成路线:______ (无机试剂任选)。
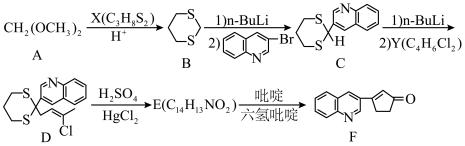
已知:R1COR2+RCH2COR′
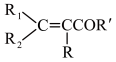
(1)X的结构简式为
(2)下列说法正确的是
| A.-SH的性质类似于-OH,化合物X一定条件下可发生缩聚反应 |
| B.化合物C中有一个手性C原子,所有原子可以在同一平面上 |
| C.化合物F可发生还原反应、加聚反应、水解反应 |
D.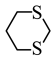 的结构中,4个C和2个S的杂化方式均相同 的结构中,4个C和2个S的杂化方式均相同 |
(4)写出所有符合下列条件的化合物C的同分异构体:
①结构中含有苯环,无其他环状结构;苯环上的一元取代物只有一种
②IR光谱显示结构中含“-CN”和“C=S”结构;
③1H-NMR谱显示结构中有3种化学环境的氢原子,个数比为1:6:6。
(5)请以化合物CH2=CH2、
 为原料,设计化合物
为原料,设计化合物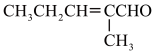 的合成路线:
的合成路线:
您最近一年使用:0次
2023-01-02更新
|
1691次组卷
|
5卷引用:浙江省杭州学军中学2022-2023学年高三上学期模拟考试化学试题
名校
解题方法
5 . 铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠 是水处理过程中的一种新型净水剂,工业上利用
是水处理过程中的一种新型净水剂,工业上利用 和
和 的混合溶液将
的混合溶液将 氧化性制备高铁酸钠,反应的化学方程式为
氧化性制备高铁酸钠,反应的化学方程式为______ ;高铁酸钠能用作新型净水剂的原理是______ 。
(2)某实验小组模拟工业制法,以含铁污泥(主要成分为 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
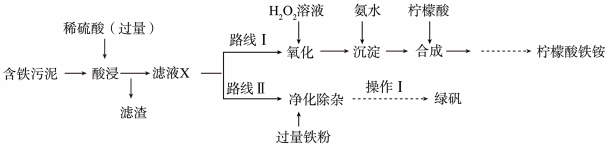
根据所学知识,回答下列问题:
①“滤液X”中一定含有的阳离子为______ 。
②路线I中,加入 溶液的离子方程式
溶液的离子方程式______ 。
③“操作I”为过滤、______ 、______ 、过滤、洗涤、低温烘干。
④实验室用绿矾配置硫酸亚铁溶液时,往往会加入适量的稀硫酸,请你解释其中原因______ (结合必要的方程式)。
(1)高铁酸钠
 是水处理过程中的一种新型净水剂,工业上利用
是水处理过程中的一种新型净水剂,工业上利用 和
和 的混合溶液将
的混合溶液将 氧化性制备高铁酸钠,反应的化学方程式为
氧化性制备高铁酸钠,反应的化学方程式为(2)某实验小组模拟工业制法,以含铁污泥(主要成分为
 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
根据所学知识,回答下列问题:
①“滤液X”中一定含有的阳离子为
②路线I中,加入
 溶液的离子方程式
溶液的离子方程式③“操作I”为过滤、
④实验室用绿矾配置硫酸亚铁溶液时,往往会加入适量的稀硫酸,请你解释其中原因
您最近一年使用:0次
解题方法
6 . 某实验小组以含铁污泥(主要成分为 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
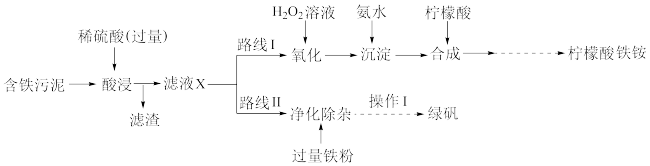
根据所学知识,回答下列问题:
(1) 有多种同位素,其中
有多种同位素,其中 核素中中子数与质子数之差为
核素中中子数与质子数之差为_______ 。
(2)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:_______ 。
(3)“滤液X”中一定含有的阳离子为_______ 。
(4)路线Ⅰ中,加入 溶液的目的是
溶液的目的是_______ 。
(5)写出加入氨水“沉淀”时的离子方程式:_______ 。
(6)写出加入过量铁粉时发生反应的离子方程式:_______ 。
(7)“酸浸”时加入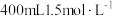 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为_______ g。
 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如下两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
根据所学知识,回答下列问题:
(1)
 有多种同位素,其中
有多种同位素,其中 核素中中子数与质子数之差为
核素中中子数与质子数之差为(2)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(3)“滤液X”中一定含有的阳离子为
(4)路线Ⅰ中,加入
 溶液的目的是
溶液的目的是(5)写出加入氨水“沉淀”时的离子方程式:
(6)写出加入过量铁粉时发生反应的离子方程式:
(7)“酸浸”时加入
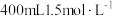 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近一年使用:0次
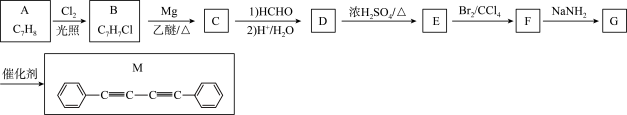
7 . 化合物M是一种新型发光材料中间体。实验室由烃A制备M的一种合成路线如下:
已知:①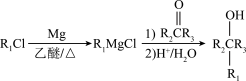
②2RC≡CH RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)
RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)
回答下列问题:
(1)由A生成B的反应类型为___________ 。
(2)C的结构简式为___________ 。D中官能团的电子式为___________
(3)E的化学名称为___________ ;由E制得高聚物的平均相对分子质量为10400,则所得高聚物的平均聚合度为___________ 。
(4)由G生成M的化学方程式为___________ 。
(5)参照上述合成路线和信息,以1,2-二氯乙烷为原料(其他无机试剂任选),设计制备丁烷的合成路线___________ 。

已知:①

②2RC≡CH
 RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)
RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)回答下列问题:
(1)由A生成B的反应类型为
(2)C的结构简式为
(3)E的化学名称为
(4)由G生成M的化学方程式为
(5)参照上述合成路线和信息,以1,2-二氯乙烷为原料(其他无机试剂任选),设计制备丁烷的合成路线
您最近一年使用:0次
名校
8 . I.过渡元素性质复杂多样,请根据下列描述回答问题。
(1)Cu元素在周期表中位于____ 区,它可与多种有机物形成配合物。CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),配位数为4,请在框内画出其结构示意图并用“→”表示出其中的配位键____ 。

(2)有机物E与铜(II)的配合物是一种可发光的发光材料,在发光器材方面有很好的应用前景。其合成E的路线如图,回答下列问题:
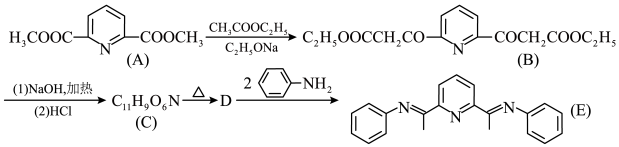
①C生成D的过程中有一种温室气体生成,写出D生成E的化学方程式____ 。
②A有多种同分异构体,其中符合以下条件的共有____ 种。
i.分子中含有吡啶环( )且环上只有2个取代基;
)且环上只有2个取代基;
ii.只含有一种官能团,且核磁共振氢谱只有四种峰;
iii.吡啶环上的一氯取代物只有2种
③结合题给信息,以 和
和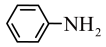 为原料合成西佛碱N-苯基苯甲亚胺
为原料合成西佛碱N-苯基苯甲亚胺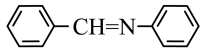 请在框内写出合成路线
请在框内写出合成路线____ 。

II.实验小组对NaHSO3溶液与可溶性铜盐溶液的反应进行探究。
已知:i.Cu2+ [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)
ii.Cu+ [Cu(NH3)2]+(无色溶液)
[Cu(NH3)2]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)
(3)推测实验I产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到____ ,反应的离子方程式为_____ 。
(4)对实验I产生SO2的原因进行分析,提出假设:
假设a:Cu2+水解使溶液中c(H+)增大;
假设b:Cl-存在时,Cu2+与HSO 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设a不合理,实验证据是____ 。
②实验表明假设b合理,实验I反应的离子方程式有_____ 、H++HSO =SO2↑+H2O
=SO2↑+H2O
(5)对比实验I、II,提出假设c:Cl-增强了Cu2+的氧化性。
下述实验III证实了假设c合理,装置如图。实验方案:闭合K,电压表的指针偏转至“X”处;向U形管_____ (补全实验操作及现象)。

(6)将实验II的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和SO 。
。
①通过实验IV证实红色沉淀中含有Cu+和Cu2+。
实验IV: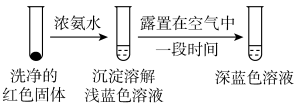
证实红色沉淀中含有Cu+的实验证据是:____ 。
②有同学认为实验IV不足以证实红色沉淀中含有Cu2+,设计实验IV的对比实验V,证实了Cu2+的存在。实验V的方案和现象是:____ 。
(1)Cu元素在周期表中位于

(2)有机物E与铜(II)的配合物是一种可发光的发光材料,在发光器材方面有很好的应用前景。其合成E的路线如图,回答下列问题:

①C生成D的过程中有一种温室气体生成,写出D生成E的化学方程式
②A有多种同分异构体,其中符合以下条件的共有
i.分子中含有吡啶环(
 )且环上只有2个取代基;
)且环上只有2个取代基;ii.只含有一种官能团,且核磁共振氢谱只有四种峰;
iii.吡啶环上的一氯取代物只有2种
③结合题给信息,以
 和
和 为原料合成西佛碱N-苯基苯甲亚胺
为原料合成西佛碱N-苯基苯甲亚胺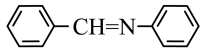 请在框内写出合成路线
请在框内写出合成路线
II.实验小组对NaHSO3溶液与可溶性铜盐溶液的反应进行探究。
| 实验 | 装置 | 试剂x | 操作及现象 |
| I |  | 1mol·L−1CuCl2溶液 | 加入2mLCuCl2溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
| II | 1mol·L−1CuSO4溶液 | 加入2mLCuSO4溶液,得到绿色溶液,3分钟未见明显变化。 |
 [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)ii.Cu+
 [Cu(NH3)2]+(无色溶液)
[Cu(NH3)2]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)(3)推测实验I产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到
(4)对实验I产生SO2的原因进行分析,提出假设:
假设a:Cu2+水解使溶液中c(H+)增大;
假设b:Cl-存在时,Cu2+与HSO
 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。①假设a不合理,实验证据是
②实验表明假设b合理,实验I反应的离子方程式有
 =SO2↑+H2O
=SO2↑+H2O(5)对比实验I、II,提出假设c:Cl-增强了Cu2+的氧化性。
下述实验III证实了假设c合理,装置如图。实验方案:闭合K,电压表的指针偏转至“X”处;向U形管

(6)将实验II的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和SO
 。
。①通过实验IV证实红色沉淀中含有Cu+和Cu2+。
实验IV:

证实红色沉淀中含有Cu+的实验证据是:
②有同学认为实验IV不足以证实红色沉淀中含有Cu2+,设计实验IV的对比实验V,证实了Cu2+的存在。实验V的方案和现象是:
您最近一年使用:0次
解题方法
9 . 某实验小组以含铁污泥(主要成分为 、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(
、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾( )和柠檬酸铁铵。
)和柠檬酸铁铵。
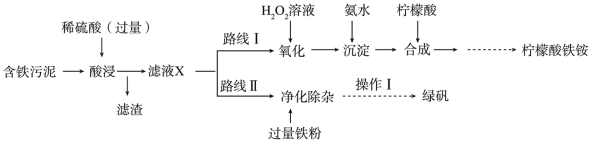
根据所学知识,回答下列问题:
(1)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:_______ 。
(2)“滤液X”中一定含有的阳离子为_______ 。
(3)路线Ⅰ中,加入 溶液的目的是
溶液的目的是_______ 。
(4)写出加入过量铁粉时发生反应的离子方程式:_______ 。
(5)“操作Ⅰ”为过滤、_______ 、_______ 、过滤、洗涤、低温烘干。
(6)“酸浸”时加入400mL1.5 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为_______ g。
 、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(
、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾( )和柠檬酸铁铵。
)和柠檬酸铁铵。
根据所学知识,回答下列问题:
(1)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(2)“滤液X”中一定含有的阳离子为
(3)路线Ⅰ中,加入
 溶液的目的是
溶液的目的是(4)写出加入过量铁粉时发生反应的离子方程式:
(5)“操作Ⅰ”为过滤、
(6)“酸浸”时加入400mL1.5
 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近一年使用:0次
10 . 以硫酸工业产生的SO2尾气和氨水、石灰石、焦炭、碳酸氢铵为原料可以合成硫化钙、硫酸铵、亚硫酸铵等物质,生产流程如下:
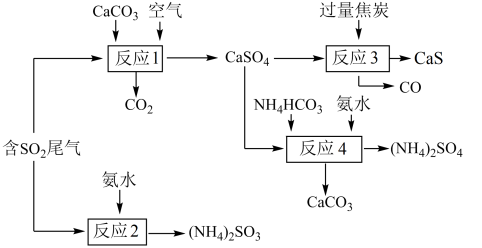
(1)反应1的化学方程式为________________ ;
(2)反应2中用足量氨水吸收SO2,该反应的离子方程式为___________________ ;
(3)为充分利用副产品CO,有人提出以熔融K2CO3为电解质,设计成CO燃料电池以减少对环境的污染。该燃料电池负极的电极反应式为______________ ;
(4)整个合成路线中可以循环利用的物质是_____________ ;
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥, 形成共生系统。计算10.00L 2.00mol/L的(NH4)2SO3溶液可以处理标准状况下NO气体的体积(写出计算过程)_______________ 。

(1)反应1的化学方程式为
(2)反应2中用足量氨水吸收SO2,该反应的离子方程式为
(3)为充分利用副产品CO,有人提出以熔融K2CO3为电解质,设计成CO燃料电池以减少对环境的污染。该燃料电池负极的电极反应式为
(4)整个合成路线中可以循环利用的物质是
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥, 形成共生系统。计算10.00L 2.00mol/L的(NH4)2SO3溶液可以处理标准状况下NO气体的体积(写出计算过程)
您最近一年使用:0次



