解题方法
1 . 下列反应的离子方程式书写正确的是
A.Fe和稀盐酸反应: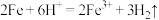 |
B.铜粉与稀硝酸的反应: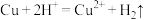 |
C.氯气与碘化钾溶液的反应: |
D.醋酸溶液与水垢中的 反应: 反应: |
您最近一年使用:0次
2 . 标准状况下,多少体积 含
含 个氢原子
个氢原子
 含
含 个氢原子
个氢原子| A.22.4L | B.44.8L | C.11.2L | D.33.6L |
您最近一年使用:0次
解题方法
3 . 下列化学用语表示正确的是
A.苯的结构式: | B.氟化氢的电子式: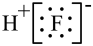 |
C. 的结构示意图: 的结构示意图: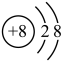 | D.氢氧化钠的电离方程式: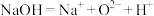 |
您最近一年使用:0次
解题方法
4 . 利用废旧镀锌铁皮制备Fe3O4胶体粒子的流程如下:
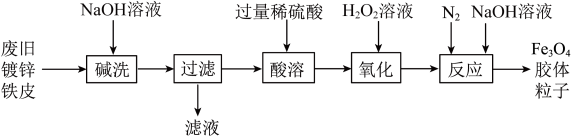
| A.Fe3O4俗称铁红 |
| B.“碱洗”的主要目的是除去镀锌铁皮表面的油污 |
| C.“酸溶”反应的离子方程式为Fe+2H+=Fe2++H2↑ |
D.“氧化”后溶液中所存在的离子为:H+、Fe3+、SO |
您最近一年使用:0次
解题方法
5 . 下列指定反应的离子方程式正确的是
A.碳酸氢钠和过量氢氧化钙反应:HCO +Ca2++OH-= CaCO3↓+H2O +Ca2++OH-= CaCO3↓+H2O |
B.用稀硝酸与铜反应:Cu+4H++ 2NO = Cu2++2NO2↑+2H2O = Cu2++2NO2↑+2H2O |
| C.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| D.H2SO4溶液与氨水反应:H++OH-=H2O |
您最近一年使用:0次
解题方法
6 . 舍勒发现氯气是在1774年,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体,发生的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是
 MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,下列对于该反应的说法正确的是| A.KMnO4是还原剂 | B.MnCl2是氧化产物 |
| C.HCl在反应中得电子 | D.HCl体现还原性和酸性 |
您最近一年使用:0次
7 . 舍勒发现氯气是在1774年,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体,发生的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。 氯气和氢气的反应属于
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。 氯气和氢气的反应属于
 MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。 氯气和氢气的反应属于
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。 氯气和氢气的反应属于| A.分解反应 | B.化合反应 | C.置换反应 | D.复分解反应 |
您最近一年使用:0次
8 . 化学促进了科技进步和社会发展,下列叙述中没有 涉及化学变化的是
| A.工业上用铁触媒作催化剂合成氨 |
| B.科学家成功将CO2转化为淀粉或葡萄糖 |
| C.北京冬奥会场馆使用CO2跨临界直冷制冰 |
| D.《神农本草经》中记载的“石胆能化铁为铜” |
您最近一年使用:0次
解题方法
9 . 已知SO2、Cl2和水的反应为SO2+Cl2+2H2O=H2SO4+2HCl,下列说法正确的是
A.硫酸的电离方程式:H2SO4=H +SO +SO | B. 、 、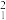 H和 H和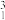 H互为同位素 H互为同位素 |
C.中子数为20的氯原子: | D.SO2属于电解质 |
您最近一年使用:0次
名校
解题方法
10 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,广泛应用于纺织业和造纸业。利用碱性NaBH4溶液或Zn还原含硫化合物是制备Na2S2O4常用方法。
已知:①Na2S2O4在水溶液可以发生歧化反应(只有S元素化合价的升降),受热易分解。
②NaBH4是一种强还原剂,酸性或受热条件下易与水反应产生氢气,在碱性溶液中比较稳定。
③生成物的ΔG越大,表示在该条件下转化成该物质的可能性较大。溶液中部分含硫组分的ΔG如图所示。

Ⅰ.NaBH4碱性溶液还原法
(1)12%NaBH4碱性溶液配制:在烧杯中加入48g水,再向其中加入___________ (请完成溶液配制,所需试剂为40gNaOH固体及12gNaBH4固体)。
(2)溶有饱和SO2的NaHSO3溶液制备:利用如图所示装置来制备该溶液,判断制备完成的方法是___________ 。

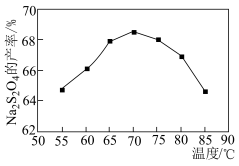
(3)将12%NaBH4碱性溶液与制备的NaHSO3溶液在无氧、水浴加热的条件下发生反应,相同时间内,Na2S2O4的产率随温度的变化如图所示,70℃后Na2S2O4的产率下降的原因是___________ 。Na2S2O4在水溶液中发生歧化反应的离子方程式为___________ 。
Ⅱ.锌粉还原法
已知:①Zn+2H2SO3 ZnS2O4(易溶于水)+2H2O;
ZnS2O4(易溶于水)+2H2O;
②二价锌在水溶液中的存在形式与pH的关系如图所示。
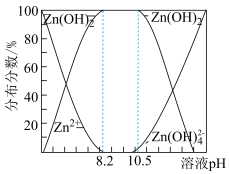
(4)请补充完整由锌粉制备Na2S2O4粗品的实验方案:向盛有水的烧杯中加入一定量的Zn粉,搅拌,___________ ,向滤液中加入氯化钠粉末至有大量晶体析出,过滤得到Na2S2O4粗品(实验中须使用的试剂:SO2、1mol·L-1NaOH溶液)。
已知:①Na2S2O4在水溶液可以发生歧化反应(只有S元素化合价的升降),受热易分解。
②NaBH4是一种强还原剂,酸性或受热条件下易与水反应产生氢气,在碱性溶液中比较稳定。
③生成物的ΔG越大,表示在该条件下转化成该物质的可能性较大。溶液中部分含硫组分的ΔG如图所示。

Ⅰ.NaBH4碱性溶液还原法
(1)12%NaBH4碱性溶液配制:在烧杯中加入48g水,再向其中加入
(2)溶有饱和SO2的NaHSO3溶液制备:利用如图所示装置来制备该溶液,判断制备完成的方法是

(3)将12%NaBH4碱性溶液与制备的NaHSO3溶液在无氧、水浴加热的条件下发生反应,相同时间内,Na2S2O4的产率随温度的变化如图所示,70℃后Na2S2O4的产率下降的原因是

Ⅱ.锌粉还原法
已知:①Zn+2H2SO3
 ZnS2O4(易溶于水)+2H2O;
ZnS2O4(易溶于水)+2H2O;②二价锌在水溶液中的存在形式与pH的关系如图所示。

(4)请补充完整由锌粉制备Na2S2O4粗品的实验方案:向盛有水的烧杯中加入一定量的Zn粉,搅拌,
您最近一年使用:0次
2024-02-22更新
|
325次组卷
|
2卷引用:江苏省南通市如东中学,如东一高等四校2023-2024学年高三上学期12月学情调研化学试题



