名校
解题方法
1 . 氧、硫及其化合物应用广泛。O2可用作燃料电池的氧化剂。S8在液态SO2中被AsF5氧化成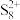 ,反应方程式为S8+3AsF5
,反应方程式为S8+3AsF5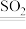 S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2
S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2 SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于化学反应表示或说法正确的是
SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于化学反应表示或说法正确的是
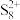 ,反应方程式为S8+3AsF5
,反应方程式为S8+3AsF5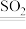 S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2
S8(AsF6)2+AsF3。氧能形成H2O、H2O2、Na2O2、SO2、V2O5等重要氧化物。SO2是一种重要的工业原料,可通过煅烧黄铁矿或加热无水硫酸钙、焦炭及二氧化硅的混合物(CaSO4+C+SiO2 SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于化学反应表示或说法正确的是
SO2↑+CO↑+CaSiO3)等方法来制取。SO2在V2O5催化作用下与O2反应生成SO3。下列关于化学反应表示或说法正确的是| A.碱性燃料电池的负极电极反应式O2+2H2O+4e-=4OH- |
| B.反应2SO2+2H2O2=2H2SO3+O2 |
C.CaSO4+C+SiO2 SO2↑+CO↑+CaSiO3中氧化剂与还原剂物质的量之比为1:1 SO2↑+CO↑+CaSiO3中氧化剂与还原剂物质的量之比为1:1 |
| D.1mol SO2在V2O5催化作用下与足量O2完全反应,可生成1molSO3 |
您最近一年使用:0次
2 . 用铁泥(主要成分为 、FeO和少量Fe)制备超顺磁性纳米
、FeO和少量Fe)制备超顺磁性纳米 (平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是
(平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是
 、FeO和少量Fe)制备超顺磁性纳米
、FeO和少量Fe)制备超顺磁性纳米 (平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是
(平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是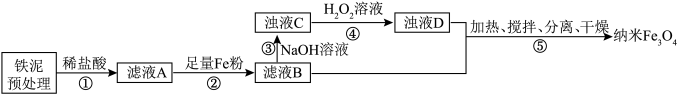
| A.滤液B的溶质主要为氯化铁 |
| B.步骤②中发生的反应均为置换反应 |
C.为防止在步骤⑤中继续氧化亚铁离子,步骤④反应完成后剩余的 需加热除去 需加热除去 |
D.将步骤⑤得到的纳米 均匀分散在水中时,不能产生丁达尔效应 均匀分散在水中时,不能产生丁达尔效应 |
您最近一年使用:0次
解题方法
3 . 为研究Na2SO3的氧化性、还原性以及H2SO3的酸性,进行如下实验(现有试剂:溴水、Na2S溶液、Na2SO3溶液、H2SO4、NaOH溶液、氨水)。
(1)欲证明Na2SO3具有还原性,在盛有约2 mL Na2SO3溶液中滴加_______ 试剂,看到的现象是_______ ,则证明之。其中发生反应的离子方程式为_______ 。
(2)欲证明Na2SO3具有氧化性,在盛有约2 mL Na2SO3溶液中滴加_______ 试剂,看到的现象是_______ ,则证明之。其中发生反应的离子方程式为_______ 。
(3)欲证明H2SO3的酸性弱于H2SO4,选用的试剂有_______ ,反应的现象是_______ ,反应的离子方程式为_______ 。
(1)欲证明Na2SO3具有还原性,在盛有约2 mL Na2SO3溶液中滴加
(2)欲证明Na2SO3具有氧化性,在盛有约2 mL Na2SO3溶液中滴加
(3)欲证明H2SO3的酸性弱于H2SO4,选用的试剂有
您最近一年使用:0次
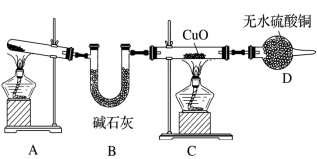
4 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产,某化学兴趣小组利用如图装置探究氨气的相关性质。
②参阅资料:Cu、Cu2O均为红色固体,其中Cu2O能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色[Cu(NH3)2]2+,而Cu不与氨水反应。
(1)装置D的作用:_______ 。
(2)甲同学认为该实验装置不严谨,应在装置D后再连接一个装有CaCl2固体的球形干燥管,其目的是_______ 。
(3)实验开始时,先点燃装置_______ (填“A”或“C”)的酒精灯,一段时间后再点燃另一装置的酒精灯。实验结束发现:C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。为进一步确定红色固体物质,乙同学提出假设:①红色固体为Cu单质;②红色固体为Cu2O;③_______ 。
设计实验操作:取反应后的红色固体物质于洁净试管中,向其中滴加足量氨水并充分振荡,观察到溶液变为蓝色,固体有剩余。丙同学为验证乙同学的假设,取CuO固体4.0 g重复上述加热实验,反应后装置C中得红色固体3.52 g。请结合上述信息,写出NH3与CuO反应的化学方程式:____ 。
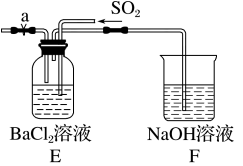
(4)已知,将SO2通入BaCl2溶液中,无明显现象。如图若将生成的NH3与SO2同时通入BaCl2溶液中,产生白色沉淀,反应的化学方程式为_______ 。若向a处通入_______ (填字母),在E中也能产生白色沉淀,其白色沉淀为_______ 。
②参阅资料:Cu、Cu2O均为红色固体,其中Cu2O能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色[Cu(NH3)2]2+,而Cu不与氨水反应。
(1)装置D的作用:
(2)甲同学认为该实验装置不严谨,应在装置D后再连接一个装有CaCl2固体的球形干燥管,其目的是
(3)实验开始时,先点燃装置
设计实验操作:取反应后的红色固体物质于洁净试管中,向其中滴加足量氨水并充分振荡,观察到溶液变为蓝色,固体有剩余。丙同学为验证乙同学的假设,取CuO固体4.0 g重复上述加热实验,反应后装置C中得红色固体3.52 g。请结合上述信息,写出NH3与CuO反应的化学方程式:
(4)已知,将SO2通入BaCl2溶液中,无明显现象。如图若将生成的NH3与SO2同时通入BaCl2溶液中,产生白色沉淀,反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 下列物质的用途或性质与解释对应关系错误的是
选项 | 用途或性质 | 解释 |
A | 钠钾合金用作核反应堆的传热介质 | 钠、钾均为活泼金属,金属性强 |
B |
|
|
C | 钢瓶可用于储存液氯 | 常温下,铁与液氯不反应 |
D | 聚乙炔具有导电性 | 聚乙炔结构中存在共轭大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
昨日更新
|
170次组卷
|
2卷引用:河北省石家庄市2024届普通高中学校高三毕业年级教学质量检测(三)化学试卷
6 . 科教兴国,我国科技发展在多个领域获得突破。下列说法错误的是
| A.新能源甲醇燃料电池汽车在行驶时其能量的转化形式:电能→化学能 |
| B.新一代航空发动机陶瓷基复合材料:具有耐高温、耐腐蚀特性 |
| C.利用高纯硅可以制成通信设备的芯片:高纯硅是广泛的半导体材料 |
| D.火焰喷雾技术制备纳米材料:在高温火焰喷雾中形成的胶体属于气溶胶 |
您最近一年使用:0次
昨日更新
|
112次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期三模理科综合试题-高中化学
名校
7 . 回答下列问题:
(1)淀粉的分子式为_______ 。
(2)写出工业上冶炼金属铝的化学方程式_______ 。
(3)简述工业合成氨采用的压强通常为 的原因
的原因_______ 。
(1)淀粉的分子式为
(2)写出工业上冶炼金属铝的化学方程式
(3)简述工业合成氨采用的压强通常为
 的原因
的原因
您最近一年使用:0次
8 . 下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 取少量 试样加水溶解,加稀硫酸酸化,滴加 试样加水溶解,加稀硫酸酸化,滴加 溶液 溶液 | 溶液呈红色 | 该 试样已经变质 试样已经变质 |
| B | 向盛有浓硝酸的试管中分别加入 片和 片和 片 片 | 前者没有明显现象,后者反应剧烈,产生大量红棕色气体 | 还原性 |
| C | 淀粉- 溶液中通入 溶液中通入 ,再通入 ,再通入 | 溶液先出现蓝色,后蓝色褪去 | 还原性: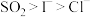 |
| D | 向纯碱中滴加足量浓盐酸,将产生的气体通入硅酸钠溶液 | 溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列有关实验说法,不正确 的是
| A.浓硝酸应保存在带橡胶塞的棕色细口试剂瓶中 |
| B.焰色反应时,先用稀盐酸洗涤铂丝并在酒精灯火焰上灼烧,然后再进行实验 |
| C.向碳酸钠和碳酸氢钠固体中分别滴加几滴水,可通过温度变化鉴别两者 |
| D.一旦发生火情,应立即切断室内电源,移走可燃物 |
您最近一年使用:0次
名校
10 . 物质的应用性是化学科学研究的重要内容。下列物质的性质与用途不具有 对应关系的是
A. 有漂白性,故能使酸性高锰酸钾溶液褪色 有漂白性,故能使酸性高锰酸钾溶液褪色 |
B.浓硫酸有吸水性,故可以干燥 |
| C.液氨汽化时要吸收大量的热,可用作制冷剂 |
D. 有强氧化性,故可以作自来水的消毒剂 有强氧化性,故可以作自来水的消毒剂 |
您最近一年使用:0次

 键
键

