解题方法
1 . 某兴趣小组的同学制备了氯气并探究其性质。试回答下列问题:
Ⅰ.写出实验室制取氯气的化学方程式:_______________________ 。
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回答下列问题:
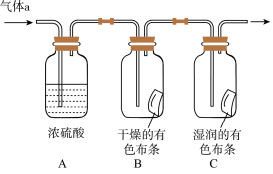
(1)浓硫酸的作用是__________________________ 。
(2)证明氯气和水反应的实验现象为___________________________ 。
(3)ICl的性质与 类似,写出ICl与水反应的化学方程式
类似,写出ICl与水反应的化学方程式_________________________________ 。
(4)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是__________________________________ 。
(5)漂白粉溶于水后,遇到空气中的 ,即产生漂白、杀菌作用,反应的化学方程式是
,即产生漂白、杀菌作用,反应的化学方程式是________ 。
Ⅰ.写出实验室制取氯气的化学方程式:
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回答下列问题:

(1)浓硫酸的作用是
(2)证明氯气和水反应的实验现象为
(3)ICl的性质与
 类似,写出ICl与水反应的化学方程式
类似,写出ICl与水反应的化学方程式(4)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是
(5)漂白粉溶于水后,遇到空气中的
 ,即产生漂白、杀菌作用,反应的化学方程式是
,即产生漂白、杀菌作用,反应的化学方程式是
您最近一年使用:0次
2020-10-02更新
|
1649次组卷
|
3卷引用:高一必修第一册(苏教2019)专题3 专题综合检测卷
2 . 如图为实验室制备乙炔并进行性质验证的装置(夹持仪器已略去)。
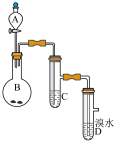
(1)实验开始前,首先进行的操作是___ ;
(2)实验室制备乙炔的方程式为___ ;
(3)仪器A在安装前必须进行的操作是___ ,为防止气体生成的速率过快,由A滴入B的试剂为___ 。
(4)装置C可选用的试剂为___ (写出一种即可),其作用为___ ;
(5)反应开始后,D中的现象为___ ,所发生反应的反应类型为___ ;
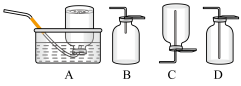
(6)D中验证实验结束后。B中反应仍在继续。此时可撤去装置D,在装置C之后连接收集装置,以下装置中最适合用于收集乙炔的是___ 。

(1)实验开始前,首先进行的操作是
(2)实验室制备乙炔的方程式为
(3)仪器A在安装前必须进行的操作是
(4)装置C可选用的试剂为
(5)反应开始后,D中的现象为
(6)D中验证实验结束后。B中反应仍在继续。此时可撤去装置D,在装置C之后连接收集装置,以下装置中最适合用于收集乙炔的是

您最近一年使用:0次
2019-11-13更新
|
865次组卷
|
4卷引用:第二章 烃
第二章 烃云南省云天化中学2019-2020学年高二上学期期中考试化学试题(已下线)2.2.2 炔烃-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)安徽省合肥市第八中学2021-2022学年高二下学期实验班开学考化学试题
13-14高一·全国·课时练习
名校
3 . 某学生在做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关的实验现象。现在请你帮助该学生整理并完成实验报告。
(1)实验目的:探究同一主族元素性质的递变规律。
(2)实验用品:
仪器:试管、胶头滴管
药品:氯水、溴水、溴化钠溶液、碘化钠溶液、四氯化碳。
(3)实验内容(在下表横线中填写相关内容):
(4)实验结论:____________________ 。
(5)问题和讨论:
①上述两个实验中发生的反应的离子方程式分别为_________ 、________ 。
②由于氟过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯强:_______ 、_____ 。
(1)实验目的:探究同一主族元素性质的递变规律。
(2)实验用品:
仪器:试管、胶头滴管
药品:氯水、溴水、溴化钠溶液、碘化钠溶液、四氯化碳。
(3)实验内容(在下表横线中填写相关内容):
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量新制溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈 |
(4)实验结论:
(5)问题和讨论:
①上述两个实验中发生的反应的离子方程式分别为
②由于氟过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯强:
您最近一年使用:0次
2017-05-02更新
|
154次组卷
|
9卷引用:人教版高中化学必修二第一章《物质结构 元素周期律》测试卷
人教版高中化学必修二第一章《物质结构 元素周期律》测试卷人教版高中化学必修二第一单元《物质结构 元素周期律》测试卷人教版高中化学必修二第一章《物质结构 元素周期律》测试卷2019-2020学年鲁科版高中化学必修2第一章《原子结构与元素周期律》测试卷(已下线)2014年高一化学人教版必修二 1-1-2元素性质练习卷(已下线)2014学年高一化学人教版必修2 1.1.2元素的性质与原子结构练习卷2015-2016学年吉林省吉林一中高一下期末化学试卷宁夏石嘴山市第三中学2016-2017学年高一下学期期中考试化学试题河南省信阳市浉河区新时代学校2020-2021学年高一下学期第一阶段教学质量检测化学试题
解题方法
4 . 实验室用二氧化锰和浓盐酸反应制取氯气并探究其性质,实验装置如图所示
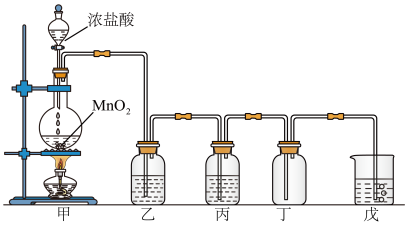
(1)装置甲中发生的离子方程式为_______ ;
(2)装置乙中盛放的试剂为_______ ;装置丙的作用为_______ ;
(3)将生成的气体通入紫色石蕊试液中,现象为_______ ;
(4)戊中反应化学方程式为_______ ;
(5)如果将甲中产生的气体和SO2一起通入品红溶液中反应的方程式为_______ ;当两气体同时按照物质的量比1:1通入时,品红溶液中的现象为_______ 。

(1)装置甲中发生的离子方程式为
(2)装置乙中盛放的试剂为
(3)将生成的气体通入紫色石蕊试液中,现象为
(4)戊中反应化学方程式为
(5)如果将甲中产生的气体和SO2一起通入品红溶液中反应的方程式为
您最近一年使用:0次
2022-12-14更新
|
839次组卷
|
3卷引用:【知识图鉴】单元讲练测必修第二册第五单元 02基础练
(已下线)【知识图鉴】单元讲练测必修第二册第五单元 02基础练辽宁省本溪展望国际学校2021-2022学年高一下学期开学检测化学试题黑龙江省海林市朝鲜族中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 请回答下列关于胶体的有关问题
(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制备Fe(OH)3胶体的化学方程式为:_____ 。
(2)已知 Fe(OH)3胶粒和Al(OH)3胶粒带正电荷,H2SiO3胶粒带负电荷,则:
①Fe(OH)3胶体和H2SiO3胶体混合的现象是_____ 。
②已知Al(OH)3胶体能够净水,则Fe(OH)3胶体_____ (填“能”或“不能”)净水。
(3)下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
①“卤水点豆腐,一物降一物”,这里说到的是豆腐的制作,利用的胶体性质是_____ (填字母,下同)。
②工厂采用高压静电除尘,利用的胶体性质是_____ 。
③拍照时,清晨或者大雨过后拍到“耶稣光”的概率比较高_____ 。
(4)是否能用渗析的方法除尽Fe(OH)3胶体中的Cl-?若能。请设计实验证明:若不能,请说明理由。___________ 。
(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制备Fe(OH)3胶体的化学方程式为:
(2)已知 Fe(OH)3胶粒和Al(OH)3胶粒带正电荷,H2SiO3胶粒带负电荷,则:
①Fe(OH)3胶体和H2SiO3胶体混合的现象是
②已知Al(OH)3胶体能够净水,则Fe(OH)3胶体
(3)下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
①“卤水点豆腐,一物降一物”,这里说到的是豆腐的制作,利用的胶体性质是
②工厂采用高压静电除尘,利用的胶体性质是
③拍照时,清晨或者大雨过后拍到“耶稣光”的概率比较高
(4)是否能用渗析的方法除尽Fe(OH)3胶体中的Cl-?若能。请设计实验证明:若不能,请说明理由。
您最近一年使用:0次
名校
6 . 铁及其化合物在生产、生活中有及其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_______ ,分散剂是_______ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是________
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备 Fe(OH)3胶体的化学方程式是________ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是_______ 。
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是_______
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠 有多种方法,其中一种方法的原理可用离子方程式表示为 3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl-+5H2O,则Na2FeO4中铁元素的化合价为_______ ,该离子反应中氧化剂与还原剂的个数比为_______ ,生成1个高铁酸钠转移 _______ 个电子。
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备 Fe(OH)3胶体的化学方程式是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠 有多种方法,其中一种方法的原理可用离子方程式表示为 3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl-+5H2O,则Na2FeO4中铁元素的化合价为
您最近一年使用:0次
名校
7 . 下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第____ 周期第_____ 族,A、B、C三种元素原子半径从大到小的顺序是_________________ ;
(2)D简单离子的结构示意图为_____________ ,D、E中金属性较强的元素是________ 。D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
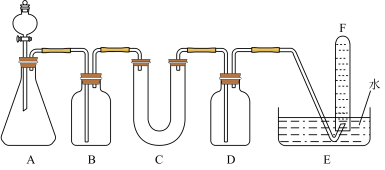
(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去_____________ ;
(4)装置C中X与CO2反应的化学方程式是_____________________ ,装置D盛放NaOH溶液的作用是除去____________ ;
(5)为检验试管F收集的气体,进行____________ 操作,出现_________ 现象,即证明X可作供氧剂。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第
(2)D简单离子的结构示意图为

(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去
(4)装置C中X与CO2反应的化学方程式是
(5)为检验试管F收集的气体,进行
您最近一年使用:0次
2019-03-25更新
|
2345次组卷
|
8卷引用:人教版(2019)高一必修第一册 全书综合训练(二)
13-14高一·全国·课时练习
8 . 黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫和铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2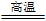 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是________ (填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是________ (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是_____________________________________________________ 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为________ 。证明炉渣中含有FeO的实验现象为_______________________ 。
(1)冶炼铜的反应为8CuFeS2+21O2
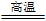 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为
您最近一年使用:0次
2018-06-27更新
|
223次组卷
|
4卷引用:苏教版高中化学必修2专题四《化学科学与人类文明》测试卷
苏教版高中化学必修2专题四《化学科学与人类文明》测试卷苏教版高一化学必修2专题4《化学科学与人类文明》测试卷(已下线)2014年高一化学人教版必修二 4-1-1金属矿物的开发利用练习卷【全国市级联考】贵州省毕节市2017-2018学年高一毕业学业达标模拟考试化学试题
名校
9 . 金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是2NaCl(熔融) 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)保存金属钠的正确方法是___________。
(2)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图所示),请写出该反应的化学方程式:___________ ,生成物的颜色为___________ 。

(3)Na、NaOH久置于空气中最终都变为___________ (填化学式)。
(4)除去碳酸钠粉末中混有的少量碳酸氢钠固体的最适宜的方法为___________ ,所涉及到的化学方程式为___________ 。
(5)工业上以NaCl、NH3、CO2等为原料先制得NaHCO3,反应的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,进而生产纯碱。
某活动小组根据上述原理,制备碳酸氢钠。实验装置如图所示(夹持、固定用仪器未画出)。

乙装置中的试剂是___________ ;实验中分离出NaHCO3晶体的操作是___________ (填分离操作名称)。
 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:(1)保存金属钠的正确方法是___________。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |

(3)Na、NaOH久置于空气中最终都变为
(4)除去碳酸钠粉末中混有的少量碳酸氢钠固体的最适宜的方法为
(5)工业上以NaCl、NH3、CO2等为原料先制得NaHCO3,反应的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,进而生产纯碱。
某活动小组根据上述原理,制备碳酸氢钠。实验装置如图所示(夹持、固定用仪器未画出)。

乙装置中的试剂是
您最近一年使用:0次
2022-02-28更新
|
898次组卷
|
4卷引用:第二章《海水中的重要元素----钠和氯》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)
(已下线)第二章《海水中的重要元素----钠和氯》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)重庆市璧山中学校2021-2022学年高一12月月考化学试题福建省三明第一中学2022~2023学年高一上学期第一次月考化学试题安徽省马鞍山市第二十二中学2022-2023学年高一上学期11月期中考试化学试题
名校
10 . 高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂。实验小组欲制备高铁酸钾并探究其性质。已知:
)是一种高效多功能的新型非氯绿色消毒剂。实验小组欲制备高铁酸钾并探究其性质。已知: 为紫色固体,具有强氧化性;在碱性溶液中较稳定,微溶于KOH溶液;在酸性或中性溶液中快速产生
为紫色固体,具有强氧化性;在碱性溶液中较稳定,微溶于KOH溶液;在酸性或中性溶液中快速产生 ,
,

(1)除了用二氧化锰和浓盐酸反应外,实验室可以用氯酸钾和浓盐酸反应制取氯气,反应方程式如下: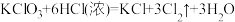 。
。
①浓盐酸在反应中显示出来的性质是___________ 。
②若产生标况下 ,则被氧化的HCl的物质的量为
,则被氧化的HCl的物质的量为___________ mol。
③如果要将装置B补充完整,除需用导管外,试剂瓶中还应装的除杂试剂为___________ 。
(2)C中得到紫色固体和溶液。C中 发生的反应有
发生的反应有 。另外还有
。另外还有______ 。(用离子方程式表示)
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是___________ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为2%,则生产1000kg该溶液需消耗氯气的质量为___________ kg(保留整数)。
 )是一种高效多功能的新型非氯绿色消毒剂。实验小组欲制备高铁酸钾并探究其性质。已知:
)是一种高效多功能的新型非氯绿色消毒剂。实验小组欲制备高铁酸钾并探究其性质。已知: 为紫色固体,具有强氧化性;在碱性溶液中较稳定,微溶于KOH溶液;在酸性或中性溶液中快速产生
为紫色固体,具有强氧化性;在碱性溶液中较稳定,微溶于KOH溶液;在酸性或中性溶液中快速产生 ,
,
(1)除了用二氧化锰和浓盐酸反应外,实验室可以用氯酸钾和浓盐酸反应制取氯气,反应方程式如下:
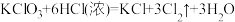 。
。①浓盐酸在反应中显示出来的性质是
②若产生标况下
 ,则被氧化的HCl的物质的量为
,则被氧化的HCl的物质的量为③如果要将装置B补充完整,除需用导管外,试剂瓶中还应装的除杂试剂为
(2)C中得到紫色固体和溶液。C中
 发生的反应有
发生的反应有 。另外还有
。另外还有(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次



