名校
1 . 甲、乙两烧杯内盛有等质量、等质量分数的盐酸。把镁粉逐渐加入甲烧杯,把锌粉逐渐加入乙烧杯;测得加入金属质量(m)及相应的烧杯内物质的质量变化量(△M),将△M~m作图得到曲线 oabe和ocde(见下图)。根据图中信息,判断下列说法错误的是
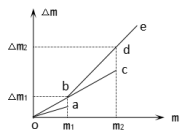

| A.镁和锌的质量比m1:m2=22:63 |
| B.m1-△M1=m2-△M2 |
| C.曲线oabe表示的是甲烧杯中△M与m的变化关系 |
| D.当乙烧杯内加入锌质量为m1时,溶液中溶质只是氯化锌 |
您最近一年使用:0次
解题方法
2 . 将偏铝酸钠溶液和盐酸等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元素的质量相等,则原偏铝酸钠溶液和盐酸的物质的量浓度之比可能是
| A.1∶3 | B.2∶1 | C.1∶4 | D.2∶5 |
您最近一年使用:0次
3 . 下列溶液中c(Cl-)与50mL1mol·L-1的AlCl3溶液中c(Cl-)相等的是
| A.150mL1mol·L-1NaCl | B.75mL2mol·L-1CaCl2 |
| C.150mL3mol·L-1KCl | D.75mL1mol·L-1FeCl3 |
您最近一年使用:0次
4 . 下列溶液与20 mL 1 mol·L-1NaNO3溶液中 的物质的量浓度相等的是
的物质的量浓度相等的是
 的物质的量浓度相等的是
的物质的量浓度相等的是| A.10 mL 1 mol·L-1Mg(NO3)2溶液 |
| B.5 mL 0.8 mol·L-1Al(NO3)3溶液 |
| C.10 mL 1 mol·L-1AgNO3溶液 |
| D.10 mL 0.5 mol·L-1Cu(NO3)2溶液 |
您最近一年使用:0次
名校
解题方法
5 . 某溶液可能含有Cl-、SO 、CO
、CO 、NH
、NH 、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体(已知:NH
、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体(已知:NH +OH-=NH3↑+H2O),同时产生2.14g 红褐色沉淀;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的白色沉淀。由此可知原溶液中
+OH-=NH3↑+H2O),同时产生2.14g 红褐色沉淀;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的白色沉淀。由此可知原溶液中
 、CO
、CO 、NH
、NH 、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体(已知:NH
、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体(已知:NH +OH-=NH3↑+H2O),同时产生2.14g 红褐色沉淀;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的白色沉淀。由此可知原溶液中
+OH-=NH3↑+H2O),同时产生2.14g 红褐色沉淀;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的白色沉淀。由此可知原溶液中| A.至少存在4种离子 |
| B.Cl-一定存在,且c(Cl-)≥0.4mol/L |
C.SO 、NH 、NH 、Fe3+一定存在,Cl-可能不存在 、Fe3+一定存在,Cl-可能不存在 |
D.CO 、Al3+一定不存在,K+可能存在 、Al3+一定不存在,K+可能存在 |
您最近一年使用:0次
2022-12-19更新
|
237次组卷
|
3卷引用:2016-2017学年河北省冀州中学高一12月月考化学卷
名校
6 . 在温度、压强、容积均相同的两个密闭容器中,分别充有甲、乙两种气体,若甲气体的质量大于乙气体的质量,则下列说法正确的是
| A.甲的物质的量等于乙的物质的量 | B.甲的物质的量比乙的物质的量多 |
| C.甲的摩尔体积比乙的摩尔体积大 | D.乙的密度比甲的密度小 |
您最近一年使用:0次
名校
7 . 某氯原子的质量为ag,12C原子的质量为bg,用NA表示阿伏加德罗常数的值,下列说法中不正确的是
A.该氯原子的相对原子质量为 g/mol g/mol |
B.xg该原子的物质的量为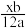 mol mol |
| C.1mol该氯原子的质量是aNAg |
D.yg该原子所含的原子数为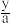 |
您最近一年使用:0次
名校
解题方法
8 . 在石灰窑中烧制生石灰,1mol CaCO3完全分解所需要的能量,可燃烧0.453mol碳来提供。设空气中O2体积分数为0.21,N2为0.79,则石灰窑产生的气体中CO2的体积分数可能是
| A.0.45 | B.0.46 | C.0.49 | D.0.52 |
您最近一年使用:0次
9 . 已知:还原性:HSO >I-,氧化性:IO
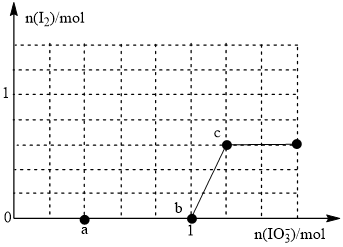
>I-,氧化性:IO >I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是
>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是
 >I-,氧化性:IO
>I-,氧化性:IO >I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是
>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是
A.0~a间发生反应:3HSO +IO +IO =3SO =3SO +I-+3H+ +I-+3H+ |
| B.a~b间共消耗NaHSO3的物质的量为0.6mol |
| C.b~c间反应:I2仅是氧化产物 |
| D.当溶液中I-与I2的物质的量之比为5:3时,加入的KIO3为1.1mol |
您最近一年使用:0次
解题方法
10 . 向 和
和 混合溶液中滴加
混合溶液中滴加 稀盐酸,
稀盐酸, 的生成量与加入盐酸的体积(
的生成量与加入盐酸的体积( )的关系如图所示。下列判断正确的是
)的关系如图所示。下列判断正确的是
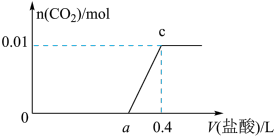
 和
和 混合溶液中滴加
混合溶液中滴加 稀盐酸,
稀盐酸, 的生成量与加入盐酸的体积(
的生成量与加入盐酸的体积( )的关系如图所示。下列判断正确的是
)的关系如图所示。下列判断正确的是
A.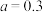 |
B.在 范围内,只发生中和反应 范围内,只发生中和反应 |
C.原混合溶液中 与 与 的物质的量之比为2:1 的物质的量之比为2:1 |
D.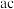 段发生反应的离子方程式为: 段发生反应的离子方程式为: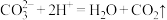 |
您最近一年使用:0次



