名校
1 . 肇州二中“爱化学”实验小组中甲、乙、丙三名同学分别进行Fe(OH)3胶体制备实验
Ⅰ.甲同学:向FeCl3稀溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向40mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是_______
(2)Fe(OH)3胶体制备的化学方程式为_______
(3)胶体和溶液的本质区别是分散质_______ 大小不同;可通过_______ 来区别胶体和溶液。
Ⅱ.三位同学在学习胶体在生产生活中应用时,对“高铁酸钠如何杀菌消毒、净水?”产生浓厚兴趣,经查阅资料,高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O,请你帮助他们解释如下问题:
(4)该反应中氧化剂是_______ (用化学式表示,下同),_______ 元素被氧化,还原剂为_______ ,还原产物为_______
(5)高铁酸钠的氧化性比高锰酸钾(KMnO4)、次氯酸(HClO)等强氧化剂还要强。高铁酸钠的的电离方程式是_______
(6)高铁酸钠之所以是水处理过程中使用的一种新型净水剂,原因是高铁酸钠中+6铁元素利用强氧化性杀菌消毒后转化为Fe(OH)3胶体,吸附水中悬浮物,达到既能杀菌消毒又能净水的目的,氢氧化铁胶体微粒直径的范围是_______ nm。
Ⅰ.甲同学:向FeCl3稀溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向40mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)Fe(OH)3胶体制备的化学方程式为
(3)胶体和溶液的本质区别是分散质
Ⅱ.三位同学在学习胶体在生产生活中应用时,对“高铁酸钠如何杀菌消毒、净水?”产生浓厚兴趣,经查阅资料,高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O,请你帮助他们解释如下问题:
(4)该反应中氧化剂是
(5)高铁酸钠的氧化性比高锰酸钾(KMnO4)、次氯酸(HClO)等强氧化剂还要强。高铁酸钠的的电离方程式是
(6)高铁酸钠之所以是水处理过程中使用的一种新型净水剂,原因是高铁酸钠中+6铁元素利用强氧化性杀菌消毒后转化为Fe(OH)3胶体,吸附水中悬浮物,达到既能杀菌消毒又能净水的目的,氢氧化铁胶体微粒直径的范围是
您最近一年使用:0次
2022-08-18更新
|
130次组卷
|
2卷引用:黑龙江省大庆市肇州县第二中学2021-2022学年高一上学期第一次月考化学试题
名校
2 . 铁作为生产、生活中的重要元素,下列方案设计、现象和结论均正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验铁锈中是否含有二价铁 | 将铁锈溶于浓盐酸,滴入酸性 溶液 溶液 | 紫色褪去,说明铁锈中含有二价铁 |
| B | 制备 胶体 胶体 | 向沸水中滴入几滴饱和 溶液,继续煮沸至产生红褐色沉淀,并用激光笔照射 溶液,继续煮沸至产生红褐色沉淀,并用激光笔照射 | 丁达尔效应,产生了胶体 |
| C | 配制 溶液 溶液 | 将 固体溶于较浓的盐酸中,再加水稀释至所需的浓度 固体溶于较浓的盐酸中,再加水稀释至所需的浓度 | 得到黄色溶液 |
| D | 比较 和 和 的氧化性强弱 的氧化性强弱 | 取适量 溶液于试管中,滴入 溶液于试管中,滴入 溶液,振荡,观察现象 溶液,振荡,观察现象 | 若产生气体使带火星的木条复燃,说明 的氧化性强于 的氧化性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究钠在氧气中燃烧所得固体成分 | 取少量加热后的固体粉末,加入少量蒸馏水 | 若有气泡产生,则证明燃烧后的固体粉末为Na2O2 |
| B | 比较KMnO4、Cl2 和Fe3+的氧化性 | 向酸性 KMnO4 溶液中滴入 FeCl2溶液,紫红色溶液变浅并伴有黄绿色气体产生 | 氧化性强弱:KMnO4>Cl2>Fe3+ |
| C | 制备 Fe(OH)3胶体 | 向沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。用红色激光笔照射液体 | 若产生一条光亮的“通路”,则得到Fe(OH)3 胶体 |
| D | 检验某溶液中是否存在K+ | 用玻璃棒蘸取待测液放在酒精灯外焰上灼烧,观察火焰的颜色 | 若看到火焰为黄色,则一定不存在 K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-27更新
|
210次组卷
|
2卷引用:山东省淄博实验中学2023-2024学年高一上学期期中考试化学试卷
名校
4 . 日常消毒应做到安全消毒、有效消毒、绿色消毒。下列是我们常见的几种消毒剂:
①“84”消毒液、②高铁酸钠 、③漂白粉、④
、③漂白粉、④ 、⑤
、⑤ 、⑥碘酒、⑦75%的酒精、⑧过氧乙酸(
、⑥碘酒、⑦75%的酒精、⑧过氧乙酸( ,是一种弱酸)。回答下列问题:
,是一种弱酸)。回答下列问题:
(1)上述物质中属于电解质的是______ (填标号);“84”消毒液的有效成分NaClO在水中的电离方程式为______ 。
(2)已知反应 ,则在该反应的条件下,氧化性:
,则在该反应的条件下,氧化性:
______ (填“>”或“<”) ,当反应中转移电子的数目为
,当反应中转移电子的数目为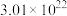 时,生成的氧气在标准状况下的体积为
时,生成的氧气在标准状况下的体积为______ L。
(3)高铁酸钠是一种新型净水剂,在水中发生反应: (胶体)
(胶体)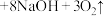 。
。
①该反应中,高铁酸钠中铁元素被______ (填“还原”或“氧化”)。
②某课外活动小组进行 胶体的制备及相关性质实验。
胶体的制备及相关性质实验。
制备:若将饱和 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是______ (填标号)。
A.冷水 B.沸水 C. 浓溶液 D.
浓溶液 D. 浓溶液
浓溶液
鉴别: 胶体与
胶体与 溶液的鉴别方法是
溶液的鉴别方法是______ 。
 胶体区别于
胶体区别于 溶液最本质的特征是
溶液最本质的特征是______ 。
①“84”消毒液、②高铁酸钠
 、③漂白粉、④
、③漂白粉、④ 、⑤
、⑤ 、⑥碘酒、⑦75%的酒精、⑧过氧乙酸(
、⑥碘酒、⑦75%的酒精、⑧过氧乙酸( ,是一种弱酸)。回答下列问题:
,是一种弱酸)。回答下列问题:(1)上述物质中属于电解质的是
(2)已知反应
 ,则在该反应的条件下,氧化性:
,则在该反应的条件下,氧化性:
 ,当反应中转移电子的数目为
,当反应中转移电子的数目为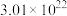 时,生成的氧气在标准状况下的体积为
时,生成的氧气在标准状况下的体积为(3)高铁酸钠是一种新型净水剂,在水中发生反应:
 (胶体)
(胶体)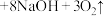 。
。①该反应中,高铁酸钠中铁元素被
②某课外活动小组进行
 胶体的制备及相关性质实验。
胶体的制备及相关性质实验。制备:若将饱和
 溶液分别滴入下列物质中,能形成胶体的是
溶液分别滴入下列物质中,能形成胶体的是A.冷水 B.沸水 C.
 浓溶液 D.
浓溶液 D. 浓溶液
浓溶液鉴别:
 胶体与
胶体与 溶液的鉴别方法是
溶液的鉴别方法是 胶体区别于
胶体区别于 溶液最本质的特征是
溶液最本质的特征是
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 比较 和 和 的 的 | 向盛有 溶液的试管中先加入足量 溶液的试管中先加入足量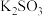 溶液,滤出沉淀后,向沉淀中加入 溶液,滤出沉淀后,向沉淀中加入 溶液,观察现象 溶液,观察现象 |
| B | 配制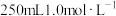 的NaOH溶液 的NaOH溶液 | 将10gNaOH固体放入小烧杯中溶解,转移至250mL容量瓶中,定容 |
| C | 验证 的还原性 的还原性 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液中,观察颜色变化 |
| D | 制备氢氧化铁胶体 | 向沸水中滴入5~6滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,停止加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 按要求填空。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是__________________ 。
(2) 的俗名
的俗名____________ ,在食品行业中常用于___________ ,其电离方程式___________ 。
(3)明矾的化学式为___________ ,明矾可做净水剂的理由是______________ 。
(4) 、
、 、
、 为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是______________ ,工业上冶炼铁的原理为 。该反应中氧化剂是
。该反应中氧化剂是___________ (填化学式),碳元素被____________ (填“氧化”或“还原”) 。
(5)84消毒液(NaClO)和洁厕灵(HCl)混合会产生有毒气体,不能混合使用,用离子方程式表示其理由:________________ 。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)
 的俗名
的俗名(3)明矾的化学式为
(4)
 、
、 、
、 为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是 。该反应中氧化剂是
。该反应中氧化剂是(5)84消毒液(NaClO)和洁厕灵(HCl)混合会产生有毒气体,不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
解题方法
7 . 按要求回答问题
Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。
现有以下物质:①固体NaHCO3 ② ③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
(1)以上物质中属于混合物的是_______ (填序号);
(2)写出①在水溶液中的电离方程式_______ ;
(3)④的实验室制备方案:向沸水中滴加几滴_______ 溶液,加热至液体呈红褐色,停止加热。
Ⅱ.空气与我们的生活息息相关。 是主要的大气污染物之一,
是主要的大气污染物之一, 是主要的温室气体。双碱法脱硫过程如图所示。
是主要的温室气体。双碱法脱硫过程如图所示。

(4)SO2属于_______ (填“酸性”或“碱性”)氧化物。过程Ⅰ发生的离子方程式是_______ 。
(5)下列反应中,能用同一离子方程式表示的是_______(填序号)。
(6)用化学方程式表示过程Ⅱ发生的化学反应_______ 。
Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。
现有以下物质:①固体NaHCO3 ②
 ③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖(1)以上物质中属于混合物的是
(2)写出①在水溶液中的电离方程式
(3)④的实验室制备方案:向沸水中滴加几滴
Ⅱ.空气与我们的生活息息相关。
 是主要的大气污染物之一,
是主要的大气污染物之一, 是主要的温室气体。双碱法脱硫过程如图所示。
是主要的温室气体。双碱法脱硫过程如图所示。
(4)SO2属于
(5)下列反应中,能用同一离子方程式表示的是_______(填序号)。
A. 和稀 和稀 | B. 和稀 和稀 |
C. 与稀 与稀 | D. 与稀 与稀 |
(6)用化学方程式表示过程Ⅱ发生的化学反应
您最近一年使用:0次
2022高三·全国·专题练习
解题方法
8 . 氯化铁溶液有较强氧化性,故可用作净水剂。(______)
您最近一年使用:0次
名校
9 . 有以下物质:①石墨②铁③蔗糖④一氧化碳⑤氯化铁固体⑥碳酸氢钠固体⑦氢氧化钡溶液⑧ ⑨熔融氯化钠⑩液态氯化氢
⑨熔融氯化钠⑩液态氯化氢
(1)其中能导电的是___________ (填序号,下同);属于非电解质的是___________ ;属于弱电解质的是___________ 。
(2)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:___________ 。
(3)写出用⑤的饱和溶液制备 胶体的化学方程式:
胶体的化学方程式:___________ 。
(4)已知 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
易溶于水,外观和食盐相似,有咸味,人误食会中毒。 能发生反应:
能发生反应: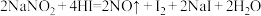 。淀粉遇碘单质会变蓝色,则鉴别
。淀粉遇碘单质会变蓝色,则鉴别 固体和NaCl固体,选用的物质为
固体和NaCl固体,选用的物质为___________ (填标号)。
a.水 b.淀粉―碘化钾溶液 c.白醋 d.白酒
某工厂的废液中含有2%~5%的 ,直接排放会造成污染。下列试剂中:a.NaCl;b.
,直接排放会造成污染。下列试剂中:a.NaCl;b. ;c.
;c. ;d.浓
;d.浓 ,能使
,能使 转化为
转化为 的是
的是___________ (填序号)。
(5)酸性条件下,加热 和
和 混合溶液制备
混合溶液制备 ,同时产生一种黄绿色气体,该反应的离子方程式
,同时产生一种黄绿色气体,该反应的离子方程式___________ 。
(6)NaCN不慎泄露时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体 ,二者溶于水均呈碱性,该反应的离子方程式为
,二者溶于水均呈碱性,该反应的离子方程式为___________ 。
 ⑨熔融氯化钠⑩液态氯化氢
⑨熔融氯化钠⑩液态氯化氢(1)其中能导电的是
(2)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:
(3)写出用⑤的饱和溶液制备
 胶体的化学方程式:
胶体的化学方程式:(4)已知
 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
易溶于水,外观和食盐相似,有咸味,人误食会中毒。 能发生反应:
能发生反应: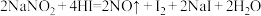 。淀粉遇碘单质会变蓝色,则鉴别
。淀粉遇碘单质会变蓝色,则鉴别 固体和NaCl固体,选用的物质为
固体和NaCl固体,选用的物质为a.水 b.淀粉―碘化钾溶液 c.白醋 d.白酒
某工厂的废液中含有2%~5%的
 ,直接排放会造成污染。下列试剂中:a.NaCl;b.
,直接排放会造成污染。下列试剂中:a.NaCl;b. ;c.
;c. ;d.浓
;d.浓 ,能使
,能使 转化为
转化为 的是
的是(5)酸性条件下,加热
 和
和 混合溶液制备
混合溶液制备 ,同时产生一种黄绿色气体,该反应的离子方程式
,同时产生一种黄绿色气体,该反应的离子方程式(6)NaCN不慎泄露时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体
 ,二者溶于水均呈碱性,该反应的离子方程式为
,二者溶于水均呈碱性,该反应的离子方程式为
您最近一年使用:0次
10 . 人类在四千五百多年前就开始使用铁器。铁是目前产量最大、使用最广泛的金属。下列关于铁及其化合物的说法正确的是
| A.常温下铁与水不反应,但红热的铁能与水蒸气发生反应,生成氧化铁和氢气 |
B.胶体是一种分散系,向沸水中滴加5~6滴 溶液,即可制得 溶液,即可制得 胶体 胶体 |
| C.由于蔬菜中的铁含量较少,吸收率低,所以食用蔬菜不是人体中铁的重要来源 |
D.新型绿色消毒剂高铁酸钠 主要用于饮用水处理,是因为其具有强氧化性 主要用于饮用水处理,是因为其具有强氧化性 |
您最近一年使用:0次



