名校
解题方法
1 . 有A、B、C、D四种有机物,A、B属于烃类物质,C、D都是烃的衍生物。A是含氢质量分数最大的有机物,分子结构为正四面体;B的球棍模型为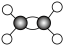 ;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为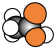 ,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
(1)A的电子式是___________ ,C中官能团的名称是___________ 。
(2)B的结构简式是___________ ,该物质发生加聚反应的化学方程式为___________ 。
(3)C与D在一定条件下反应生成一种有香味的物质,写出其化学方程式___________ 。
(4)下列说法正确的是___________ (填序号),
①B与其加聚反应产物组成元素及其原子个数比相同
②A与B都属于烃类,二者互为同系物
③C和D中都有—OH,其水溶液都显酸性
 ;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为 ,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:(1)A的电子式是
(2)B的结构简式是
(3)C与D在一定条件下反应生成一种有香味的物质,写出其化学方程式
(4)下列说法正确的是
①B与其加聚反应产物组成元素及其原子个数比相同
②A与B都属于烃类,二者互为同系物
③C和D中都有—OH,其水溶液都显酸性
您最近一年使用:0次
解题方法
2 . 利用零价铁(Fe)耦合过硫酸盐( )和过氧化氢产生自由基去除污水中的有机化合物是目前研究的热点。其中自由基
)和过氧化氢产生自由基去除污水中的有机化合物是目前研究的热点。其中自由基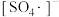 和HO·产生的机理如图所示。
和HO·产生的机理如图所示。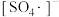 的结构式是
的结构式是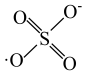 ,则
,则 的结构式是
的结构式是___________ 。
(2)过程ⅰ中反应的离子方程式是___________ 。
(3)过程ⅱ会导致溶液酸性增强,其中硫元素在反应前后均为+6价。该过程参与反应的物质还有(填化学式)___________ 。
(4)探究零价铁和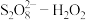 混合氧化剂体系降解水样中有机化合物M的能力。
混合氧化剂体系降解水样中有机化合物M的能力。
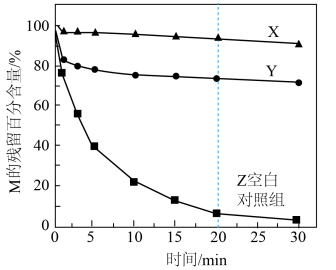
Ⅰ.通过加入甲醇或叔丁醇探究不同自由基降解M的能力。测得M的残留百分含量随时间变化如图所示。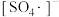 ,叔丁醇只消耗HO·
,叔丁醇只消耗HO·
a.X中加入的是___________ (填“甲醇”或“叔丁醇")。
b.0~20min,Z中降解M的自由基主要是HO·,判断依据是___________ 。
Ⅱ.探究混合氧化剂中 的物质的量分数对水样中总有机碳(TOC)去除率的影响。实验开始时,水样的pH=7且加入的
的物质的量分数对水样中总有机碳(TOC)去除率的影响。实验开始时,水样的pH=7且加入的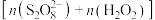 相同,其他条件不变。在相同时间内测得的实验数据如图所示。
相同,其他条件不变。在相同时间内测得的实验数据如图所示。
a.从①到④,TOC去除率升高的原因是___________ 。
b.从④到⑦,TOC去除率下降的原因是___________ 。
 )和过氧化氢产生自由基去除污水中的有机化合物是目前研究的热点。其中自由基
)和过氧化氢产生自由基去除污水中的有机化合物是目前研究的热点。其中自由基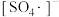 和HO·产生的机理如图所示。
和HO·产生的机理如图所示。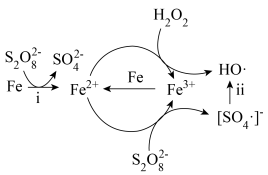
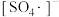 的结构式是
的结构式是 ,则
,则 的结构式是
的结构式是(2)过程ⅰ中反应的离子方程式是
(3)过程ⅱ会导致溶液酸性增强,其中硫元素在反应前后均为+6价。该过程参与反应的物质还有(填化学式)
(4)探究零价铁和
 混合氧化剂体系降解水样中有机化合物M的能力。
混合氧化剂体系降解水样中有机化合物M的能力。Ⅰ.通过加入甲醇或叔丁醇探究不同自由基降解M的能力。测得M的残留百分含量随时间变化如图所示。
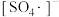 ,叔丁醇只消耗HO·
,叔丁醇只消耗HO·a.X中加入的是
b.0~20min,Z中降解M的自由基主要是HO·,判断依据是
Ⅱ.探究混合氧化剂中
 的物质的量分数对水样中总有机碳(TOC)去除率的影响。实验开始时,水样的pH=7且加入的
的物质的量分数对水样中总有机碳(TOC)去除率的影响。实验开始时,水样的pH=7且加入的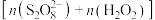 相同,其他条件不变。在相同时间内测得的实验数据如图所示。
相同,其他条件不变。在相同时间内测得的实验数据如图所示。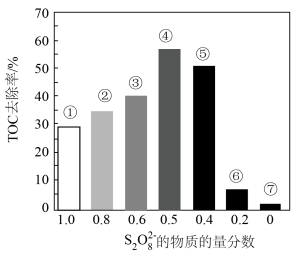
a.从①到④,TOC去除率升高的原因是
b.从④到⑦,TOC去除率下降的原因是
您最近一年使用:0次
名校
解题方法
3 . 已知氮元素及其化合物的转化关系如下图所示,回答下列问题。
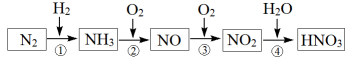
(1)氮气用于工业合成氨,写出氮气的电子式_______ ;
(2)①~④各步转化中,属于氮的固定的是_______ (填序号)。
(3)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
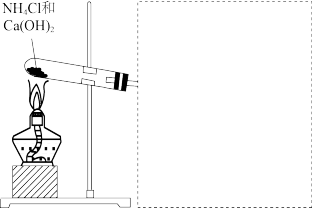
①化学方程式是_______ 。
②在图中方框内绘制用小试管 收集氨气的装置图__________ 。
(4)工业上用氨气制备NO的化学方程式是_______ 。
(5)工业制硝酸时尾气中含有NO、 ,可用NaOH溶液吸收,发生的反应有:
,可用NaOH溶液吸收,发生的反应有:
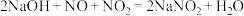
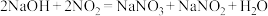
用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如下图:(
含量不同的尾气,关系如下图:( 表示尾气里NO、
表示尾气里NO、 中
中 的含量)
的含量)

i.根据上图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______ 。
(6)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),反应的化学方程式为
),反应的化学方程式为_______ 。若反应中有0.3mol电子发生转移时,生成亚硝酸的质量为_______ g(小数点后保留两位有效数字)。

(1)氮气用于工业合成氨,写出氮气的电子式
(2)①~④各步转化中,属于氮的固定的是
(3)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。

①化学方程式是
②在图中方框内绘制用
(4)工业上用氨气制备NO的化学方程式是
(5)工业制硝酸时尾气中含有NO、
 ,可用NaOH溶液吸收,发生的反应有:
,可用NaOH溶液吸收,发生的反应有: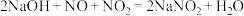
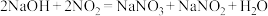
用不同浓度的NaOH溶液吸收
 含量不同的尾气,关系如下图:(
含量不同的尾气,关系如下图:( 表示尾气里NO、
表示尾气里NO、 中
中 的含量)
的含量)
i.根据上图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大ii.当α小于50%时,加入
 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(6)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),反应的化学方程式为
),反应的化学方程式为
您最近一年使用:0次
名校
4 . 图是自然界中氮循环的示意图。

(1) 的电子式是
的电子式是_______ ,氮气在常温下稳定,很难与 反应,说明断开其化学键所吸收的能量
反应,说明断开其化学键所吸收的能量_______ (填“大”或“小”)。
(2)“雷电作用”中氮元素发生了_______ 反应。(填“氧化”或“还原”)
(3)氮循环中,过程①②均会使水中溶解氧的含量_______ (填“增大”或“降低”)。
(4)长期饮用硝酸盐含量超标的水会对健康产生不利影响,某课题组在一定温度下,用铁粉降解水系中的 ,将之转化为
,将之转化为 。
。
①根据Ⅰ、Ⅱ可知, 降解速率的主要影响因素是
降解速率的主要影响因素是_______ 。
②Ⅱ中, 降解的速率为
降解的速率为_______  。(列式即可)
。(列式即可)
③Ⅱ中,铁粉还原 的离子方程式是
的离子方程式是_______ 。

(1)
 的电子式是
的电子式是 反应,说明断开其化学键所吸收的能量
反应,说明断开其化学键所吸收的能量(2)“雷电作用”中氮元素发生了
(3)氮循环中,过程①②均会使水中溶解氧的含量
(4)长期饮用硝酸盐含量超标的水会对健康产生不利影响,某课题组在一定温度下,用铁粉降解水系中的
 ,将之转化为
,将之转化为 。
。| 编号 |  浓度 浓度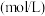 | 反应时间 |  初始浓度 初始浓度 |  终了浓度 终了浓度 |
| Ⅰ | 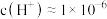 | 24 | 100 | 91 |
| Ⅱ | 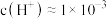 | 24 | 100 | 0 |
 降解速率的主要影响因素是
降解速率的主要影响因素是②Ⅱ中,
 降解的速率为
降解的速率为 。(列式即可)
。(列式即可)③Ⅱ中,铁粉还原
 的离子方程式是
的离子方程式是
您最近一年使用:0次
名校
5 . 人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)工业合成氨是制取氮肥的基础。合成氨反应中,反应物 N2的结构式是_______________ ,产物NH3的电子式是_________________ 。
(2)某小组在实验室模拟以 NH3为原料, 制备少量硝态氮肥 Ca(NO3)2,转化途径如下(转化所需试剂及条件已略去)。
NH3 NO
NO NO2
NO2 HNO3
HNO3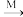 Ca(OH3)2
Ca(OH3)2
①NO→NO2的现象是______________ , NO2→HNO3的化学方程式为____________________ 。
②将HNO3转化为 Ca(NO3)2,列举两种不同类别的化合物 M___________________ (写化学式) 。
(3)①NH4HCO3是一种铵态氮肥,需阴凉处保存,原因是_______________ (写化学方程式)。
②实验室检验某化肥是铵态氮肥,检验过程中发生反应的离子方程式为___________________ 。
(4)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)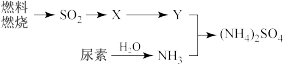
①X可能是SO3 或_______________ ,Y是_____________ 。
②尿素CO(NH2)2是一种常用有机氮肥,缓慢与 H2O 发生非氧化还原反应释放出NH3和另外一种气体,该反应的化学方程式为________________ 。
(1)工业合成氨是制取氮肥的基础。合成氨反应中,反应物 N2的结构式是
(2)某小组在实验室模拟以 NH3为原料, 制备少量硝态氮肥 Ca(NO3)2,转化途径如下(转化所需试剂及条件已略去)。
NH3
 NO
NO NO2
NO2 HNO3
HNO3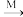 Ca(OH3)2
Ca(OH3)2①NO→NO2的现象是
②将HNO3转化为 Ca(NO3)2,列举两种不同类别的化合物 M
(3)①NH4HCO3是一种铵态氮肥,需阴凉处保存,原因是
②实验室检验某化肥是铵态氮肥,检验过程中发生反应的离子方程式为
(4)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
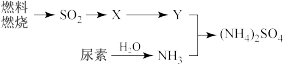
①X可能是SO3 或
②尿素CO(NH2)2是一种常用有机氮肥,缓慢与 H2O 发生非氧化还原反应释放出NH3和另外一种气体,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 短周期元素W、X、Y、Z的原子序数依次增大。W的气态氢化物遇湿润的红色石蕊试纸变蓝色,X是地壳中含量最高的元素,Y在同周期主族元素中原子半径最大,Z与Y形成的化合物的化学式为YZ。下列说法不正确的是
| A.W在元素周期表中的位置是第二周期第VA族 |
| B.同主族中Z的气态氢化物稳定性最强 |
| C.X与Y形成的两种常见的化合物中,阳离子和阴离子的个数比均为2∶1 |
D.用电子式表示YZ的形成过程为: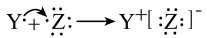 |
您最近一年使用:0次
2020-05-23更新
|
288次组卷
|
7卷引用:北京市西城区2020届高三一模化学试题
北京市西城区2020届高三一模化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:元素周期律 元素周期表北京市人大附中朝阳学校2019~2020年高一下学期阶段练习化学试题(选考班)北京市第一六六中学2023-2024学年高三上学期10月考月考化学试题 天津市大港油田实验中学2020届高三开学考试化学试题天津市第一中学2020届高三下学期第四次月考化学试题天津市第一中学2020届高三4月月考化学试题
解题方法
7 . “塑料袋——想说爱你不容易!”自1902年10月24日奥地利科学家马克斯•舒施尼发明它以来,也只有短短的一百多年时间。这些花花绿绿、大大小小的塑料袋,不仅破坏城市景观,对环境的危害也是极惊人的。2008年6月1日起,根据国务院要求,所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用。下列说法正确的是
A.聚丙烯塑料的结构简式为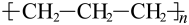 |
B.聚氯乙烯塑料单体的电子式为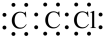 |
| C.塑料购物袋的生产原料需要消耗大量木材 |
| D.聚乙烯中含碳质量分数与其单体的含碳质量分数相同 |
您最近一年使用:0次



